レカネマブの米国における適正使用ガイドラインでは「安全性確保のために遺伝子検査(ApoE遺伝子型)が推奨される」と記載されています.今後発表される日本のガイドラインでどうなるかが注目されます.当科のカンファレンスで「なぜApolipoprotein E(ApoE)遺伝子遺伝子検査が重要なのか?」を解説しました.結論として,まず正しい情報をみんなが共有することが重要ということで意見が一致しました.
【なぜApoE4遺伝子検査が必要なのか?】
ApoE遺伝子にはε2,ε3,ε4の3種類の型があり,両親から1つずつ受け継ぐため,ε2/ε2,ε2/ε3,ε2/ε4,ε3/ε3,ε3/ε4,ε4/ε4の6パターンに分類されます.ε2はアミロイドβ(Aβ)の凝集を抑えますが,ε4を持つとリスクが高まります.1つ持つと(ヘテロ接合)3倍,2つ持つと(ホモ接合)12倍の発症リスクがあると言われています.ε4/ε4は全人口では1%程度と言われますが,アルツハイマー病患者の集団では当然頻度が高まります.
アルツハイマー病の進行抑制効果をもつレカネマブやドナネマブは,ともにアミロイドβに対する抗体薬です.急速かつ長期に脳からAβを除去することが重要ですが,この作用が強いため血管壁に沈着したアミロイドβも除去します.この際,おそらく血管(血液脳関門)の破綻が生じ,頭部MRIでアミロイド関連画像異常(amyloid–related imaging abnormalities:ARIA)と呼ばれる脳の浮腫性変化(ARIA–E)や出血性変化(ARIA–H)が生じます(図1).ARIAには症状を伴うことがあります(症候性ARIA).また無症状であっても長期的にこれらの変化が認知機能にどのような影響をもたらすのかがまだ分かっていません.

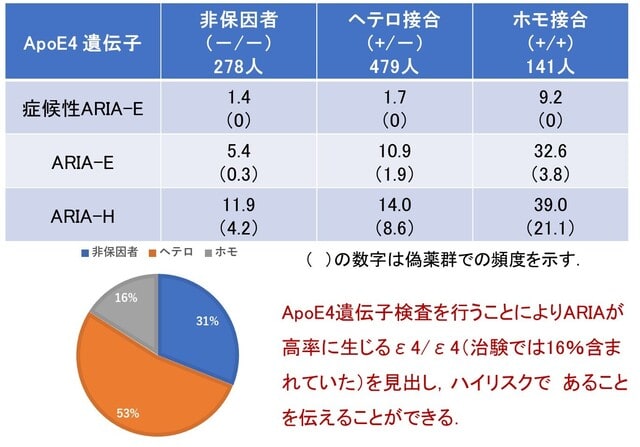
ここで重要なのはARIAの出現頻度が,ApoE遺伝子のε4の保有により大きく変わってくるということです.表1と表2はレカネマブとドナネマブによるARIAの発生率をApoE遺伝子のε4の個数により3つ(0個,1個,2個)に分類してまとめたものです.レカネマブは,ホモ接合(2個)の患者に使用した場合,症候性ARIA-Eは9.2%,ARIA-E全体は32.6%,ARIA-Hを39.0%で生じます(図2).この頻度は非保因者(0個)で使用した場合と比べて順に6.6倍,6.0倍,3.3倍高いことになります.
より切れ味の鋭いドナネマブはARIA-E全体は40.6%,ARIA-Hは50.3%で生じます(図3).

そうなると合併症リスクが高いε4/ε4の患者の頻度が問題になりますが,レカネマブ研究で16%,ドナネマブ研究で17%存在しています.よって治験患者の2割弱がハイリスク群となるわけです.これらの患者群は,おそらく脳梗塞治療に対して使用される抗凝固薬や血栓溶解薬rt-PAでも出血合併症が生じるリスクが高いです.このようなリスクの高い患者さんにはその情報を伝えた上で,治療の適応を考えるべきです.これがオバマ大統領が発表して有名になった「プレシジョン・メディシン」の考え方に沿った医療と言えます(遺伝子などを調べ,個人レベルで最適な治療を行うという先端治療の考え方です).米国同様,日本でもApoE4遺伝子検査を行うべきと考えますが,反対とする意見もあります.なにが問題なのか,次回,考察します.
Cummings, J., Apostolova, L., Rabinovici, G.D. et al. Lecanemab: Appropriate Use Recommendations. J Prev Alzheimers Dis (2023).
van Dyck CH, et al. Lecanemab in Early Alzheimer’s Disease. N Engl J Med. 2023 Jan 5;388(1):9-21.(doi.org/10.1056/NEJMoa2212948)
Sims JR, et al. Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA. 2023 Aug 8;330(6):512-527.(doi.org/10.1001/jama.2023.13239.)
DiFrancesco JC, et al. Anti-Aβ Autoantibodies in Amyloid Related Imaging Abnormalities (ARIA): Candidate Biomarker for Immunotherapy in Alzheimer's Disease and Cerebral Amyloid Angiopathy. Front Neurol. 2015 Sep 25;6:207.(doi.org/10.3389/fneur.2015.00207)
【なぜApoE4遺伝子検査が必要なのか?】
ApoE遺伝子にはε2,ε3,ε4の3種類の型があり,両親から1つずつ受け継ぐため,ε2/ε2,ε2/ε3,ε2/ε4,ε3/ε3,ε3/ε4,ε4/ε4の6パターンに分類されます.ε2はアミロイドβ(Aβ)の凝集を抑えますが,ε4を持つとリスクが高まります.1つ持つと(ヘテロ接合)3倍,2つ持つと(ホモ接合)12倍の発症リスクがあると言われています.ε4/ε4は全人口では1%程度と言われますが,アルツハイマー病患者の集団では当然頻度が高まります.
アルツハイマー病の進行抑制効果をもつレカネマブやドナネマブは,ともにアミロイドβに対する抗体薬です.急速かつ長期に脳からAβを除去することが重要ですが,この作用が強いため血管壁に沈着したアミロイドβも除去します.この際,おそらく血管(血液脳関門)の破綻が生じ,頭部MRIでアミロイド関連画像異常(amyloid–related imaging abnormalities:ARIA)と呼ばれる脳の浮腫性変化(ARIA–E)や出血性変化(ARIA–H)が生じます(図1).ARIAには症状を伴うことがあります(症候性ARIA).また無症状であっても長期的にこれらの変化が認知機能にどのような影響をもたらすのかがまだ分かっていません.

ここで重要なのはARIAの出現頻度が,ApoE遺伝子のε4の保有により大きく変わってくるということです.表1と表2はレカネマブとドナネマブによるARIAの発生率をApoE遺伝子のε4の個数により3つ(0個,1個,2個)に分類してまとめたものです.レカネマブは,ホモ接合(2個)の患者に使用した場合,症候性ARIA-Eは9.2%,ARIA-E全体は32.6%,ARIA-Hを39.0%で生じます(図2).この頻度は非保因者(0個)で使用した場合と比べて順に6.6倍,6.0倍,3.3倍高いことになります.

より切れ味の鋭いドナネマブはARIA-E全体は40.6%,ARIA-Hは50.3%で生じます(図3).

そうなると合併症リスクが高いε4/ε4の患者の頻度が問題になりますが,レカネマブ研究で16%,ドナネマブ研究で17%存在しています.よって治験患者の2割弱がハイリスク群となるわけです.これらの患者群は,おそらく脳梗塞治療に対して使用される抗凝固薬や血栓溶解薬rt-PAでも出血合併症が生じるリスクが高いです.このようなリスクの高い患者さんにはその情報を伝えた上で,治療の適応を考えるべきです.これがオバマ大統領が発表して有名になった「プレシジョン・メディシン」の考え方に沿った医療と言えます(遺伝子などを調べ,個人レベルで最適な治療を行うという先端治療の考え方です).米国同様,日本でもApoE4遺伝子検査を行うべきと考えますが,反対とする意見もあります.なにが問題なのか,次回,考察します.
Cummings, J., Apostolova, L., Rabinovici, G.D. et al. Lecanemab: Appropriate Use Recommendations. J Prev Alzheimers Dis (2023).
van Dyck CH, et al. Lecanemab in Early Alzheimer’s Disease. N Engl J Med. 2023 Jan 5;388(1):9-21.(doi.org/10.1056/NEJMoa2212948)
Sims JR, et al. Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA. 2023 Aug 8;330(6):512-527.(doi.org/10.1001/jama.2023.13239.)
DiFrancesco JC, et al. Anti-Aβ Autoantibodies in Amyloid Related Imaging Abnormalities (ARIA): Candidate Biomarker for Immunotherapy in Alzheimer's Disease and Cerebral Amyloid Angiopathy. Front Neurol. 2015 Sep 25;6:207.(doi.org/10.3389/fneur.2015.00207)

























