既述のページへのリンク: ①炭素という名称の起源 ②炭素の認識:木炭は何故炭素なのか ③元素としての炭素の性質 ④炭素の誕生 ⑤宇宙の炭素 ⑥原始太陽系の炭素 ⑦炭素と有機物 ⑧炭素原子とメタン分子 ⑨炭化水素分子内での炭素の結合 ➉分子内での炭素と酸素の共有結合 ⑪窒素の形成と水素と炭素と酸素 ⑫窒素を含んだ有機化合物と無機化合物 ⑬星(恒星)と炭素 ⑭炭化水素分子内での炭素―炭素結合と電子 ⑮複雑な構造の炭化水素、⑯複素環式化合物、⑰炭素化合物の多様性、⑱炭素原子と星間分子
------------------ーーーーーーーーーーー
ビッグバンから少し時間が経過した時、水素原子(H) ができ宇宙にばらまかれた。宇宙における水素の分布は均一でなく、濃度の高いところでは集合が進み濃密な原子の集団ができた。集団がある程度の大きさを持つと、内部で水素がぶつかり合うことによって核融合反応が起こり、恒星として輝き、内部ではヘリウム(He)ができた。この水素とヘリウムでできた星を第一世代の星と呼ぶことがある。第一世代の星はその大きさにより内部で形成できる元素が異なり、星としての進化の終末も異なる。第一世代の星の超新星爆発や質量放出により宇宙にばらまかれた元素が再度集合し、第二世代の星を形成した。星の質量が太陽の50%より大きいと、内部で炭素(C)、酸素(O)、窒素(N)の核合成が進行し、再度の超新星爆発などにより、宇宙空間に様々な元素を放出した。第二世代の星誕生以降、元素の集合による星形成、核融合による新しい元素の合成、超新星爆発などによる宇宙空間への元素の放出は繰り返し行われた。このプロセスの中で、現在地球上に存在する全ての元素が作られた(放射性崩壊によって地球上で作られる元素は、宇宙空間でも同じプロセスで作られる)。星の内部や衝撃波表面のような超高温・超高圧条件下では、原子は単体で存在するが、原子を放出する星の周辺の冷却された大気では、分子が形成された。
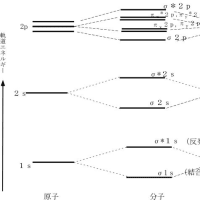
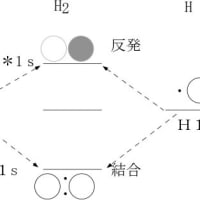
ヘリウムのような希ガス元素(単原子分子)を除いて、単体の原子は、他の原子と衝突すると、比較的低いエネルギー(核融合に必要なエネルギーに比べるとはるかに小さい)で反応して、複数の原子よりなる分子(多原子分子)を形成する。分子は単体の原子として存在するより、エネルギー的に安定に存在し得る。宇宙空間へ放出されて間もないころや、星形成へ向かって原子が再集合し始めている場所では、原子の濃度が高いので原子どうしが衝突する機会が多くあり、そこでは様々な種類の分子が形成される。ただし、分子が高エネルギーの場にさらされると分解して原子に戻る。
第一世代の星から放出される分子は水素分子(H2)であるが、第二世代の星からは、星の大きさによって形成される元素が異なるため、放出される分子も異なってくる。水素やヘリウムに次いで出現する安定な元素は炭素(C)である。ただし、炭素(C)が出来る時には酸素(O)も創られる場合が普通で、さらにCNOサイクルによって窒素(N)も作られるが、それらの元素の相対的な量で、形成される分子の種類が異なってくる。炭素の量が他の元素より多い星は炭素星と呼ばれるが、それには、幾つかの異なった種類が存在する。炭素星では、炭素どうしが反応したC2が存在し、その他にCO、 CH、CN、C3、SiC2などの分子も存在する。ここで、元素記号の右下に付した数字は、1個の分子に含まれる元素の数を示している(ただし、1は省略)。
星間空間に存在する分子は星間分子と呼ばれる。宇宙空間(星間空間)では、原子や分子の濃度が極端に低くいため、相互に衝突して反応する機会は少なく、温度も非常に低いため、地球上には通常存在しない様々な不安定な分子も多種存在する。炭素は宇宙における原子形成の早い段階から存在し、かつ存在量も大きい。さらに炭素は共有結合を介して異なった構造を持った無数の安定な分子を形成できるという他の元素には無い性質を持っている。これらの性質のため、炭素を含んだ分子は星間分子の主成分となっている。炭素を含まない星間分子は2個の原子が結合した分子(2原子分子)としては比較的多種類(OH、N2、O2、NaCl・・・等々)存在するが、3個以上の原子が結合した分子には炭素を含んだものが圧倒的に多い。原子を10個以上含んだものとして、ベンゼン(C6H6)、メチルトリアセチレン(C7H4)、ナフタレン(C10H8)なども存在する。星間分子は電波による天体観測によってその存在が決定される。
星間分子の濃度が上がると光の透過が困難となり、暗黒星雲として観測される。これは星が形成される前段階である。そこには分子同士が衝突して反応して新しい分子を形成する機会がある。しかし、暗黒星雲の中に存在する分子の持つエネルギーは小さい。そのため分子同士が衝突しても、中性の分子どうしでは、反応して新しい分子を作る前に反発して離れてしまう。ところが、衝突する分子の一方がイオン化している場合には、ほとんど相互に反発することなく衝突する。これはイオン分子反応と呼ばれるもので、星間分子の間で起こる主たる反応であるとされている。分子雲内で起こっていると推定されるイオン分子反応の主なものとして以下の式に表わされるものがある。ただし、右肩の(+)の記号は原子または分子が1個の陰電子を失って、一価の陽イオンとなっていることを示す。
C+ + H2 → CH+ + H
CH+ + H2 → CH2+ + H
CH2+ + H2 → CH3+ + H
炭素を含んだ主な星間分子は以下のとおりである。ただし、1個の分子の中で同じ元素が別々に書かれている場合は、構造上の特徴を強調するためである。例えば、CH3はメチル基という特定の構造が分子の中に存在することを示す。
CO、CS、C2、OCS、CH4、C3、C5、C3O、C3S、C4Si、HCN、HC3N、HC5N、HC7N、HC9N、HC11N 、HC2CHO、CH3CN、CH3C3N、CH3C2H、CH3C4H、CH3CH2CN、CH2CHCN、HNC、HNCO、HNCS、HNCCC、CH3NC、HCCNC、C2H4、C2H2、H2CO、H2CS、CH3CHO、NH2CHO、CH3OH、CH3CH2OH、CH3SH、HCOOH、HCOOCH3、(CH3)2O、H2CCO、CH2NH、CH3NH2、NH2CN、CH2CC、CH2CCC、C3H2、SiC2、c-C3H、CH+、HCO+、HCNH+、H3O+、HN2+、HCS+、HOCO+、SO+、CH、C2H、C3H、C4H、C5H、C6H、CN、C3N、HCCN、CH2CN、C2O、HCO、C2S、SiC、CP
















※コメント投稿者のブログIDはブログ作成者のみに通知されます