既述のページへのリンク: ①炭素という名称の起源 ②炭素の認識:木炭は何故炭素なのか ③元素としての炭素の性質 ④炭素の誕生 ⑤宇宙の炭素 ⑥原始太陽系の炭素 ⑦炭素と有機物 ⑧炭素原子とメタン分子 ⑨炭化水素分子内での炭素の結合 ➉分子内での炭素と酸素の共有結合 ⑪窒素の形成と水素と炭素と酸素 ⑫窒素を含んだ有機化合物と無機化合物 ⑬星(恒星)と炭素 ⑭炭化水素分子内での炭素―炭素結合と電子 ⑮複雑な構造の炭化水素、⑯複素環式化合物、⑰炭素化合物の多様性、⑱炭素原子と星間分子
------------------ーーーーーーーーーーー
有機化合物の分子としての基本は炭化水素である。炭化水素の原料である水素と炭素は宇宙における元素形成の極初期から存在する。さらに、炭化水素分子に結合することによって有機化合物に多様な変化をもたらす酸素や窒素も、宇宙における元素合成の早い段階で形成される。従って宇宙には様々な有機化合物が存在する可能性がある。ただし、有機化合物の基本単位である有機分子が形成されるためには、炭素原子が自分以外の原子と結合する必要がある。
分子を形成する原子の間の結合には電子が介在する。元素の合成が進行している場では原子核が単独で存在する。原子核が電子と結合して原子となるのは、核合成の場から離れて温度が下がってからである。原子は直径が0.1~0.2nm(nm=10-9m、1億分の1メートル)ぐらいの電気的に中性で丸くて硬い極微の物体とみなすことができる。原子どうしが0.5nm以上離れていると、原子間に引力も斥力も働かない。ところが原子が触れ合う距離になった時、突然、強い引力や斥力が現れる。原子同士が斥力を乗り越えて接近するとお互いの電子を共有したり、融通しあったりして原子間の結合を形成し、分子が作られる。
宇宙のどのような場所にどのような種類の有機分子が存在するかは、炭素の置かれた環境(どのような元素がどのような形と濃度で共存し、どのような種類と強度のエネルギーにさらされているか)によって左右される。比較的小さな有機分子は宇宙空間における炭素星の大気成分や宇宙空間の星間分子として、地球から観測可能な濃度で存在しているものもある。現在我々が知っている天体で、最も多種類の有機化合物が存在するのは地球である。それは、地球に生命が誕生したことに起因するが、その元を辿れば、有機分子が安定に存在するのに適した環境に地球があるからであ。そして、そこに存在する非常に低濃度の分子でも、我々から近距離に存在するため、多種多様な手段を用いて観測し同定することが可能であることによって、存在が確認できる分子の種類が膨大なものとなっているからである。
有機化合物の基本である炭化水素で構造的に最も単純なものは直鎖状飽和炭化水素と呼ばれるもので、炭素と炭素が単結合で一本の鎖状に繋がれたものである。これを元素の数で一般的な形で表すとCnH2n+2(n=1,2,3,・・・)。と表現される分子である。個々の分子はギリシャ語(一部はラテン語)の数詞によって炭素の数を表す固有の名称を持っていて、下の表にその例を示す。これらの名称は日本語の表現では分かりにくいが、語尾はアンとなっていて飽和炭化水素を意味している。例えばヘキサン(hexane)はヘキサ(6)+アン(飽和炭化水素)である。
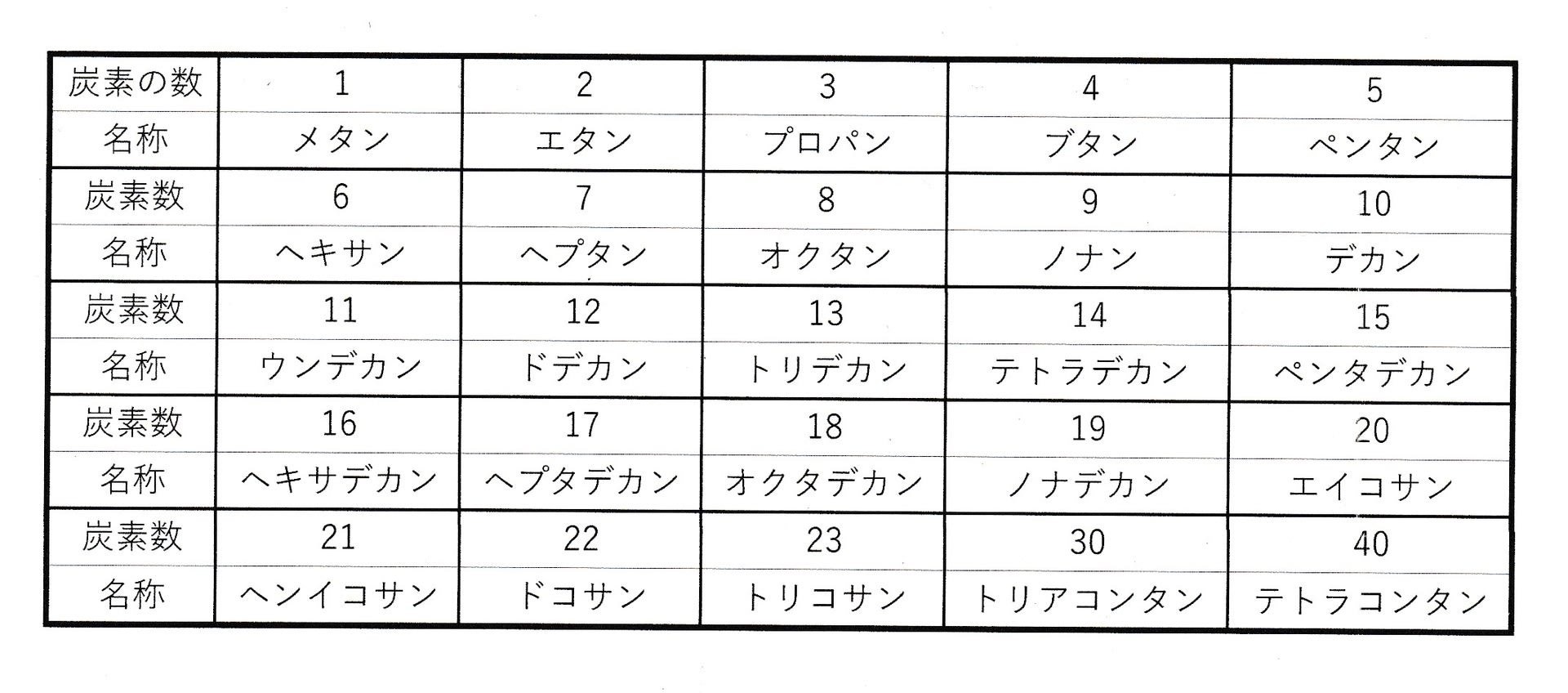
下図に直鎖状炭化水素の構造式の例を示した。直鎖状飽和炭化水素の炭素と炭素の結合は、結合を軸にして自由に回転ができるので、分子内の結合していない原子同士の反発が最も少ない安定な三次元構造が主体となる。モデル計算で導かれる安定な分子モデルを示したが、原子同士の相対位置が見えるように眺める位置と原子の相対的大きさは調整してある。
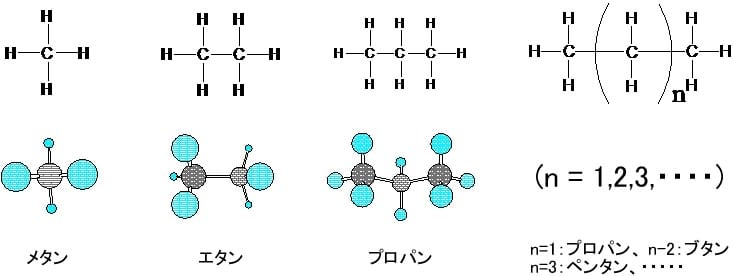
炭化水素における炭素と炭素の結合の仕方には単結合の他に二重結合と三重結合が存在し、二重結合や三重結合を含む炭化水素を不飽和炭化水素と呼ぶ。古典的共有結合論による平面構造式では、構造や反応を分かりやすく表現するために、これらの炭素と炭素の結合を直線の本数で表す。量子論による電子軌道の表現では、単結合は原子間に新しく形成された一つの電子軌道に、結合する原子がお互いに一つずつ電子を出し合って結合するもので、σ(シグマ)結合と呼ばれる。二重結合ではσ結合を形成するsp2混成軌道の他に、各炭素原子に存在する1個の電子軌道(p軌道)が重なり合って相互作用することによって作られるπ(パイ)結合と呼ばれる結合が、一つ加わる。三重結合ではσ結合を形成するsp混成軌道の他に各炭素原子に存在する2個のp軌道が相互作用して二重にπ結合が形成され、結果としてσ結合の周りに円筒形の電子雲を作る。それぞれの結合の電子分布の様子を下図に示す。

σ結合とπ結合では結合の性質が異なり、σ結合はπ結合に比べて結合力が強く、π結合はσ結合に比べて結合力は弱いが反応性が高い。σ結合は、結合軸にそって新しく形成された直線的電子軌道であるため、周辺に障害となる条件が無ければ、結合軸を回転軸にして自由に回転できる。それに対してπ結合は、原子が個別に持っているp電子軌道の側面の重なりによって形成される。p軌道にはσ結合と直交した方向性があり、軌道の重なりを最大にするためには特定の方向がある。このことにより結合軸の周りの回転が制限される。これらのことが、分子の構造と反応性に大きく影響する。三重結合はπ電子雲が結合軸を取り囲む円筒形に均等に分布する。炭素結合に関与する電子は単結合、二重結合、三重結合の順に多くなり、原子間の結合の強さはその分だけ強くなる
IUPACの命名規則によれば、二重結合を含む炭化水素は、相当する飽和炭化水素の接尾語のアンをエンとし、三重結合を含む炭化水素はインとすることになっている。炭素の数に拘らない炭化水素の一般名称として飽和炭化水素をアルカンと言い、二重結合を含んだ炭化水素をアルケン、三重結合を含んだ炭化水素をアルキンと言う。炭素2個からなる和炭化水素はエタンであり、不飽和炭化水素としては、二重結合を含むとエテン、三重結合を含むとエチンと呼ばれることになる。ただし、エテンはエチレン、エチンはアセチレンという慣用名が広く使われている。σ結合はπ結合に比べて結合エネルギーが非常に大きいため、不飽和化合物では、σ結合は分子の骨格を形成し、π電子は活性な電子として働く。炭素2個よりなる分子の平面構造式、並びに原子と結合を球と棒で表したボール・スティックモデル及び相当する模型を覆う電子の分布の様子を示したスペースフィリングモデルで、分子を見る角度を変えて示すと下図のようになる。

炭素を4個以上含む直鎖状炭化水素分子でその鎖に不飽和結合が存在する場合には、分子内におけるその存在位置で異なった化合物(異性体)となる場合がるため、その存在位置を明示することが必要となる。そのため、鎖の端から順に炭素に番合を付けて、不飽和結合を含む炭素の番号が一番小さくなるように命名する。4個の炭素原子からなる直鎖状炭化水素は飽和していればブタンであり、二重結合を一つ含むとブテン、三重結合を一つ含むとブチンとなる。ブタンの場合に端から番号を付けると、1番目から4番目の炭素があることになる。不飽和結合が存在している場合、その位置を示す炭素の番号が小さくなるようにする。ブテンの場合は炭素1と炭素2の間に二重結合が有ると接頭辞として最小位置番号としての 1を付けて1-ブテンとする。ただし、IUPAC1993年規則によると、同一の鎖上に複数の不飽和結合が存在する場合を考慮して、二重結合、三重結合の位置番号は、相当する接尾語の前に記すこととなっているので、ブタ―1-エンとなる。しかし、1-ブテンの方が通俗的に使われている。2番目と3番目の炭素の間に二重結合があると2-ブテンとなる。3番目と4番目の炭素の間に二重結合が存在する場合には、1番目と2番目の炭素の間に二重結合があるものと同一となるので1-ブテンである。
2-ブテンの場合には、二重結合の両端にメチル基が存在するが、二重結合は結合軸を中心にした分子内での回転ができないため、メチル基の空間的相対的位置によって異なった性質を示す化合物(幾何異性体)となり、「トランス―」及び「シス―」の接頭語を付けて区別する。ブテンの平面構造と分子モデルを示すと下図のようになる。なお、トランス―、シス―の位置関係を、分子内のもっと複雑な位置関係に一般的に適応させるためにはE,Z命名法が用いられる。

同一の直鎖炭化水素分子の中に複数の不飽和結合が存在する場合には、不飽和結合の位置と共に個数も示す。不飽和結合の個数を示す数詞にはモノ(1個:通常は略)、ジ(2個)、トリ(3個)、ブタ(4個)、ペンタ(5個)・・・(以下は直鎖状炭化水素の炭素の数を示す数詞と同じ数詞を使う)。二重結合と三重結合が共存する場合には、二重結合のエンと三重結合のインをつないでエンインの接尾語を使うがそれぞれの接尾語の前に個数を示す接頭語と位置を示す数字を付ける。ヘキサンを例に示すと以下のようになるが、ここでは二重結合に関する幾何異性体は省略してある。二段に名称が書いてある場合には、上段が通俗的に使われている名称で、下段はIUPAC1993の命名法によるものである。
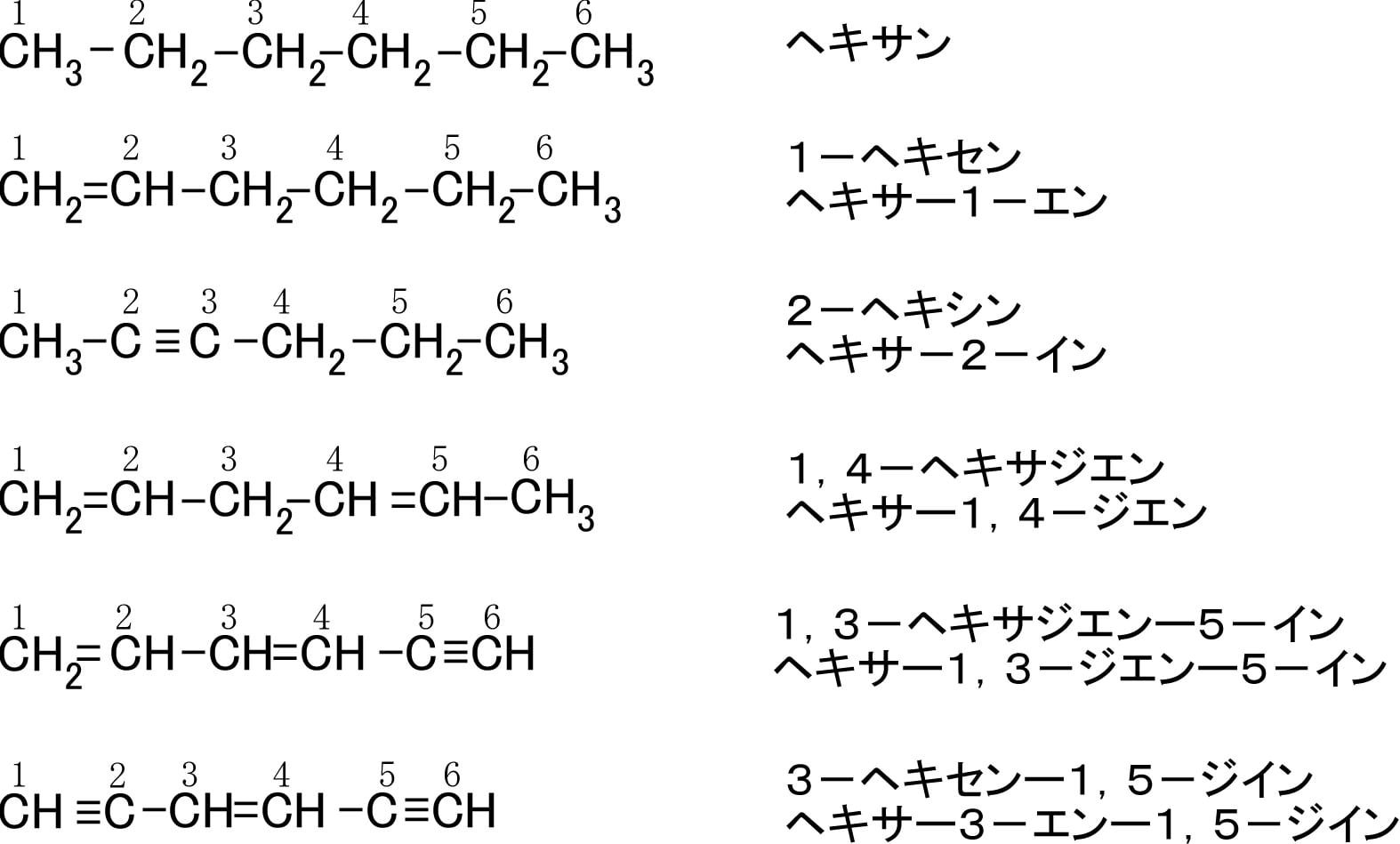
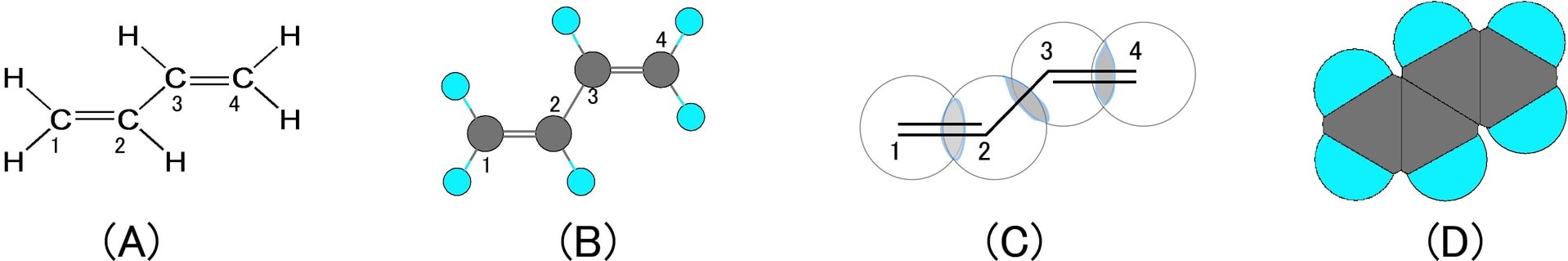
ブタンに二重結合が二つ存在する分子に1,3-ブタジエン(下図)がある。通常その構造は、1位と2位の炭素及び3位と4位の炭素がそれぞれ二重結合で結ばれ、2位と3位の炭素が単結合で結ばれた構造式(下図のA)で表される。ボール・スティック分子モデル(下図のB)でも1位と2位の炭素間及び3位と4位の炭素間の結合は二重結合で表現され、2位と3位の炭素間の結合は単結合で表される。従って、炭素2と炭素3は、障害物が無ければ、結合軸を中心に自由に回転できるはずである。ところが、実際の分子は全体が平面に固定されている。これは、2位の炭素のp電子軌道と3位の炭素のp電子軌道が炭素骨格の図(下図のC)で示したように重なりあっていてπ結合を作り得る状態にあることに起因している。実際に1本の単結合を挟んで2本の二重結合がある場合に、二重結合を形成しているπ電子は非局在化して、4個の炭素原子全体に分布する。このように配置された二重結合を共役していると言い、一般的に複数の二重結合が共役している系を共役系と呼ぶ。
共役ジエンを原子価結合構造で示すと、下図のⅠとⅡの共鳴混成体で表される。Ⅱの点線は形式結合を表していて、C1の電子とC4の電子は互いにスピンが逆で対をなしていることを意味している。Ⅱが共役ジエン構造に寄与する分だけ、C2-C3結合が二重結合性を帯び、またC1-C2結合とC3-C4結合が単結合性を帯びる。結果としてⅠの構造単独から推定されるものに比べてより安定な分子となる。このような分子の電子軌道を非局在化分子軌道と呼ぶ。

炭化水素には鎖状分子の両端の炭素が結合して輪を作った脂環式化合物(環状炭化水素)と呼ばれる炭化水素分子も存在する。この場合には、相当する直鎖状炭化水素の名称にシクロという接頭辞を付ける。例えば、3個の炭素からなるシクロプロパン、4個の炭素からなるシクロブタン、5個の炭素からなるシクロペンタン、6個の炭素からなるシクロヘキサンなどである。これらの分子を平面構造式と分子モデルで表すと下に示すようになる。図の分子モデルには平面構造の示す面の真上から見たものと真横から見たものが示してある。
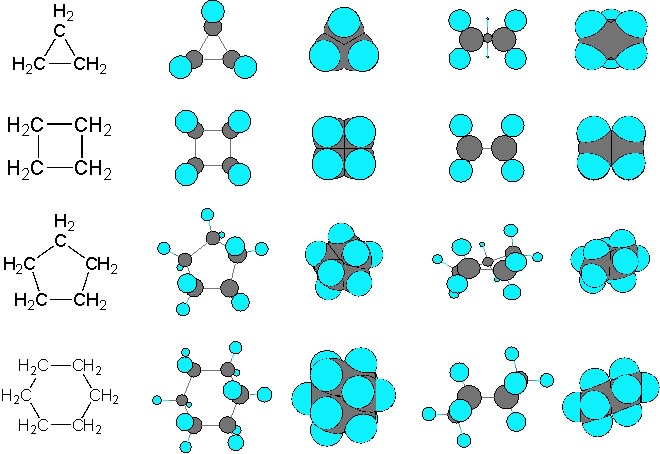
シクロプロパンとシクロブタンの立体構造の炭素骨格は平面である。この骨格を形成している炭素の結合の角度はsp3混成軌道のものとかなり異なっている。そのためこれらの分子には本来のsp3混成軌道の形に戻ろうとする力が働き不安定となっている。それに対して、シクロヘキサンの場合には、炭素骨格は三次元構造になっていて、全ての炭素が水素の配置も含めて完全にsp3混成軌道の形を満たした構造をとり得る。そのため、環状の飽和炭化水素の中では安定なものとなっている。
シクロヘキサンに二重結合が一つ存在するとシクロヘキセンとなり、二つ存在するとシクロヘキサジエンとなるが、シクロヘキサンの骨格が環状であるため、鎖状炭化水素の炭素のように端から順番を付けるということはできない。そこで、一つだけ二重結合が存在する場合には、二重結合を形成している炭素の片方を炭素1もう片方を炭素2とする。この場合、炭素1と炭素2には差異は無いので、単にシクロヘキセンと呼ぶ。二重結合が二つ存在すると、下図のように二つの構造異性体が存在するため、炭素に番号を付けることが必要となる。そのため、一つの二重結合の炭素の番号を1、2とするが、その順番に従って番号を付けた場合に、他の二重結合の炭素の番号が小さくなるようにする。例えば、シクロヘキサンに2個の二重結合が孤立状態で存在する場合には、1,4-シクロヘキサジエンに命名が固定される。しかし、共役ジエンの形で存在すると、1,3-シクロヘキサジエンと1,5-シクロヘキサジエンの表現が可能となる。この場合は1,3-シクロヘキサジエンとする。1,3-ヘキサジエンの二重結合は共鳴二重結合構造で炭素1から炭素4までのπ結合に関与する電子は非局在化分子軌道を形成し平面となる。

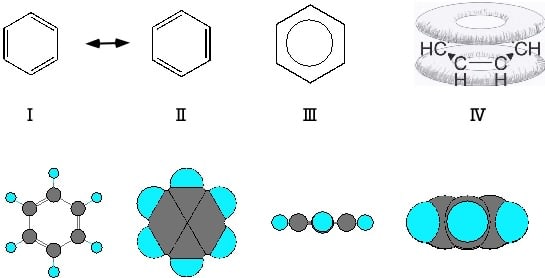
シクロヘキサンには3つの二重結合を組み込むことができる。この場合にはすべての二重結合が共役していることになるが、共役の末端となる炭素は存在せず、下図に示したように、分子全体に均等に非局在化分子軌道が形成される。これを平面構造ではIとIIの共鳴混成体として表わし、π電子が均等に存在することを示すためにⅢで表すこともある。π電子の分布の概観をⅣに示したが、分子全体が完全な平面となり、分子モデルからも示されるように全ての炭素の結合角がsp2混成軌道の要求に完全に一致している。このため、1,3,5―シクロヘキサトリエンの構造を持つこの化合物は異常に安定で、1,3-シクロヘキサジエンの延長として推定されるものとは非常に異なった物性と反応性を示す。そのため、この化合物はベンゼンという固有名称で昔から呼ばれ、IUPACでものここの名称を使うことに定めている。このベンゼンに類似した性質をを示す化合物を一般的名称として芳香族化合物と呼ぶ。ンゼン以外にも芳香族化合物は多く存在する。例えば2個のベンゼン環が縮合した形のナフタレン(文末の星間分子の図参照)もベンゼンと同様にsp2の混成軌道の構造的条件をほぼ満たし、かつπ電子は分子全体に非局在化している。
なお、ベンゼンの水素が炭化水素基(アルキル)で置換されてできる下図に示した、トルエン、キシレン、メシチレン、クメン、シメン、スチレンの名称は化合物固有名称として昔から広く使われているため、これらの慣用名を使用することがIUPACの規則で認められている。下図では上段に慣用名、下段にIUPACの規則による命名が示してあるが、慣用名で使われているo-、m-、p-の記号は、それぞれベンゼン環のオルト位(1,2-位)置換体、メタ位(1,3―位)置換体、パラ位(1,4-位)置換体を意味している。この表現は慣用的には良く使われるが、IUPACでは極力使用しないようにと指示されている。

下図に示すアセチレン(Ⅰ)、エチレン(Ⅱ)、プロピン(メチルアセチレン)(Ⅲ)、プロペン(メチルエチレン)(Ⅳ)、ペンタ―1,3―ジイン(メチルジアセチレン)(Ⅴ)、ヘプター1,3,5-トリイン(メチルトリアセチレン)(Ⅵ)、ベンゼン(Ⅶ)、ナフタレン(Ⅷ)は星間分子としても報告されている。

















この原因をしぶとく究明してこの材料は実用化されたのがその舞台裏である。
1/h^n=1/f^n+1/g^n、
第一式おもしろい着想ですね。経済学のホットな話題として財政均衡主義と現代貨幣理論(MMT)の競合モデルの方程式や関数なんてものはできないのでしょうかね。
いくら機械的特性(材料強度・硬さ)が高くても、材料というものは摩擦に弱い。
そのため潤滑油が存在する。しかしながら、それでも弱いので
コーティングをする。
しかし、日立金属が開発した自己潤滑性冷間ダイス鋼SLD-MAGICは
コーティングレスで摩擦に強いことが特徴。そのメカニズムは
潤滑油と特殊鋼が相互作用を起こし、グラファイト層間化合物(GIC)
という高性能な潤滑物質を作るためであることが、日立金属技報
2017で公表された(CCSCモデル、炭素結晶の競合モデル)。
これにより機械部品の設計は小型化され、摩擦損失と軽量化の同時
解決が見込まれ、低フリクションによる自動車の燃費向上に大いに寄与することが期待
されている。
GICって言う物質がフリクションを下げるなんて初めて知りました。