
おひさしぶりです!皆さんお元気ですか!?
私は、僕は、Meは、拙者は、
先月から始まった某特別講座のテキスト作りに追われています。
(^^;
毎月一回の講義で、向こう一年間の予定です。
受講される皆さんも真剣なので、
講義にも真剣に取り組んでいきます。
レイアウトも含め、講義内容などもすべて自分で、
まさに「手作りテキスト~」です。
たいていの人が苦手な「化学」の分野にも、
必然的にかなり足を踏み入れる事になるので、
なるべく難しくならないよう、分かりやすく分かり易く、
気をつけながら作っています。←これが結構大変なわけでス)

では、せっかくなので、皆さんにも問題を出しましょう。(笑)
あまり身近な事ではないと思いますが、何かの役に立つ事もあるかなと・・。
「酸性」と「アルカリ性」を水に混ぜたら、何が出来ると思いますか?
ここでは
塩酸(強酸性)と、水酸化ナトリウム(強アルカリ性)
を使って、化学式で解いてみます。
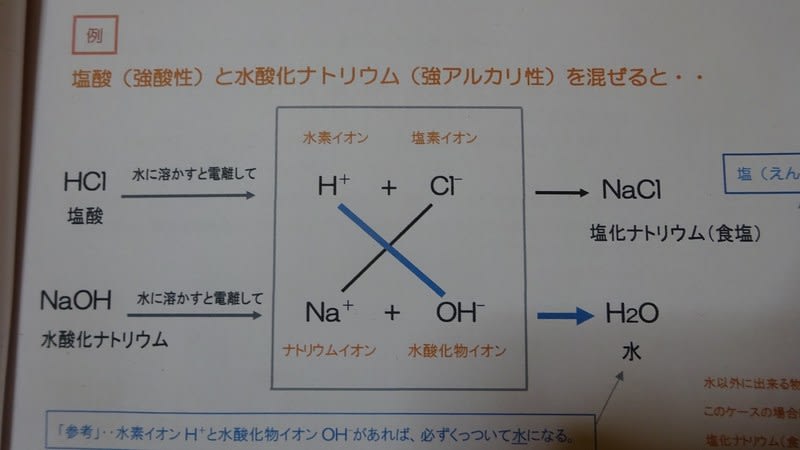
答え・・水と食塩 ができます。
「塩化ナトリウム」、つまりNaCl、食塩のことです。
(・・・Naはナトリウム、Clは塩素の元素記号です)
 なるほど。。
なるほど。。
では、
今度は少し身近な暮らしに関係のある問題を出しましょう!。(^^)
洗剤で、「混ぜるな危険!」の表示を目にする事もあるかと思います。
(トイレ用やカビ取り漂白剤の商品に多いですね。)
これは、酸性の液と塩素系漂白剤を混ぜてしまうと、
化学兵器にも使用される猛毒ガス(塩素ガス)が発生して
しまうからなのですが、
なぜ、発生するのか、簡単に説明してみましょう。
(なんだか今日はいつもの「星空Cafe」じゃないっしょ。
たまにはイイですね。笑)

酸性タイプのトイレ用洗剤の主成分にはたいてい「塩酸」が使われます。
「塩酸」は尿石などのカルシウム分を溶かすのには効果が強い
成分だからです。
そこへ、カビキラーなどの塩素系漂白剤を
うっかり一緒に使ってしまったとします。
トイレの黒ズミは、じつはカビなので、
カビキラーなどをシュッシュ!してしまうケースが多いのです。
(一般のご家庭での事故発生件数も相変わらず多いです。)
カビ取り漂白剤の主成分には、たいてい「次亜塩素酸ナトリウム」
という成分が使われていますが、
じつは、水道水の消毒・殺菌剤「カルキ」の正体が
この次亜塩素酸なのです。
(小規模な浄水場では次亜塩素酸カルシウム、大規模な浄水場では
次亜塩素酸ナトリウムが使われています。)
では、この「次亜塩素酸ナトリウム」と「塩酸」の混ぜ合わせを
化学式で表してみましょう。
「カビキラー」 「酸性トイレクリーナー」
次亜塩素酸ナトリウム + 塩酸 → 塩素(ガス) + 水酸化ナトリウム
NaClO + HCl → Cl2 + NaOH
となるわけです。
混ぜる側の両方にCl(塩素)の原子がひとつずつありますね。
これが2つ合わさってくっつくと、 Cl+Clで Cl2 に。
(Cl2=塩素の原子粒が2コ結びついた状態=塩素ガス)
つまり原子が2コ結びついて、その物質の性質を初めて発揮する
「分子」になったわけです。
塩素が「分子」の状態になると、「塩素ガス」という毒ガスに
変身してしまうのです。恐いですね。

浴室やトイレなどをお掃除する時は、
「酸性」と「塩素系」の洗浄剤の組み合わせに、
皆さん、くれぐれも気をつけて下さい。
塩素ガスは黄縁色をしていて、発生したら必ずムセます。
おかしいなあと思いながらも吸い続けていると、
突然呼吸困難に陥ります。
むせたら、すぐに換気をして、その場から退避して下さい。
星空Cafe それじゃまた!。
分かり易く講義するというのは、本当に難しいものです。
特に「化学」は。(むははのは。イオン化傾向。)

コメント欄しばらくCloseで。m(^^;)m


















※コメント投稿者のブログIDはブログ作成者のみに通知されます