コロナワクチンで、スパイクによる自己免疫疾患がいろいろ出てきます。多発性硬化症もその例です。その多発性硬化症に対して、全身的な免疫抑制を引き起こすことなく自己反応性T細胞を制御するmRNAワクチンが次々に出てきます。
研究例を挙げると
A noninflammatory mRNA vaccine for treatment of experimental autoimmune encephalomyelitis
Christina Krienke ら 2021, American Association for the Advancement of Science.
https://pubmed.ncbi.nlm.nih.gov/33414215/
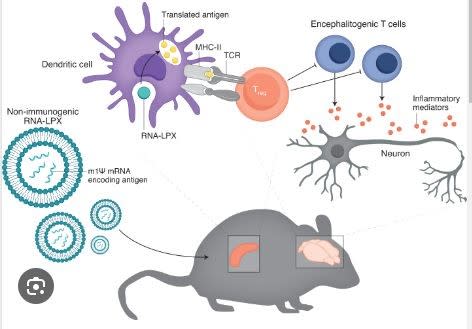
【全身的な免疫抑制を引き起こすことなく自己反応性T細胞を制御する能力は、自己免疫疾患の治療における主要な目標である。そのためには、薬学的に明確に定義された抗原を、非炎症的な状況で安全かつ効率的に送達することが重要な課題である。ここでは、疾患関連自己抗原をコードする1メチルシュードウリジン修飾メッセンジャーRNA(m1Ψ mRNA)をナノ粒子で形成した全身投与により、コスト刺激シグナルがない状態で脾臓CD11c+抗原提示細胞での抗原提示が得られることを示す。多発性硬化症のいくつかのマウスモデルにおいて、このようなm1Ψ mRNAを用いた治療により、疾患が抑制される。この治療効果は、エフェクターT細胞の減少と制御性T細胞(Treg細胞)集団の発達に関連している。注目すべきは、これらのTreg細胞が強力なバイスタンダー免疫抑制を行うことで、同族および非同族の自己抗原によって誘発される疾患を改善することである。】
mRNA vaccines take on immune tolerance
Christine M. Wardell & Megan K. Levings
Nature Biotechnology volume 39, pages419-421 (2021)Cite this article
【COVID-19のパンデミックでは、mRNAを用いたワクチンが、その高い有効性と前例のない開発・製造スピードから、大きな話題となりました。COVID-19のmRNAワクチンの開発を主導したUgur Sahinとその共同研究者は、このワクチン技術を利用して、抗原特異的な免疫反応を促進するのではなく、むしろ抑制することに成功しました。多発性硬化症のマウスモデルを用いて、自己抗原をコードする改変mRNAを非炎症性リポプレックス担体に封入したワクチンを接種すると、抗原特異的制御性T細胞が活性化し、自己免疫の抑制につながることを明らかにした(図1)。この戦略の臨床的可能性を評価するためにはさらなる研究が必要ですが、寛容化ワクチン接種のアプローチが成功すれば、自己免疫疾患、アレルギー、同種移植の治療法を一変させることができるでしょう。】