腎動脈狭窄
Endocrinol Metab Clin North Am
2019; 48: 765-778
腎動脈狭窄(renovascular disease)は二次性高血圧の主な原因である。動脈硬化性腎動脈狭窄は腎動脈狭窄の最も多い原因であり、次に多いのは線維筋性異形成 (fibromuscular dysplasia: FMD) である。腎動脈狭窄はアンジオテンシン依存性高血圧の原型として長い間認識されてきた。しかし、腎血管性高血圧症の病理は複雑であり、腎動脈狭窄の病因を鑑別する必要がある。現時点では、腎動脈血行再建術の有用性に関する前向き臨床試験の結果は中立的であり、腎動脈狭窄の原因と腎閉塞の程度を認識することは管理上重要である。多くの腎動脈狭窄患者は薬物療法で管理されるが、高リスクの臨床像や臓器不全の可能性がある患者では、薬物療法に加えて血行再建術が有効である。最大の課題は、併存疾患が大きく異なる中で、個々の患者にとって最善の方法を個別に考え、実行することである。
1. はじめに
腎血管疾患は、進行性の閉塞性腎動脈疾患によって引き起こされ、腎血管性高血圧から虚血性腎症 (ischemic nephropathy) まで無数の症状を呈する。腎血管性高血圧(renovascular hypertension)は二次性高血圧の最も一般的な原因の一つであり、アンジオテンシン依存性高血圧の原型として広く研究されている。しかし、頻度は少ない。
20 世紀初頭に Goldblatt が行った 2-kidney 1-clip model を用いた研究から、腎低灌流が高血圧の主な原因となることが判明した。この研究の後に Page と Braun-Menendez によって、血管作動性ペプチドであるアンジオテンシン (angiotensin) が同定され、腎血管疾患におけるレニン-アンジオテンシン-アルドステロン系(renin-angiotensin-aldosterone system: RAAS)軸の活性化の役割が確認された。 これらの知見から、全身的な血圧上昇の可逆的な原因が特定された。これにより、腎動脈閉塞性病変が同定された場合に、外科的に腎性高血圧の原因となっている腎を摘出することによって治療できる可能性がもたらされた。この介入は、高血圧の内科的治療が不可能であった時代に、高血圧の「治癒」あるいはより良いコントロールを可能にした。残念ながら、外科的腎摘除術は高血圧治療に成功しないことが多く、後に推奨されなくなった。降圧薬の集中的な開発により、1980 年代に RAAS 遮断薬を含む複数の治療薬が開発された。これは、血管拡張術やステント留置術が拡大した時期と重なる。
中等度の腎動脈狭窄は無症状の場合もあるが、腎動脈狭窄が進行するとやがて高血圧が発症する。血行動態学的に有意な狭窄を同定する基準として一般的に用いられているのは、腎動脈の内腔径が少なくとも 60%減少していることであり、これはドップラー超音波検査による収縮期ピーク速度が 200-300 cm/s を超えることと関連している。それにもかかわらず、狭窄腎は中等度の流量の減少に適応できるため、血圧をコントロールするための降圧薬物療法を比較的安全に長期にわたって使用できることが研究で示されている。このような症例では、腎血管性高血圧が進行し、「急性肺水腫, flash pulmonary edema」を伴う高血圧性緊急症や進行性の腎機能低下などのハイリスク症候群を発症する可能性がある。こうなると、内科的治療と腎動脈狭窄の血行再建術の併用が必要となる。この総説では、疫学、腎血管疾患の種類、病態生理、臨床的特徴、診断、そして現在の複雑な症例を診る臨床医に推奨される治療法について述べる。
2. 腎血管性高血圧の疫学と原因
腎血管疾患は高血圧の主要な原因であり、一般集団における高血圧症例の 1-5%、若年成人における二次性高血圧症例の 5.4%を占める。腎血管疾患は、65 歳以上の高齢者集団に多く、有意な腎動脈狭窄(ドップラー超音波検査による閉塞が 60%以上)が 7%近くを占めるという報告もある。しかし、腎動脈狭窄の定義のばらつきや研究対象集団の種類により、実際の発生率や有病率は異なる。症例の 90%において、腎血管疾患は動脈硬化性腎動脈狭窄症(atherosclerotic renal artery stenosis: ARAS)が原因であり(図 1)、次いで線維筋性異形成(9%)である。残りは表 1 に示すような雑多な原因によるものである。
図 1. CT アンギオグラフィにより右腎に中等度の腎動脈狭窄 (矢印) が示されている。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7184322/figure/F1/
表 2. 腎動脈疾患の原因
3. 動脈硬化性腎動脈狭窄症
腎動脈狭窄の原因としてアテローム性腎動脈狭窄症は最多であり、全身性アテローム性動脈硬化症を伴う高齢者に多くみられる。これらのプラークの多くは大動脈プラークの腎動脈への進展である。したがって、アテローム性動脈硬化性疾患の部位は、腎血管のどこにでも認められるが、通常は動脈の起始部付近である。片側の場合も両側の場合もある。患者はしばしば糖尿病、高血圧症、喫煙歴、末梢動脈疾患、冠動脈疾患などの他の関連危険因子を有している。画像検査や他のインターベンション治療中に偶然発見される無症候のものから、難治性高血圧、再発性急性肺水腫、進行性腎機能低下などの心血管系症状を呈するものまで様々である。
ある程度の動脈硬化性腎血管疾患は、末梢血管疾患患者の血管検査を受けた症例の 12-45%、冠動脈造影を受けた症例の 14-40%に認められる。
4. 線維筋性異形成
FMD は、血管壁の内膜または線維層を侵す非動脈硬化性、非炎症性の不均一な疾患である。一般に腎動脈と脳動脈(65-70%)が侵されるが、他の血管床も侵されることがある。動脈狭窄、解離を伴う動脈瘤形成、かつ/または中動脈 (medium sized artery) の閉塞を引き起こす可能性がある。FMD には 2 つの亜型がある。多巣性 FMD (multifocal FMD) はいわゆる "数珠つなぎ "のような外観を呈し、局所性 FMD (focal FMD) より多い病型である。FMD 病変は通常、腎動脈の起始部から離れた場所、しばしば血管の中間部または最初の動脈分岐部に位置する。主に女性が罹患し、中年期に診断されることが多い。高血圧のために腎血行再建術を受けた患者のうち、FMD が占める割合は 16%以下であることが、介入研究によって示唆されている。高血圧が最も一般的な症状であるが、拍動性耳鳴、脳卒中、胸痛などの他の症状が、腎動脈以外の血管床に生じた病変に起因することもある。さらに、United States FMD Registry を用いた研究では、多巣性 FMD と診断された時点で 65 歳以上の患者は無症状である可能性が高い可能性が示された。
前向きの ARCADIA(Assessment of Renal and Cervical Artery Dysplasia)registry において、FMD を有する症候性患者に対して大動脈弓から頭蓋内動脈まで、頸部 FMD を有する患者に対しては横隔膜 (diaphragm) から骨盤 (pelvis) までの CT アンギオグラフィまたは MR アンギオグラフィを行った。脳血管病変を有する患者においては、腎動脈病変の有病率は高血圧患者をともなう患者で高かった。腎病変を有する患者では、頸部病変の有病率は、一側性腎動脈病変を有する患者よりも両側性腎動脈狭窄を有する患者で高かった。これらの研究は、FMD は全身性動脈疾患であることを示している。
5. 腎血管性高血圧の病態生理
腎血管性高血圧は、腎臓への血流灌流の低下によって起こる。他の原因で血管撮影を受けた患者に偶発的な腎血管疾患が見つかることがあるが、軽微な狭窄は臨床的に重要でない場合がある。臨床研究によると、拡張バルーンを用いて腎動脈を閉塞させると、バルーン遠位側の圧力が病変近位側の圧力より 10-20%低下した場合にレニンが放出される。腎動脈狭窄が進行すると、圧力と流量は急峻に低下する(図 2)。
図 2. 腎動脈における圧較差とレニン分泌の関係
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7184322/figure/F2/
実験的に腎動脈疾患を再現すると高血圧を来すのは、腎血流を維持するために全身の血圧と腎末梢の血圧を上昇させるためにレニン分泌が亢進するためと解釈されている。この血圧上昇はクリップ狭窄を用いた実験モデルでは急性のものとなるが、ヒトの腎動脈疾患では緩徐に血圧が上昇する。このような低灌流状態が続くと、腎血流を維持するためのメカニズムが働く。RAAS の活性化とナトリウム貯留が腎血管性高血圧において主要な役割を果たすことは、実験モデルやヒトにおいて十分に確立されている。
アンジオテンシン I は、肺毛細血管床でアンジオテンシン変換酵素(angiotensin-converting enzyme: ACE)によってアンジオテンシン II に変換される。アンジオテンシン II はそれ自体強力な血管収縮作用があり、副腎皮質からアルドステロンの分泌させ、塩と水分の貯留を促進する。腎血管性高血圧の病態生理にアンジオテンシンが必要であることは、アンジオテンシン II サブタイプ 1A 受容体ノックアウト(angiotensin II subtype 1A receptor knockout: AT1A-/-)マウスにおいて、2-kidney 1-clip Goldblatt 高血圧モデルで高血圧を来さないことから確認されている。この研究は、アンジオテンシン II サブタイプ 1A 受容体が血圧コントロールにおいて重要な役割を果たしていることを示している。
腎血管疾患において RAAS が果たす役割は、部分的には、対側の狭窄していない腎の有無に依存することを指摘しておくことは重要である。ヒトの片側腎血管疾患は、末梢抵抗の増加を特徴とする 2-kidney 1-clip Goldblatt モデル、あるいは「レニン依存性」高血圧とも呼ばれる動物モデルに相当する。血圧の上昇は、インタクトな対側腎によるナトリウム利尿を刺激し、ナトリウム貯留と体液貯留を防ぐ。すなわち、狭窄していない方の腎は全身性の血圧上昇に対抗する傾向があり、狭窄腎の低灌流状態を維持し、レニンの持続的分泌をもたらす。腎血管疾患は依然としてアンジオテンシン依存性高血圧の原型であるが、これらのホルモン反応は通常一過性である。閉塞が進行するにつれて、あるいは対側の非狭窄腎がない場合には、病態生理は異なり持続的な高血圧を来す。対側の腎も機能しないためにナトリウムと水分の排泄が障害され、血管内容積が増加すると、レニン分泌は時間とともに漸減する。この段階は「容積依存性」高血圧と呼ばれる。
アンジオテンシン II が介在する血管収縮によって狭窄部より遠位の糸球体濾過圧は維持されるが、この血管収縮は遠位細動脈に優先的に作用する。腎血流が減少すると、糸球体濾過量がアンジオテンシン II に依存する状況になることがある。こうなると、RAAS を遮断してアンジオテンシン II の作用を除去することで、糸球体濾過量は劇的に低下する。この臨床例としては、両側腎動脈狭窄による RAAS 遮断や、単独機能腎の著しい狭窄がある。この機序による腎機能低下の可能性があるため、両側腎動脈狭窄または孤発性狭窄腎の患者における ACE 阻害薬やアンジオテンシン受容体拮抗薬(angiotensin receptor blocker: ARB)などの降圧薬の投与は慎重を期すべきである。
腎血管疾患の病態生理学は、カプトプリル負荷レノグラム (captopril renography) を用いた核医学検査や腎静脈レニン測定による腎動脈狭窄の診断と治療の基礎となっている。RAAS は血管収縮やナトリウム貯留以外にも広範な作用を持つ。アンジオテンシン II は複雑な細胞間相互作用を持ち、炎症および線維化を引き起こす。これにより狭窄腎における血管リモデリングと線維化、さらに左室肥大が起こる。さらに、動脈硬化性腎動脈狭窄は通常、全身性アテローム性動脈硬化とこの疾患に伴う炎症との関連で起こる。交感神経の活性化、内皮機能障害、酸化ストレスの増加の関与も臨床研究で証明されている。これらの因子はすべて、動脈硬化性腎動脈狭窄患者における高血圧の一因となっている。
どの程度の血管閉塞があると腎機能が障害されるのかについては、まだ議論の余地がある。腎臓は血流が豊富な臓器であり、動脈径が減少しても自己調節を維持することができる。しかし、臨界狭窄(75-80%)を超えて腎血流が低下すると、血中酸素濃度依存性(blood oxygen level-dependent: BOLD)画像によって測定されるように、組織の低酸素症を来す(図 3)。
図 3. 腎血管疾患における BOLD-MRI
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7184322/figure/F3/
アテローム性動脈硬化性腎血管疾患が、炎症性環境の中で急性虚血性傷害を繰り返し、低酸素症に至り、最終的に生命維持に必要な腎機能を失うという、「虚血性腎症」と呼ばれる緩徐に進行する過程を示す可能性を排除することはできない。この過程が不可逆的になる前に、腎血流が低下している患者を特定することは、臨床上重要である。
6. 臨床的特徴
上述したように、腎血管性高血圧は腎臓への血流を低下させるあらゆる原因によって発症する可能性がある。FMD 病変は、一般的に腎動脈の中間部を侵し、15-55 歳の女性に好発し、若年での高血圧を来す。動脈解離のような血管障害を発症した患者では進行が見られることがあるが、大きな腎機能低下を引き起こすことはほとんどなく、喫煙者に好発する。このタイプの腎動脈病変は経皮的血管形成術 (percutaneous angioplasty) によく反応する傾向がある。
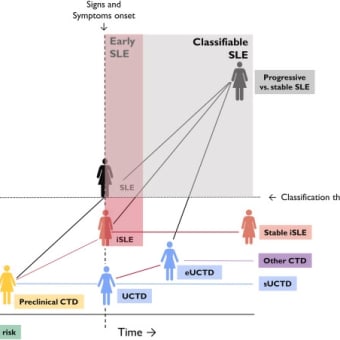
アテローム硬化性腎動脈狭窄はより広範な悪影響を伴う。しばしば両腎を巻き込み、一般に血管閉塞の重症度に関連して様々な症状を伴う多臓器疾患過程である(図 4)。
図 4. 腎動脈疾患のスペクトラム
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7184322/figure/F4/
動脈硬化性腎動脈狭窄は他の心血管系疾患や合併症を有する高齢者によくみられる。高血圧の評価を受けるすべての患者において、腹部/側腹部の聴診を含む徹底的な身体検査を行い、腹部拍動の存在を確認すべきである。これにより、腎動脈狭窄の可能性のある高血圧患者を同定する有用なヒントが得られるかもしれない。このような腹部拍動が発見された場合には、さらなる画像検査を行うきっかけとすべきである。
腎動脈狭窄は、冠動脈カテーテル検査、磁気共鳴 (magnetic resonance: MR) 検査、コンピュータ断層撮影 (computed tomography: CT) 血管造影など、他の適応のための画像検査や処置中に診断されることが多い。腎動脈狭窄に伴う腎血管疾患は、慢性腎疾患の有無にかかわらず、しばしば抵抗性または難治性高血圧に至る進行性の血圧上昇を伴う臨床症状によって診断される(表 2)。
表 2. 腎血管疾患に関連する臨床症状
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7184322/table/T2/
臨床症状としては、進行性の、時には急激な動脈圧上昇がある。これは、すでに降圧薬による治療を受けている高血圧症の既往がある高齢者にしばしば起こる。したがって、臨床医は、降圧薬の必要量が徐々に増加している患者、特にアテローム性動脈硬化性疾患のリスクが高い患者では、高血圧の二次的原因がないかどうかを強く疑う必要がある。特に、喫煙歴のある患者では重要であり、喫煙歴自体が、腎血管性高血圧患者における心および腎の有害な転帰と強い関連がある。
このような集団における RAAS 軸の活性化は、特に患者が最適な薬物療法を受けていない場合、血圧変動を増大させる。RAAS 活性の亢進に伴う塩分と水分の再吸収は、しばしば体液貯留と肺うっ血を引き起こす。体液貯留と RAAS 活性の亢進が組み合わさると、直接的な血管障害、左室肥大、腎機能障害などの臓器障害が加速される。これらは、同じ程度の血圧コントロールの年齢をマッチさせた集団と比較した場合、本態性高血圧患者よりも腎血管疾患患者でより多くみられる。
腎血管疾患は心血管系疾患のリスクである。重症の場合、血圧の上昇は体液貯留を伴い、左室機能障害に伴ううっ血を来す。この一連の現象は「急性肺水腫」と呼ばれ、一般に腎機能障害を伴う心腎症候群である。腎血管疾患に伴う肺水腫は、うっ血性心不全患者における入院の増加および死亡率の上昇につながる。最終的に、進行性の閉塞性腎動脈疾患は、腎に低酸素症を生じさせ、特に糖尿病、高血圧、喫煙などの他の危険因子との関連において、「虚血性腎症」と呼ばれる不可逆的な腎機能の悪化を引き起こす。
7. 画像診断と臨床検査
腎血管疾患を疑う臨床症状があれば、画像検査を検討すべきである。しかし、費用のかかる、あるいは危険な画像検査を行う前に、臨床医はまず画像検査の目標を設定すべきである。すなわち、画像検査を行う前に、1. 検査検査によって現在の医学的管理が変わるか? 2. 血管インターベンションを考慮すべき臨床的特徴があるか? 3. 検査結果は薬物療法の変更、腎血行再建術、あるいは腎摘除術につながるのか?を問うべきである。
画像診断の選択は、患者の臨床的状況によって異なる。非侵襲的画像診断技術の進歩により、診断の感度と精度はかつてないほど向上している。コンピュータ断層撮影血管造影(computed tomography angiography: CTA)や磁気共鳴血管造影(magnetic resonance angiography: MRA)、ドップラー超音波検査は、血管系の評価によく用いられる非侵襲的画像診断法である。しかし,これらの検査はいずれも完全なものではない。臨床的に有益な情報が得られるのは、検査前確率が高い集団でで画像検査の結果が陽性であった場合である。デュプレックス超音波検査 (Duplex ultrasonography) は最も安価な検査であり、多くの場合、最初に行う検査である。
デュプレックス超音波検査法
https://www.msdmanuals.com/ja-jp/professional/24-%E3%81%9D%E3%81%AE%E4%BB%96%E3%81%AE%E3%83%88%E3%83%94%E3%83%83%E3%82%AF/%E6%94%BE%E5%B0%84%E7%B7%9A%E5%AD%A6%E7%9A%84%E6%A4%9C%E6%9F%BB%E3%81%AE%E5%8E%9F%E5%89%87/%E8%B6%85%E9%9F%B3%E6%B3%A2%E6%A4%9C%E6%9F%BB
造影剤を静脈内投与する必要もない。この手技の限界は、術者の技量と患者の体格に依存することにある。
臨床的に重症の腎血管疾患が強く疑われ、非侵襲的検査で結論が出ない場合は、カテーテル血管造影を行うことがある。この手技は通常、検査と同時に血管内治療を行うことが望ましいと考えられる患者にのみ行われる。
治療のために腎摘除術を行う前に左右の腎の相対的機能を評価する必要がある場合には、カプトプリル負荷レノグラフィによる腎機能検査を考慮することもできる。しかし、腎機能検査は腎機能不全、特に両側腎血管疾患の場合、まだ信頼性に限界がある。
腎血管疾患では血液検査は正常か、腎不全の程度と一致する。クレアチニンが徐々に上昇するようであれば、腎動脈デュプレックス超音波検査などの評価が必要である。尿検査は一般的に所見に乏しく、蛋白尿はごくわずかである。著明な蛋白尿や尿沈渣で異常所見を認める場合は、腎血管疾患以外の腎疾患の可能性を考慮する必要がある。
血漿レニン活性はナトリウムや体液の貯留状態によって変化するため、血漿レニン活性だけでは病態の評価はできない。場合によっては、血漿アルドステロン/レニン比から低カリウム血症の原因が腎血管疾患による二次性アルドステロン分泌過剰であることが推測できることもあり得る。腎静脈のレニン濃度の測定は、狭窄腎のレニン高値と対側腎のレニン濃度の低下を同定するために、かつては用いられた。しかし、腎静脈レニン測定は、薬剤や体液量の影響を受ける。腎機能の保護が目的とならない場合、腎血管疾患が腎血行再建術の適応となることはあまりないため、これらの検査が行われることはほとんどない。腎静脈レニン測定は,血圧コントロールのために腎摘除術を考慮する場合に最もよく用いられる。
8. 腎血管疾患の管理
腎血管疾患の治療は、腎血管疾患のタイプと臨床症状によって異なる。FMD 患者では、腎動脈にバルーン血管形成術が適応となる複数の病変が存在することがある。これらの症例の約 10-15%が再狭窄を起こすが、血管形成術を繰り返し行っても良い。血管形成術に成功しても、高血圧が「治癒」、すなわち降圧療法をすべて中止できるのは、症例の 3 分の 1 以下である。「治癒」の可能性は、患者の年齢、高血圧の罹病期間、重症度などの因子に依存する。一般に、臨床医は FMD 患者、特に若年患者に対して、降圧薬の中止または減量を目的とした腎血管インターベンションを考慮すべきである。
動脈硬化性腎動脈狭窄患者の治療は FMD 患者とは多少異なる。なぜなら、血管形成術だけでは近位部または血管起始部のアテローム性動脈硬化病変の開存を維持できないことが多いからである。血管起始部の広範な石灰化プラークは治療抵抗性の傾向があり、再狭窄率が高い。直径 5 mm 未満の血管に留置されたステントでは、最大で 20%の症例で再狭窄が起こる可能性がある。
内科的治療と腎血行再建術を比較したいくつかのランダム化比較試験の結果では、血圧コントロール、腎アウトカム、心血管アウトカムの改善に関して、内科的治療単独に加えて血管内ステント治療を追加することの決定的な有益性を示すことはできなかった。しかし、これらの研究の大きな限界は、「高リスク」の臨床像(すなわち、急速に進行する腎不全、ACE/ARB 治療開始時の急性腎障害、難治性の高血圧、および/または急性肺水腫)を有する患者の割合が低いということである。このような患者には腎動脈狭窄を治療することが有効であろう。複数の観察研究から、このような患者では腎循環が回復すると臨床的に大きな利益が得られることが示されている。臨床医にとっての課題は、このような治療により腎予後を改善できる見込みのあるサブグループを同定し、適切な介入を行うことである。
腎血管性高血圧症と虚血性腎症の管理のための臨床アルゴリズムが提案されている(図 5)。
図 5. 腎血管性高血圧症と虚血性腎症の管理についてのアルゴリズム
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7184322/figure/F5/
他の血管閉塞性疾患と同様に、腎血管性高血圧症と診断された患者は、高血圧のコントロールと腎機能が安定していることを確認するために経過観察するべきである。血行再建術後に内科的治療を行い 3-5 年間追跡した調査では、血行再建術の明らかな利点は認められなかったが、尿蛋白が正常であった集団では、事後解析で心血管系および死亡率に明らかな利点が認められた。動脈硬化性疾患は一般に長期にわたって進行する。腎血管狭窄以外の合併症を持つ患者の中には、高度狭窄および高リスク群の特徴を発現する者もいる。このような患者に対しては、臨床医は完全閉塞や不可逆的な損傷を防ぐために、腎臓の血行再建のリスクとベネフィットを定期的に再評価する必要がある。
9. キーポイント
·腎血管疾患は二次性高血圧の主な原因であり、無症候性高血圧から腎不全、肺うっ血までさまざまな臨床症状を呈することがある。
·腎動脈狭窄の種類、程度、臨床症状を区別することは、個々の患者にとって最良の管理を考えるために必要である。
·最適な薬物療法に関する前向き試験の結果から、中等度の腎動脈狭窄患者では、腎動脈ステント留置による追加的利益は得られないことが示されている。
·動脈硬化性腎血管疾患の管理の基本はレニン・アンジオテンシン系を遮断する薬剤の使用と脂質コントロールを含む包括的な内科的治療である。
·臨床医は、腎と心血管のアウトカムを改善するために腎血行再建術を受けるべき「高リスク」の腎血管性高血圧患者を認識する必要がある。
元論文
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7184322/