気になる内容の記事を見つけましたのでメモ。
■AFの二次イベントリスクが明らかに〜男性はAMI、女性はISが最も高い
(2017年09月06日;メディカル・トリビューン)
スウェーデンにおける初発心房細動(AF)患者約50万例の登録データを基に、発症後10年間の二次性イベントの発症リスクを検討したところ、男性では致死性または非致死性の急性心筋梗塞(AMI)、女性では虚血性脳卒中(IS)の発症リスクが最も高く、これらのリスクは年々増加傾向にあることが明らかとなった。スウェーデン・University of GothenburgのLena Björck氏が欧州心臓病学会(ESC 2017、8月26~30日、バルセロナ)で報告した。
1年後、5年後、10年後の二次性イベント発症率を検討
AFは全身性塞栓症のリスク因子であり、AMI発症リスクの増加と関係することが知られているが、これらの二次性イベントのうち、いずれの血栓イベントを最初に発症するかは明らかになっていない。そこで、Björck氏らはスウェーデンにおけるAFの大規模患者登録データを用いて、初発AF患者の致死性または非致死性AMI、IS、静脈血栓塞栓症(VTE)の初発イベントの長期発症リスクを検討した。
対象は、1987~2012年にSwedish Inpatient Registerに登録されたAMI、IS、VTEの既往歴がない初発AF患者49万6,173例。2013年12月31日まで追跡し、1年後、5年後、10年後の致死性または非致死性AMI、IS、VTE〔深部静脈血栓症(DVT)または肺塞栓症(PE)〕の初発イベントを記録し、イベント発症率を算出した。
女性でより高い二次性イベント発症リスク
対象の年齢は18~84歳と幅広く、男性が53%(平均年齢70.2歳)、女性が47%(同76.6歳)を占めた。
ベースライン時の併存疾患は、高血圧(26.5%)、心不全(25.2%)が高率で、AMI以外の虚血性心疾患(16.7%)、がん(12.5%)、糖尿病(11.3%)、心弁膜症(7.0%)、一過性脳虚血発作(TIA、4.0%)が続いた。脳内出血、先天性心疾患、末梢血管障害の既往例は1%未満であった(図1)。
図1. ベースライン時の併存疾患

また、1年後、5年後、10年後における致死性または非致死性AMI、IS、VTEの二次性イベントについて男女別に検討したところ、男性では致死性または非致死性AMI、女性ではISが一貫して最も頻度が高く、これらのイベント発症率は、男女とも経時的に増加する傾向にあった(図2)。
図2. 1年後、5年後、10年後の二次性イベント発症率
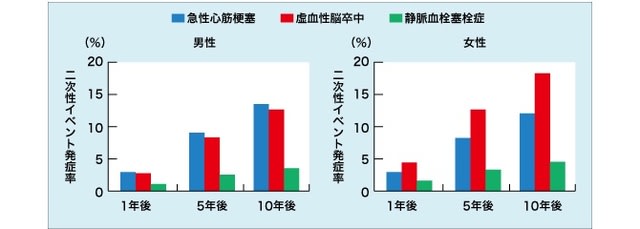
(図1、2ともにESC 2017発表データ)
以上の結果から、Björck氏は「初発AF後、最初に発症する二次性イベントは、男性では致死性または非致死性AMIとISがほぼ同率で、女性ではISが最も多かった。VTEは長期的な発症率は高くはなかったが、女性では男性よりも高率であったことから、総合的なリスクは男性より女性の方が高いと考えられた」と結論。さらに、「相対的に二次性イベントの発症リスクが男性よりも女性で高い理由は不明であり、今後さらなる研究が必要」と付言した。
■AFの二次イベントリスクが明らかに〜男性はAMI、女性はISが最も高い
(2017年09月06日;メディカル・トリビューン)
スウェーデンにおける初発心房細動(AF)患者約50万例の登録データを基に、発症後10年間の二次性イベントの発症リスクを検討したところ、男性では致死性または非致死性の急性心筋梗塞(AMI)、女性では虚血性脳卒中(IS)の発症リスクが最も高く、これらのリスクは年々増加傾向にあることが明らかとなった。スウェーデン・University of GothenburgのLena Björck氏が欧州心臓病学会(ESC 2017、8月26~30日、バルセロナ)で報告した。
1年後、5年後、10年後の二次性イベント発症率を検討
AFは全身性塞栓症のリスク因子であり、AMI発症リスクの増加と関係することが知られているが、これらの二次性イベントのうち、いずれの血栓イベントを最初に発症するかは明らかになっていない。そこで、Björck氏らはスウェーデンにおけるAFの大規模患者登録データを用いて、初発AF患者の致死性または非致死性AMI、IS、静脈血栓塞栓症(VTE)の初発イベントの長期発症リスクを検討した。
対象は、1987~2012年にSwedish Inpatient Registerに登録されたAMI、IS、VTEの既往歴がない初発AF患者49万6,173例。2013年12月31日まで追跡し、1年後、5年後、10年後の致死性または非致死性AMI、IS、VTE〔深部静脈血栓症(DVT)または肺塞栓症(PE)〕の初発イベントを記録し、イベント発症率を算出した。
女性でより高い二次性イベント発症リスク
対象の年齢は18~84歳と幅広く、男性が53%(平均年齢70.2歳)、女性が47%(同76.6歳)を占めた。
ベースライン時の併存疾患は、高血圧(26.5%)、心不全(25.2%)が高率で、AMI以外の虚血性心疾患(16.7%)、がん(12.5%)、糖尿病(11.3%)、心弁膜症(7.0%)、一過性脳虚血発作(TIA、4.0%)が続いた。脳内出血、先天性心疾患、末梢血管障害の既往例は1%未満であった(図1)。
図1. ベースライン時の併存疾患

また、1年後、5年後、10年後における致死性または非致死性AMI、IS、VTEの二次性イベントについて男女別に検討したところ、男性では致死性または非致死性AMI、女性ではISが一貫して最も頻度が高く、これらのイベント発症率は、男女とも経時的に増加する傾向にあった(図2)。
図2. 1年後、5年後、10年後の二次性イベント発症率

(図1、2ともにESC 2017発表データ)
以上の結果から、Björck氏は「初発AF後、最初に発症する二次性イベントは、男性では致死性または非致死性AMIとISがほぼ同率で、女性ではISが最も多かった。VTEは長期的な発症率は高くはなかったが、女性では男性よりも高率であったことから、総合的なリスクは男性より女性の方が高いと考えられた」と結論。さらに、「相対的に二次性イベントの発症リスクが男性よりも女性で高い理由は不明であり、今後さらなる研究が必要」と付言した。









