数年前のANZBMS(The Australian and New Zealand Bone and Mineral Society)で破骨細胞のfissionの演題発表を聴いたときに、大変美しい動画と詳細な解析に驚いた記憶があります。中々論文にならないなーと思っていたのですが、満を持してCELL誌に論文が発表されました。著者を見ると、オーストラリアの骨代謝関係者が多数名前を連ねており、オーストラリアの破骨細胞オタク (osteoclasters)が総力をあげて取り組んだ研究であることがわかります。
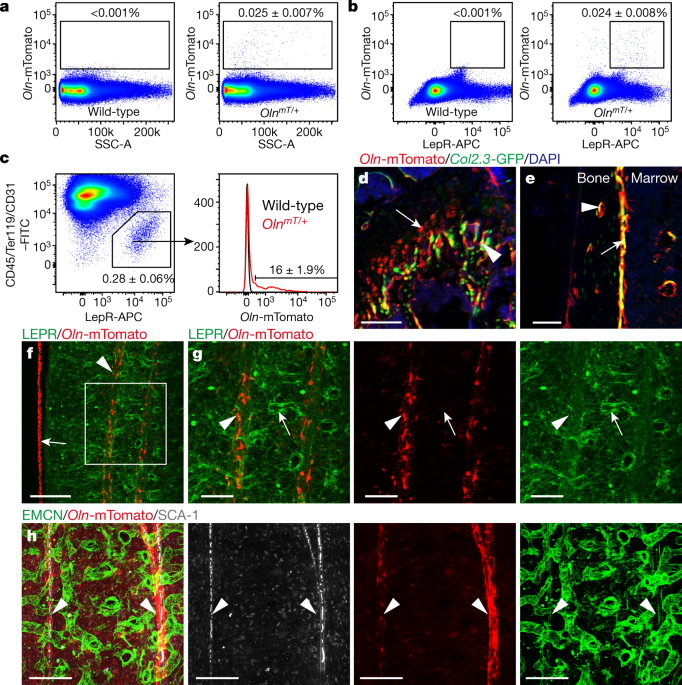
ご存知のように破骨細胞は単球・マクロファージ系の前駆細胞に由来する骨吸収細胞です。その分化にはRANKL (およびM-CSF)の存在が必須で、RANKLは破骨細胞分化のみならず、活性化にも関与していることが明らかになっています。著者らは生体内における多核破骨細胞の動態を明らかにするために、大変凝ったイメージング手法を用いています。破骨細胞のin vivo imagingには、大阪大学の石井優先生らが用いられているようなTRAPやV-ATPase、あるいはcathepsin Kをマーカーとして用いるラベル法がしばしば用いられていますが、これらの分子は必ずしも破骨細胞に特異的ではありません。そこで著者らは放射線照射をしたマウスに①LysmCre/+.TdtomatoLSL/LSLマウスおよび②Blimp-1Egfp/+.Rag-1−/−マウスあるいはCsf1rEgfp/+マウスから採取した骨髄を1:4あるいは1:1でミックスした細胞を移植したマウスを使用しました。さらにこのマウスにAF647-Zolを投与することで骨吸収を行った破骨細胞をラベルしています。破骨細胞オタク以外にはなんのこっちゃだと思いますが、これによってRed, Green, Yellowでtriple labelされた細胞は、ドナー側の2種類のマウス骨髄細胞が融合し、さらに骨吸収を行った破骨細胞であることが確実となるわけです。
このマウスの骨組織を2光子顕微鏡で観察したところ、生体内の破骨細胞は骨内膜上で突起を伸ばした樹状の形態をしており、広範囲なネットワークを形成していました。マウスをRANKLで刺激したところ、細胞融合fusionが促進すると同時に、細胞の一部がちぎれて分裂fissionするような像が認められました。Fissionによって形成されたdaughter cellはアポトーシスによって生じる細胞のfragmentとは異なり、マクロファージによって貪食されることはなく、それ同志がfusionしたり、あるいは破骨細胞とfusionしたりすることも明らかになりました。つまり前駆細胞→fusionによる多核細胞形成→fissionによるdaughter cell形成→fusionという”recycling”を行うことが明らかになりました。
Fissionという現象は定常状態ではほとんど認められず、RANKLによる刺激、あるいはOPG:Fcによる骨吸収抑制状態からの離脱(OPG withdrawal)によって促進されました。著者らはfissionによって形成されたdaughter cellを破骨細胞自体と区別するために”osteomorphs”と命名しています。OsteomorphsはOPG:Fcによる抑制状態においてはosteomorphが骨髄および末梢血中に蓄積し、OPG:Fc投与を中止するとこれらが破骨細胞へと融合することがわかりました。これはデノスマブを中止した時の骨吸収の亢進overshootingが生じる原因と考えられました。
Osteomorphsの遺伝子発現を検討したところ、破骨細胞前駆細胞よりも成熟破骨細胞に近い遺伝子発現profileを示しますが、一部遺伝子発現が異なっていることも明らかになりました。いくつかのosteomorphs特異的遺伝子(例として挙げられているのはDdx56, Myo7a, Wdr89)遺伝子改変マウスでは骨組織の異常が認められました。またosteomorphsに発現する遺伝子のヒトorthologsには骨系統疾患に関連するものも見られました。
骨吸収抑制薬のdiscontinuationを考慮する上でも、破骨細胞のfusion-fissionによるrecyclingは重要な現象であると思います。ついでに言えばosteomorphsは以前溝口俊英先生、高橋直之先生が報告されたquiescent osteoclast precursors(QOPs)に近い細胞なのかもと思いました。
ということで終わりまで読んでくださった方は、めでたく「超絶破骨細胞オタク」に認定させていただきます。
Osteoclasts recycle via osteomorphs during RANKL-stimulated bone resorption
McDonald et al., 2021, Cell 184, 1–18