金沢大学は10月25日、米・ピッツバーグ大学、米・ブリストルマイヤーズスクイブとの共同研究により、ヒト死後脳を用いた研究を行い、統合失調症患者の大脳皮質で「KCNS3」と呼ばれる分子が減少していることを発見したと発表した。
【もっとほかの写真をみる】
成果は、金沢大 医薬保健研究域医学系 脳情報病態学の橋本隆紀准教授、同・医薬保健研究域医学系のDanko Georgiev氏(2013年3月まで)、同・三邉義雄教授(金沢大子どものこころ発達研究センター長兼任)、金沢大子どものこころ発達研究センターの菊知充特任准教授、ピッツバーグ大精神医学部門のDominique Arion氏、John F. Enwright、Dav id A. Lewis氏、ブリストルマイヤーズスクイブ 応用遺伝学部門のJohn P. Corradi氏らの国際共同研究チームによるもの。研究の詳細な内容は、米国東部標準時間10月30日付けで米精神医学専門雑誌「American Journal of Psychiatry」オンライン版に掲載された。
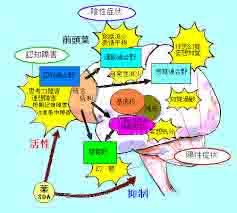
代表的な精神疾患である統合失調症は、幻覚や妄想に加え、注意や思考などの認知機能に障害を引き起こすが、この認知機能障害に対しては効果的な治療法が現時点では確立されていない。認知機能を司る大脳皮質には、ほかの神経細胞の活動を抑える抑制性神経細胞の1種である「パルブアルブミン陽性細胞」(画像1の緑色の球)があり、周囲の多くの神経細胞(画像1の青色の三角形)の活動を同期させ、脳の活動に周期性を与えることで、情報処理を促進し認知機能を支えている。しかし統合失調症では、周期性脳活動の異常が多く報告されており、そこに問題があるというわけだ。
精神疾患の治療法の開発には、病気の症状を引き起こしている脳の変化を分子レベルで解明する必要がある。そのために重要なことの1つが死後脳の研究だ。現在、米国やオーストラリアでは、大規模な死後脳バンクが整備されており、今回の研究は、死後に遺族の同意により提供された脳が保存されているピッツバーグ大精神医学部門の死後脳バンクを利用して行われた。
統合失調症患者22名と性別や年齢などの条件が等しい健常者22名から前頭前野と呼ばれる大脳皮質の部位を切り出して、分子生物学の手法で解析を実視。すると、統合失調症ではKCNS3の発現量が23%ほど低下していることが判明した(画像2)。さらに、別の統合失調症患者14名と健常者14名の前頭前野からパルブアルブミン陽性細胞のみを顕微鏡下に切り出しての解析も実施され、その結果、統合失調症ではKCNS3の発現が41%ほど低下していることが確認されたのである。
KCNS3は、パルブアルブミン陽性細胞の膜に存在する分子で、細胞の中と外をつないでカリウムイオンを通すゲート、つまり「カリウムイオンチャネル」を構成している。KCNS3が作るチャネルは、パルブアルブミン陽性細胞による神経細胞活動の同期化を促進し、周期性を持つ脳活動の形成に役立っていると考えられるという。
KCNS3の減少は、周期性脳活動の異常の背景にある分子変化であり、認知機能障害に結びついていると推察されている。今回の発見により、低下しているKCNS3を活性化することが統合失調症の認知機能障害を改善させる可能性が示され、今後治療法の開発につながることが期待されるとした。