IBDの再燃
UC再燃前にはBacteroides, Escherichia,Eubacterium,Lactobacillus,Ruminococcusといった嫌気性菌が減少し、腸内細菌 叢の多様性が低下すると報告されている。腸内特に下部消化管領域の腸内細菌叢と宿主免疫との調和が重要。
硝酸性窒素の行方
最近の研究では、TLR5をノックアウトしたマウスの腸内細菌は、炎症性サイトカインを誘導し、酸化ストレスをあげている。その結果、脂肪蓄積を通じたメタボに似た症状を示すことまでわかって来た。メタボは単なる肥満ではなく、内なる炎症の長期化が特に腸内細菌が関係しているらしいというところまでわかってきた。
現代の食生活を原因とする病気が今後も解明されていく事でしょう。
⇧
この記事は、実は2010年に書いたものだ。10年前から消化管仮説を立てるが、最近の研究はSCFAを介した脂肪蓄積のメカニズムまで理解されてきた。
餌の量と食物繊維の関係は何万年も比例していたので、冬の到来はSCFAの低下だった。だから内蔵脂肪を溜め込むシグナルになっているんでしょうね。

Nature Medicine 22, 1079–1089 (2016) doi:10.1038/nm.4185
Received 30 March 2016 Accepted 23 August 2016 Published online 06 October 2016
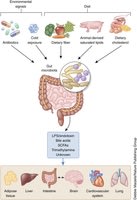
ヒト腸内の生態系は数兆個の細菌からなり、これらの細菌は食物中の多量栄養素を燃料として使って、生物活性を持つ化合物を産生するバイオリアクターを形成している。微生物相に由来するこうした代謝産物は体内の離れた器官にシグナルを送り、これによって腸内細菌は免疫系やホルモン系、あるいは脳(腸脳軸)、さらに宿主の代謝だけでなく他の機能とも連携することができる。微生物と宿主の間のこうした情報交換は、健康な宿主の生体機能を維持する上で必須である。しかし最近、腸内微生物相はさまざまな病気とも関連することが明らかになってきており、その範囲は肥満や炎症性疾患から、神経発達障害と関連した行動的異常あるいは生理的異常まで幅広い。本総説では、微生物相と宿主の間のクロストークおよび腸内マイクロバイオームから腸外部にある器官へのシグナル伝達について論じる。また、このような情報交換が宿主の生理にどのように関わっていると考えられるかを概観し、不適切に設定されたシグナル伝達が多様な疾患に関わる仕組みについても検討する。
小麦粉をあえて使わない、いわゆる「グルテンフリー」のブームの中で、米粉をめぐる新たな動きがあった。
グルテンフリーは、小麦粉などに含まれるグルテンをとらない食事療法のことで、モデルのミランダ・カーさんやテニスのノバク・ジョコビッチ選手らが実践し、健康や美容に感心の高い人々の間で、話題となっている。
町のスーパーにもグルテンフリーをうたう商品は多数並んでいる。
米粉の需要が伸びていることから「日本米粉協会」設立
そんな中、25日、「日本米粉協会」の設立総会が開催された。
小麦粉に代わって米粉の需要が伸びていることから設立された「日本米粉協会」。
参加者の一人で、あきたこまち協会の涌井徹代表は、「私の人生の中で、コメの消費拡大はもうダメだと諦めていた。そこにグルテンフリーというキーワードが登場した」と話す。
そもそもグルテンとは、小麦粉に含まれるたんぱく質の一種で、弾力性と粘着性があり、パンを膨らませたり、うどんにコシを与えるなどの作用がある。
一方で、グルテンには、腸内の悪玉菌を増やしたり、消化不良や吸収阻害、むくみなどの症状を引き起こす場合があるといわれている。
米粉が世界に「グルテンフリー」ブームで日本農業に新たな希望
(画像:ホウドウキョク)
「グルテンフリー」標記で売り上げ増
グルテンフリーの代表格、米粉の工場を訪れると、ショートパスタが製造されていた。
大潟村あきたこまち生産者協会の長谷部満さんは、「小麦独特の風味はないが、食感は通常の麺と同じように仕上げている。どちらかというと、プリッとした食感の方が強くなっている」と話す。
国内のコメ消費が減り続ける中、この工場では10年前から米粉商品を作り始め、昨年、「グルテンフリー」というパッケージに変えてからは、売り上げが急激に伸びたという。
米粉が世界に「グルテンフリー」ブームで日本農業に新たな希望
(画像:ホウドウキョク)
東京・渋谷区のグルテンフリー専門レストラン「リトル・バード」では、パスタをはじめ餃子、バーガー、スイーツなどメニューのすべてが小麦粉を使わず調理されている。


























体によいとされるビフィズス菌が腸内で働く仕組みを解明したのは初めて。27日付の英科学誌ネイチャーに発表する。
研究では、無菌のマウスに特定のビフィズス菌を1週間経口投与し、その後に、下痢などを引き起こす病原性大腸菌O157を感染させて腸内を調べた。その結果、O157による血液中の毒素量が、ビフィズス菌を与えていないマウスに比べて5分の1以下に抑えられていた。与えていないマウスはこの毒素で死んだ。
このほか、大腸の細胞を使った実験から、酢酸が細胞を保護してO157から守っていることがわかった。また、別のビフィズス菌では酢酸を作る量が少なく、血中の毒素量を減らせなかった。
(2011年1月27日08時23分 読売新聞)
急性期病態において腸管は全身性炎症反応の源となる傷害臓器のひとつであり、特に腸内細菌叢の崩壊は感染合併症や予後と関連している。腸内細菌叢を安定化させるプロバイオティクス・プレバイオティクス治療は、侵襲外科手術や外傷後の感染合併症予防に対して有効性が報告されており、急性期疾患での適応が広がっている。
また、基礎研究の発展とともに腸内細菌叢の免疫系への深いかかわりが近年注目されている。腸内細菌叢の解析方法も培養だけなく網羅的なメタゲノム解析によって未知の原因菌が明らかになってきた。このような基礎・臨床研究によって急性期におけるプロバイオティクス・プレバイオティクス治療のメカニズムの解明と新たな治療法の開発が望まれる。
https://www.jstage.jst.go.jp/article/jspen/31/3/31_797/_pdf