がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
712)筋萎縮性側索硬化症(ALS)とミトコンドリアとニコチンアミド・モノヌクレオチド(NMN)
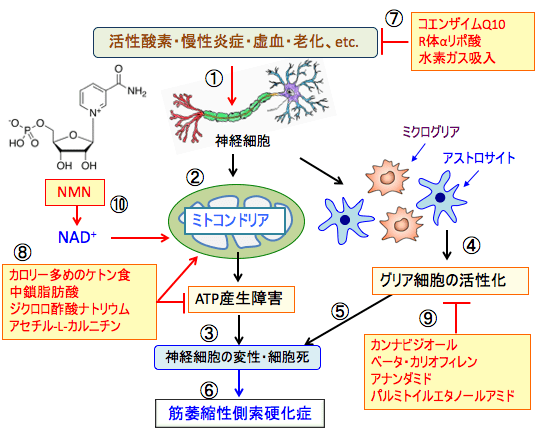
図:活性酸素や慢性炎症や虚血や老化などによって神経細胞が傷害されると(①)、ミトコンドリアでのATP産生が障害され(②)、神経細胞の変性や細胞死が誘導される(③)。一方、炎症などの刺激によってグリア細胞が活性化されると(④)、神経細胞の変性・細胞死が誘導される(⑤)。神経細胞の変性や細胞死は筋萎縮性側索硬化症(ALS)などの神経変性疾患を引き起こす(⑥)。コエンザイムQ10やR体αリポ酸や水素ガス吸入は抗酸化作用によって神経傷害を抑制できる(⑦)。カロリーが高めのケトン食、中鎖脂肪酸、ジクロロ酢酸ナトリウム、アセチル-L-カルニチンはミトコンドリアの働きを高めてATP産生を増やして神経細胞死を抑制する(⑧)。内因性カンナビノイドに作用するカンビジオール、ベータ・カリオフィレン、アナンダミド、パルミトイルエタノールアミドはグリア細胞の活性化を抑制することによって神経細胞死を抑制する(⑨)。体内の生命活動に必須の補酵素のニコチンアミド・アデニン・ジヌクレオチド(nicotinamide adenine dinucleotide:NAD+)の前駆物質であるニコチンアミド・モノヌクレオチド(nicotinamide mononucleotide:NMN)をサプリメントとして補充すると、体内のNAD+量を増やしてミトコンドリア機能を改善して神経細胞死を阻止する(⑩)。これらを併用すると、筋萎縮性側索硬化症の進行の抑制に効果が期待できる。
712)筋萎縮性側索硬化症(ALS)とミトコンドリアとニコチンアミド・モノヌクレオチド(NMN)
【筋萎縮性側索硬化症は運動ニューロンが死滅して発症する】
筋萎縮性側索硬化症(Amyotrophic lateral sclerosis:ALS)は、脳や末梢神経からの命令を筋肉に伝える神経細胞(運動ニューロン)の障害で発症する神経変性疾患の一つです。
手や足や顔など、自分の思いどおりに体を動かすときに必要な随意筋を支配する神経を運動ニューロンといいます。運動ニューロンは、歩行や物を持ち上げたり、飲み込んだりするなど、いろいろな動作をするときに、脳の命令を筋肉に伝える役目をしています。
この運動ニューロンが侵されると、筋肉を動かそうとする信号が伝わらなくなり、筋肉を動かしにくくなったり、筋肉がやせ細ってきます。
運動系が広範に障害されますが、感覚神経や自律神経系や認知機能の障害は通常認めません。
運動ニューロンの変性・消失によって進行性の筋肉の萎縮と筋力低下をきたします。進行が早く、患者さんの半数ほどが発症後3年から5年で呼吸筋麻痺により死亡します。(人工呼吸器の装着による延命は可能)
大リーグの国民的人気選手であったルー・ゲーリッグ(1941年に死亡)がこの病気に罹患したことから別名「ルー・ゲーリッグ病 (Lou Gehrig's disease)」とも呼ばれています。
発病率(1年間に発症する率)は人口10万人当たり1.1~2.5人で、50歳代から発症率が上昇しはじめて、60歳代から70歳台で最も発症率が高く、80歳台では減少傾向となります。
日本での有病率は 人口10万人当たり7~11人人で、平成25年度の特定疾患医療受給者数によると全国で約9,200人がこの病気に罹患しています。
【ALSに有効な治療法はまだ無い】
病理学的には運動ニューロンの選択的な変性・消失がALS発症の原因ですが、なぜ「運動ニューロンが選択的に脱落するのか」というメカニズムに関してはまだ不明です。いろんな仮説が報告されています。
代表的なものがグルタミン酸による興奮性神経毒性(glutamate excitotoxicity)です。
グルタミン酸は神経系においては、グルタミン酸受容体を介して興奮性の刺激を神経シナプス間で伝達する物質で、記憶・学習などの脳高次機能に重要な役割を果たしています。一方、脳虚血などで細胞外に放出されると神経毒として作用し、神経細胞の細胞死を引き起こすことが知られています。
グルタミン酸受容体が活性化されると細胞内のカルシウム濃度が上昇し、細胞死が誘導されます。
このグルタミン酸の興奮性神経毒性がALSにおける神経細胞死に関与していると考えられています。
さらにカルシウム流入とそれによって産生される活性酸素種もALSの病態に関係があると考えられています。
ALSにおける活性酸素の重要性は、一部の家族性ALSがスーパーオキシド・ディスムターゼ 1 (SOD1)の変異により引き起こされることが明らかになって以来注目されています。
SOD1は活性酸素の一種のスーパーオキシドの消去酵素で、最近では、活性酸素のよる酸化傷害は家族性ALSのみならず孤発性ALSにおいてもその発症に関係があるというデータが蓄積されつつあります。
現時点では、ALSに対して根治を期待できる治療法はありません。
ALSの治療薬として、グルタミン酸による神経毒性や活性酸素による酸化傷害の軽減をターゲットにした薬が使われています。
グルタミン酸放出抑制剤のリルゾール(商品名:リルテック)は進行を遅らせることが確かめられており、日本でも1999年より健康保険の適用になっています。「ALS患者の生存期間や人工呼吸器装着までの期間を約3ヵ月間延長させる」という結果が報告されています。
急性脳梗塞などの治療薬として使われてきたフリーラジカル消去剤のエダラボン(商品名:ラジカット)が「筋萎縮性側索硬化症における機能障害の進行抑制」として効能・効果の承認を2015年6月に受けています。
比較的早期の患者を対象にした臨床試験で、日常生活機能の評価スコアでプラセボ群と統計的有意差が認められています。「24週(約6ヵ月)の試験期間において、ALSによる機能障害の進行を約2ヶ月分遅延させることが期待できる」という結果が報告されています。
グルタミン酸放出抑制剤やフリーラジカル消去剤を併用すると、ALSの進行を遅くする効果は期待できますが、進行をストップさせるほどの効果は得られていないようです。
そこで、このような標準治療に加えて、ALSの進行を抑制する効果が期待できる代替医療を検討することも重要です。進行を遅くする可能性のある治療法を組み合わせれば、進行を止めることができるかもしれません。
【ALSの治療法としてミトコンドリアの活性化が注目されている】
神経毒として作用するグルタミン酸は、カルシウム流入を引き起こして活性酸素の産生を高めます。活性酸素はミトコンドリアの酸化傷害を引き起こします。
ミトコンドリアが損傷して機能が低下すると、ATPの産生が低下します。
細胞のエネルギー供給が減少すると、細胞は興奮性神経毒性に対して抵抗力がさらに弱くなります。
この悪循環を薬物治療で断ち切ればALSの進行を遅らせることが可能と考えられています。
つまり、グルタミン酸の神経毒性の抑制、活性酸素による酸化傷害の抑制、ミトコンドリア障害の抑制と機能の活性化の組合せの可能性が指摘されています。

図:様々な要因がALS(筋萎縮性側索硬化症)の発症原因に関与している。グルタミン酸の放出抑制、酸化ストレスの軽減、ミトコンドリアの活性化、神経栄養因子の産生刺激、グリア細胞の活性化抑制などが治療の主なターゲットになる。
サプリメントを使ったALSの治療法としてDeannaプロトコール(Deanna protocol)というのがあります。
これは抗酸化剤(グルタチオン、ニコチンアミド・アデニン・ジヌクレオチド、コエンザイムQ10、ユビキノール)、中鎖脂肪酸(MCTオイル)、アルギニン、αケトグルタール酸、GAGA(γアミノ酪酸)などが入っており、神経細胞のミトコンドリアの酸化傷害を防ぎながら、ミトコンドリアでのTCA回路と酸化的リン酸化を亢進してATP産生を増やすことを目的にしています。
このように、神経細胞のミトコンドリアの機能が低下してエネルギーのATP産生が低下して細胞死が起こることがALSの発症メカニズムに関与しているという報告が増えています。
以下のような論文があります。
Metabolic Dysfunctions in Amyotrophic Lateral Sclerosis Pathogenesis and Potential Metabolic Treatments(筋萎縮性側索硬化症の発症における代謝異常と代謝治療の可能性)Front Neurosci. 2016; 10: 611.
【要旨】
筋萎縮性側索硬化症(Amyotrophic lateral sclerosis:ALS)は致死性の神経変性疾患であり、大脳と脊髄における運動神経の脱落によって特徴づけられる。
運動神経の細胞死は筋肉の神経支配が無くなり、筋肉の萎縮や麻痺を引き起こし、最終的には呼吸機能の麻痺から死に至る。
ALS患者やALSの動物実験モデルの研究から、ALSの発症とその進展の機序にエネルギー代謝の異常が関与していることを示すエビデンスが増えている。
特に、糖代謝の低下とミトコンドリア機能の異常が中枢神経系組織や筋肉組織のATPの利用を妨げている。
ALSにおけるミトコンドリア機能の改善を目標にした代謝治療が幾つか試みられており、ALSの機能改善に様々な効果を示している。
ALSの実験モデルにおいて代謝をターゲットにした治療の効果は、運動障害の発症を遅らせ、運動神経を保護し、生存期間を延長することが明らかになっており、ALSの発症メカニズムに代謝の異常が重要な関与をしていることを示している。
ALSに対する代謝治療の有効性を検証する比較対照臨床試験を早急に実施する必要がある。
さらに、ALS患者やALSの動物実験モデルにおけるエネルギー代謝の異常を解明することは、代謝をターゲットにした有効な治療法の開発に必要であり、このような治療法はALSの進行を遅らせ、ALS患者の延命につながる。
神経細胞のエネルギー源はグルコース(ブドウ糖)ですが、ALSの運動ニューロンではグルコースの取込みも代謝も低下し、ミトコンドリアでのATP産生が低下してエネルギー不足になって細胞死が引き起こされているので、ミトコンドリアの働きを高める方法はALSの進行を抑制できるという意見です。
神経変性疾患ではミトコンドリアの働きが低下してATP産生が低下して死滅するので、ミトコンドリアの働きを亢進すると、神経細胞死を避けることができるということです。
【ALS患者は肥満の方が生存期間が長い】
ALSでは栄養状態が良いほど生存期間が長いことが明らかになっています。
ALSの動物実験モデルを使った実験では、高脂肪食で運動ニューロンの死滅が減少し、生存期間が20%延長したという報告があります。
高脂肪食(脂肪47%、炭水化物38%、たんぱく質15%)と普通食(脂肪17%、炭水化物64%、たんぱく質15%)の比較では、普通食の生存期間が180日以下に対して高脂肪食では220日(一部のマウスは270日以上生存)という結果が報告されています。
BMI(body mass index)とALS患者の生存期間が比例するという報告があります。
100万人以上を14〜28年間追跡して前向き試験では、標準体重の人より肥満の人の方がALSを発症するリスクは30〜40%低いという結果が報告されています。
結論的には、少し肥満になるくらいにカロリーオーバーの食事がALSの生存期間を延ばす効果が期待できるということです。
【ALSの代謝治療】
前述の論文の中で、ミトコンドリアの働きを高めるサプリメントや薬や食事療法が解説されています。その多くは、「ミトコンドリアを活性化してがん細胞を自滅させる治療」にも使われています。以下のようなものが記載されています。
○ ケトン食とカプリル酸トリグリセリド:
ケトン食は高脂肪+超低糖質食によって血中のケトン体(アセト酢酸、βヒドロキシ酪酸)を増やす食事です。
ケトン体は、グルコースの代替エネルギー源として神経細胞に利用され、ミトコンドリアでATP産生に使われます。
中鎖脂肪酸の炭素数8個のカプリル酸は肝臓で速やかに代謝されてケトン体の産生を高めます。
米国では中鎖脂肪酸トリグリセリド(中鎖脂肪酸中性脂肪)のカプリル酸トリグリセリドがアルツハイマー病の治療に有効な医療食( medical food) として認可されています(2009年3月にFDAが認可)。
神経細胞はグルコース(ブドウ糖)とケトン体しかエネルギー源として利用できないのですが、アルツハイマー病ではグルコースの取り込みや利用に障害があり、そのため中鎖脂肪酸を摂取してケトン体の産生を増やすと神経組織のエネルギー産生が改善して症状が良くなると考えられています。
ケトン体のβヒドロキシ酪酸には、抗炎症・抗酸化・抗アポトーシスの機序による神経細胞保護作用が報告されています。
ケトン食が、アルツハイマー病や脳外傷や脊髄損傷や脳虚血の治療に有効であることが報告されています。
ケトン食や中鎖脂肪酸による神経保護作用や神経機能改善効果に関しては327話、330話、386話、468話、481話、482話などで解説しています。
ケトン食を実践する場合、体重が減少しやすいのですが、体重を減らさないように脂肪やたんぱく質を多く摂取することが大切です。肥満の方が生存期間が長いという結果が出ているからです。
脂肪は、脳の働きに良いオメガ3系不飽和脂肪酸(DHAやEPAやαリノレン酸)、ケトン体の産生を増やす中鎖脂肪酸、抗酸化成分を多く含むオリーブオイルを多く摂取し、オメガ6系不飽和脂肪酸や動物性脂肪を減らすことが重要です。
○ ジクロロ酢酸ナトリウム(Sodium Dichloroacetate):
ジクロロ酢酸ナトリウムはピルビン酸脱水素酵素キナーゼを阻害してピルビン酸脱水素酵素を活性化します。ピルビン酸脱水素酵素はピルビン酸をアセチルCoAに変換する酵素で、ミトコンドリアでのTCA回路での代謝を亢進します。
がん細胞のミトコンドリアを活性化するときも使います。がん細胞のミトコンドリアをジクロロ酢酸で活性化するとがん細胞を死滅させることができます。(506話参照)
ジクロロ酢酸ナトリウムはミトコンドリアでのグルコース代謝とATP産生を亢進します。
ALSの動物実験モデルでジクロロ酢酸ナトリウムは脊髄の運動ニューロンの減少を25%抑制し、ALSの運動機能障害の発症を遅らせ、生存期間を延ばす効果が報告されています。
医薬品のジクロロ酢酸ジイソプロピルアミン製剤のリバオールもミトコンドリアの活性を高めます。
ジクロロ酢酸ナトリウムやジクロロ酢酸ジイソプロピルアミンを摂取するときはビタミンB1を多めに摂取します。
健康飲料のリゲインにはジクロロ酢酸ジイソプロピルアミンとビタミンB1が入っています。体力や運動能力を高める効能を宣伝している健康飲料の多くにジクロロ酢酸ジイソプロピルアミンとビタミンB1が添加されてます。
○ コエンザイムQ10:
ミトコンドリアにおける呼吸鎖における電子受容体の一つで、強力な抗酸化作用を持ち、フリーラジカルを消去します。
○ アセチル-L-カルニチン:
アセチル-L-カルニチン(Acetyl-L-Carnitine)はL-カルニチン(L-Carnitine)にアセチル基(CH3CO-)が結合した体内成分です。
L-カルニチンは、生体の脂質代謝に関与するビタミン様物質で、アミノ酸から体内で生合成されます。L-カルニチンは脂肪酸と結合し、脂肪酸をミトコンドリアの内部に運搬する役割を担っています。
体内のL-カルニチンのうち一部はアセチル-L-カルニチンの状態で存在します。
アセチル-L-カルニチンは、血液脳関門を通過して脳内に到達し、アセチルコリンの量を増やします。アセチルコリンは副交感神経や運動神経の末端から放出される神経伝達物質で、アセチルコリンの減少はアルツハイマー病との関連が指摘されています。実際に、アセチル-L-カルニチンはアルツハイマー病初期症状の改善に効果があることが報告されています。
アセチル基はアセチルCoAの合成にも使われます。つまり、アセチル-L-カルニチンは神経細胞のミトコンドリアでの酸素呼吸(酸化的リン酸化)を亢進し、筋肉細胞での脂肪酸のβ酸化を亢進します。
脳外傷、脊髄損傷、脳虚血、脳卒中、アルツハイマー病などの疾患の治療に有効性が示されています。
○ レスベラトロール:
赤ワインに多く含まれるレスベラトロールはサーチュインやAMPK(AMP活性化プロテインキナーゼ)を活性化する作用や抗酸化作用などによって、寿命延長やがん予防効果が報告されています。(513話参照)
【R体αリポ酸と水素ガス吸入】
前述の論文には記載されていませんが、抗酸化作用のあるものとしてR体αリポ酸と水素ガス吸入が有効です。
R体αリポ酸はピルビン酸脱水素酵素の補酵素になるので、ミトコンドリアの活性化にも有効です。
水素ガス(分子状水素:molecular hydrogen)はヒドロキシラジカルを選択的に消去したり抗酸化酵素を誘導する作用(抗酸化作用)、炎症性サイトカインの産生抑制や炎症性の転写因子の抑制などの抗炎症作用があります。
水素ガスは様々な炎症性疾患(自己免疫疾患など)や神経変性疾患(アルツハイマー病やパーキンソン病など)、呼吸器疾患、循環器疾患、糖尿病、腎障害など多くの疾患に対して治療効果を示すことが報告されています。
水素分子は無味無臭のガスで、脂質膜を通って速やかに拡散し、細胞内に入り、ミトコンドリアや核といった細胞内小器官に容易に達することができます。
水素ガスは室温および触媒の不存在下では不活性の気体です。
水素は容易に血液脳関門を通過し、神経組織の細胞に到達します。
細胞毒性などの有害作用はなく、生理的には、腸内細菌が複合糖質の発酵によって体内でも産生されています。そのため、動脈血には水素が含まれており、この水素を細胞が利用していることを示唆しています。
水素はフリーのヒドロキシルラジカルとは反応しますが、その他の活性酸素とは反応しません。ヒドロキシルラジカル以外のフリーラジカルはシグナル伝達などの生理的な機能にも役割を担っているので、ヒドロキシルラジカルだけを消去することは理論的な利点になります。
実際に、様々な実験モデルで、水素はヒドロキシラジカルを消去する作用によって脳組織の酸化傷害から神経細胞を保護する効果が報告されています。
体内に水素を投与する方法として、水素含有水の飲用はほとんど効果が期待できません。水素が水に飽和した状態での水素の量は0.8mM(1.6ppm)程度です。つまり、水素で飽和した水素水を1リットル飲んでも1.6mgの水素を摂取したに過ぎません。
一方、体内では腸内細菌が1日に1リットル程度の水素を発生していると言われています。(実際は、食事の内容などで産生量は個人差があります)
1リットルの水素ガスは、1モルの水素(H2)は2グラムで、体積は22.4リットルになるので(22.4リットルの中にアボガドロ数の約6x(10の23乗)個の水素分子が存在する)、腸内細菌が1日に発生する1リットルの水素は約90mgになります(2÷22.4=0.0892857)。
つまり、体内で毎日100mg(1リットル)程度の水素が腸内で産生されている条件では、水素が飽和した水を1リットルを飲用して体内に1.6mgの水素を摂取しても、どれだけの効果があるのかという議論があります。(426話参照)
【ALSとカンナビノイド】
大麻成分のカンナビノイドは脳虚血による神経細胞死を抑制する作用があります。
脳組織の低酸素や虚血は神経細胞を死滅させる最も一般的な原因となっています。
神経組織が虚血になってグルコースや酸素の供給が止まると、グリア細胞のアストロサイトに乳酸が蓄積して酸性になり、興奮性アミノ酸のグルタミン酸を放出します。
グルタミン酸はグルタミン酸受容体を介して興奮性の刺激を伝達する物質ですが、細胞外に放出されると神経細胞に非常に危険な毒性を示します。グルタミン酸受容体が活性化されると細胞内のカルシウム濃度が上昇し、細胞死が誘導されます。
大麻成分のカンナビジオールはグリア細胞の活性化を抑制し、グルタミン酸による神経細胞のダメージを抑制する作用が報告されています。
カンナビジオールはカンナビノイド受容体のCB1とCB2には作用しません。カンナビジオールが作用する受容体やタンパク質が多数報告されていますが、その中には細胞内への電解質などの物質の出入りを調節する様々な種類のイオンチャネルやトランスポーター、細胞のシグナル伝達に関与する受容体や酵素などが含まれ、これらの物質を活性化したり抑制する作用が報告されています。
アメリカ合衆国はカンナビジオールを脳保護剤として特許を取得して、医薬品として開発しています。(501話)
精油のβカリオフィレンはカンナビノイド受容体CB2のアゴニストです。CB2の活性化は筋萎縮性側索硬化症に効く可能性があります。(434話、435話)
βカリオフィレンとカンナビジオールは相乗効果が期待できます。(436話)
内因性カンナビノイドの一種のパルミトイルエタノールアミドやアナンダミドもアストロサイトやミクログリアの活性化を抑えて神経組織の炎症を抑制する機序で神経変性疾患に効く可能性があります。(440話、442話)
パルミトイルエタノールアミドはヨーロッパでは医薬品として使用されています。アナンダミドも原料として入手できます。(708話)
【ニコチンアミドアデニンジヌクレオチドはミトコンドリアの働きを高める】
前述のDeannaプロトコール(サプリメントを使ったALSの治療法)にニコチンアミド・アデニン・ジヌクレオチドが含まれています。
ニコチンアミド・アデニン・ジヌクレオチド(nicotinamide adenine dinucleotide:NAD+)はナイアシンというビタミンから体内で合成される補酵素です。
補酵素というのは、ある種の酵素の活性発現に必要な低分子の有機化合物です。
NAD+は解糖系やミトコンドリアでのエネルギー産生反応に必要な因子です。
NAD+レベルは加齢とともに低下し、加齢に関連する疾患の発症に重要な役割を担っていることが明らかになっています。
NAD+の細胞内レベルを上昇させる方法は、動物モデルで老化を遅らせ、筋肉機能を回復させ、脳での神経再生を促進し、代謝性疾患を改善することが示されています。
NAD+はサーチュインの活性を高めて、ミトコンドリアの数を増やし、細胞寿命を延ばす効果があります。
【PGC-1αを活性化するとミトコンドリアが増える】
細胞内のミトコンドリアの増殖を刺激することによって、細胞内のミトコンドリアの数と量を増やすことができます。
その方法として、ペルオキシソーム増殖因子活性化受容体(PPAR)のリガンド(ベザフィブラートなど)、AMPプロテインキナーゼ(AMPK)を活性化するメトホルミン、カロリー制限、絶食やケトン食で体内で産生されるケトン体(βヒドロキシ酪酸など)が報告されています。
ミトコンドリアが増えることを「ミトコンドリア新生」や「ミトコンドリア発生」と呼んでいます。細胞内でミトコンドリアが新しく発生することです。通常、既存のミトコンドリアが増大して分かれて増えていきます。
ミトコンドリア新生で最も重要な働きを担っているのが、PGC-1α(Peroxisome Proliferator- activated receptor gamma coactivator-1α)です。日本語訳は「ペルオキシソーム増殖因子活性化受容体γコアクチベーター1α」です。
PPARのリガンド(フェノフィブラート、ベザフィブラートなど)やメトホルミンやレスベラトロールやカロリー制限やβヒドロキシ酪酸はこのPGC-1αを活性化する作用があります(下図)。

図:カロリー制限は体内のエネルギー低下によってAMP/ATP比とNAD+/NADH比を高める(①)。AMP/ATP比の上昇はAMP活性化プロテインキナーゼ(AMPK)を活性化し(②)、NAD+/NADH比の上昇はサーチュイン1(Sirtuin 1)を活性化する(③)。サーチュイン1はセリン・スレオニン・キナーゼのLKB1を活性化し、LKB1はAMPKを活性化する(④)。AMPKはサーチュイン1を活性化する(⑤)。サーチュイン1はPGC-1αの発現を亢進する(⑥)。PGC-1αは、ミトコンドリア新生を亢進し、脂肪酸β酸化とTCA回路と酸化的リン酸化と糖新生とケトン体合成を亢進する(⑦)。メトホルミンやレスベラトロールはミトコンドリアの呼吸酵素複合体Iを阻害して、カロリー制限と類似のメカニズムでPGC-1αたんぱく質の発現を亢進する(⑧)。ケトン体のβヒドロキシ酪酸やPPARαのリガンド(フェノフィブラートやベザフィブラートなど)はPGC-1αたんぱく質の発現を亢進する(⑨)。
ALSの治療では、ミトコンドリアでのエネルギー産生は阻害したくないので、メトホルミンやレスベラトロールやカロリー制限は適さないと思います。それ以外の方法でミトコンドリアを増やすのが良く、その方法としてケトン食(βヒドロキシ酪酸)やPPARαのリガンド(フェノフィブラートやベザフィブラートなど)が適しています。
【サーチュイン1はPGC-1αを活性化してミトコンドリア新生を亢進する】
サーチュイン(サーチュインファミリー)は食物不足(飢餓状態)の時に活性化される遺伝子群で、NAD依存性脱アセチル化酵素です。哺乳類では七つのサーチュイン(SIRT1~7)が存在し、SIRT1、 6、7は核内、SIRT3、4、5はミトコンドリア、SIRT2は細胞質に局在します。
カロリー制限(栄養不良を伴わない低カロリー食事療法)で、霊長類を含む多岐にわたる生物種において老化を遅延させ、寿命を延長させることが知られていますが、このカロリー制限のときに活性化されて寿命延長と抗老化作用に関与するのがサーチュイン遺伝子です。
サーチュイン1はPGC-1αを脱アセチル化することによって活性化します。活性化したPGC-1αはミトコンドリア新生を亢進します。

図:サーチュインはNAD+/NADHの比率の変動を感知することによって、細胞内の栄養素の供給状況や物質代謝の状況を把握している。栄養素、特に糖が減少すると、NAD+が増え、サーチュインが活性化する。細胞質や核に存在するSIRT1やミトコンドリアに存在するSIRT3など7種類が知られている。サーチュインはタンパク質の脱アセチル化(アセチル基を除去する)によって様々な転写因子や酵素などの活性を調整することによって、細胞周期、代謝、抗酸化システム、オートファジーなどの細胞機能に影響する。その結果、細胞老化や発がんを抑制し、寿命を延長する効果を発揮する。
【NAD+はサーチュインを活性化する】
ニコチンアミド・アデニン・ジヌクレオチド(NAD+)は、古くから酸化還元反応の補酵素として知られていますが、ポリADPリボースポリメラーゼ(poly(ADP ribose)polymerases:PARPs)やサーチュインの基質としての役割が知られるようになりました.
特に、サーチュインによるNAD+からニコチンアミド(nicotinamide:NAM)への分解反応は、それと共役するサーチュインによるリシン残基脱アセチル化反応を促進することで、健康や長寿に関わるさまざまな生命現象に関与していることが注目されています。
栄養素、特に糖が減少すると、NAD+が増え、サーチュインが活性化します。
サーチュインはNAD+/NADHの比率の変動を感知することによって、細胞内の栄養素の供給状況や物質代謝の状況を把握しているのです。
サーチュインはタンパク質の脱アセチル化(アセチル基を除去する)によって様々な酵素の活性を調整することによって、細胞周期、代謝、抗酸化システム、オートファジーなどの細胞機能の制御に関与しています。
老化とともにミトコンドリア新生が低下します。特にエネルギー消費の多い筋肉、脳、心臓などでミトコンドリアの機能や新生が低下します。
カロリー制限や運動やレスベラトロールのような食品成分がミトコンドリア機能を維持するメカニズムとして、NAD+とサーチュインが重要と考えられています。
老化に伴いNAD+量およびサーチュイン活性が低下しますが、ニコチンアミドモノヌクレオチド(nicotinamide mononucleotide:NMN)やニコチンアミドリボシド(nicotinamide riboside:NR)などのNAD+中間代謝産物の補充がサーチュインを効果的に再活性化することが明らかになっています。

図:ニコチンアミド・モノヌクレオチド(nicotinamide mononucleotide:NMN)はニコチンアミド・アデニン・ジヌクレオチド(nicotinamide adenine dinucleotide:NAD+)の前駆物質で、NMNをサプリメントとして摂取すると体内のNAD+を増やすことができる。
以上をまとめると、ALSの代替医療として試してみる価値があるのは、カロリーを多めに設定したケトン食、カプリル酸トリグリセリトなどの中鎖脂肪酸、βヒドロキシ酪酸のケトンサプリメント、ジクロロ酢酸ナトリウム(あるいはジクロロ酢酸ジイソプロピルアミン)、水素ガス吸入、R体アルファリポ酸、コエンザイムQ10、アセチル-L-カルニチン、カンナビジオール、βカリオフィレン、パルミトイルエタノールアミド、アナンダミド、ニコチンアミド・モノヌクレオチド(NMN)、ニコチンアミド・リボシド(NR)、ビタミンB製剤(ビタノイリンなど)ということになります。
大麻がALSに有効という報告がありますが、医療大麻は日本では使えないため、カンナビジオール+βカリオフィレン+パルミトイルエタノールアミド+アナンダミドで代替する方法はあります。
ニコチンアミド・モノヌクレオチド(NMN)は数年前まではかなり高額でALSの治療に使うことは困難でしたが、最近はかなり安価になっています。毎日1グラムを摂取しても1ヶ月1〜2万円程度で使用できます。
これらは、基礎実験レベルではALSに対する有効性が示唆されていますが、まだ臨床試験で効果が確認されているわけではありません。
しかし、ALSは進行を止められなければ患者さんの半数くらいは3〜5年で呼吸筋麻痺で人工呼吸器が必要になる疾患なので、新薬を待つ時間はありません。現在の保険適用された治療法では病気の進行を数ヶ月遅らせる程度の効果しかありません。
ある程度のエビデンスや可能性のある方法を組み合せて実践するしかありません。
ポイントは抗酸化作用とミトコンドリアの活性化です。
問題は費用ですが、ニコチンアミド・モノヌクレオチド(NMN)やニコチンアミド・リボシド(NR)がかなり安価になったので、いずれも1ヶ月分が数千円から数万円程度です。全てを使用しなくても、いくつかの方法を選択することもできます。
今までの個人的な臨床経験から、カロリーと中鎖脂肪酸が多めのケトン食、コエンザイムQ10、R体アルファリポ酸、アセチル-L-カルニチン、パルミトイルエタノールアミド、ニコチンアミド・モノヌクレオチド(NMN)、ニコチンアミド・リボシド(NR),ジクロロ酢酸ジイソプロピルアミン(商品名:リバオール)、ビタミンB製剤(ビタノイリン)などの組み合わせが推奨されます。これらの組み合わせで、食費以外のサプリメントと医薬品の費用の合計は1ヶ月分は6万円程度です。
ALSは現時点で有効な治療法がない難病ですが、進行を抑えることはできると思います。
その根拠は、多くの患者さんは中年以降に発症しているからです。先天的な遺伝子異常が原因で発症する場合でも、若年では発症せず中年以降に発症することは、その発症に細胞老化の要因が関与していると推測されます。つまり、細胞老化を抑制する方法を多く行えば、病気の進行を遅らせたり、止めることは可能だと思います。
その方法として、抗酸化とミトコンドリア活性化が基本になると思います。
ここに紹介した方法は「がん細胞のミトコンドリアを活性化して自滅させる方法」でがんの代替医療で長く利用していますが、副作用はほとんど無い(むしろ健康寿命を延ばす)ので、ALSの治療で試してみる価値はあると思います。
最近、ALS患者さんの安楽死をめぐる衝撃的な事件が起こり、安楽死の是非について様々な議論や報道が行われています。
「ALSは有効な治療法の無い致死的な病気」という前提で議論されています。現在使用できる標準治療だけでは数ヶ月の進行抑制しか得られないのは確かです。
しかし、代替療法の研究分野では、ALSの病状の進行を抑える可能性のある方法は多数報告されており、それらは実践してみる価値はあると思います。
| « 711)代謝をタ... | 713)NAD前駆体... » |



