がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
548) シンバスタチン(高脂血症治療薬)は乳がんの再発を予防する
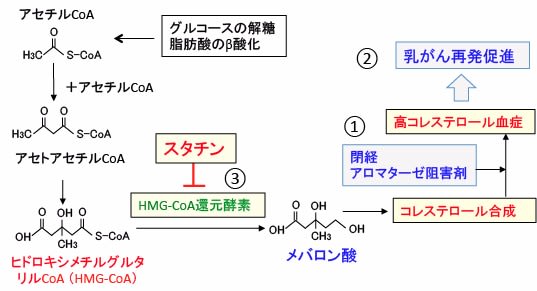
図:閉経やアロマターゼ阻害剤によってエストロゲンの血中濃度が低下すると高コレステロール血症になる(①)。高コレステロール血症は乳がんの再発を促進する(②)。スタチンはヒドロキシメチルグルタリル-CoA(HMG-CoA)からメバロン酸に変換するHMG-CoA還元酵素を阻害することによってコレステロール合成を抑制する(③)。スタチン(特に脂溶性のシンバスタチン)が乳がんの再発を予防する効果が報告されている。
548) シンバスタチン(高脂血症治療薬)は乳がんの再発を予防する
【閉経するとコレステロールが高くなる】
がん再発の予防のために、野菜の豊富な食事や運動や標準体重の維持を目標にしているがん患者さんは多くいます。しかし、閉経後の女性の場合、このような健康的な食生活や運動を実践しているにもかかわらず、「体重が減らない」「コレステロール値が高い」という相談を良く受けます。
特に、乳がんでホルモン療法を受けている場合、「コレステロールが高いので、どうしたら良いか」という相談をよく受けます。薬で下げるべきかどうかという相談です。
コレステロールは脂肪の一種で、細胞膜の構成成分やステロイドホルモン、性ホルモン、胆汁酸、ビタミンDの材料として生命維持に重要な役割を果たしています。
しかし、血中コレステロール値が高い状態(高コレステロール血症)が続くと動脈硬化が促進されるので、食事療法や薬によってコレステロール下げるような治療が行われます。
女性は閉経後、高脂血症になりやすくなります。女性ホルモンのエストロゲンはコレステロールや中性脂肪を低下させる作用があるのですが、閉経後はエストロゲンが低下するためです。
女性の場合、閉経までの間(エストロゲンがある間)は男性に比べて動脈硬化になりにくく、動脈硬化による病気(狭心症や心筋梗塞や脳血管障害)になる確率も男性に比べて低いことが知られています。しかし、閉経後はこのエストロゲンが極端に低下するため、動脈硬化が進んでいきます。女性における虚血性心疾患の発症は、閉経を境に急激に上昇することが知られています。
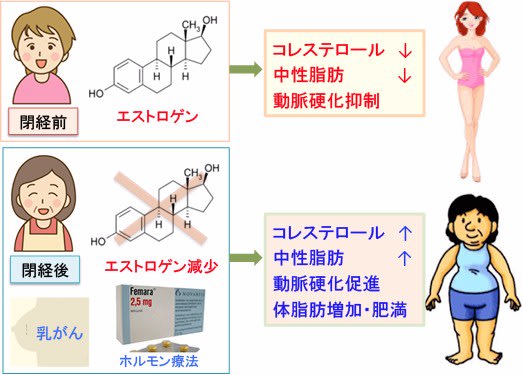
図:女性ホルモンのエストロゲンは血中のコレステロールや中性脂肪の値を低下させ、血管内皮を保護し動脈硬化を予防する作用がある。閉経後や乳がんでホルモン療法を受けている場合は、エストロゲンの減少によってコレステロールや中性脂肪が増え、動脈硬化や肥満が促進される。
エストロゲンはステロイドホルモンの一種で、その受容体(エストロゲン受容体:ER)は細胞内にあります。エストロゲン-受容体複合体は核内へ移動し、特定の遺伝子の転写を活性化することによって効果を現します。
エストロゲンは脂質代謝に対して多彩な作用を示します。エストロゲンは、肝臓に働きかけて、悪玉コレステロールと言われるLDLコレステロール(low density lipoprotein cholesterol)の受容体を増やし、血中のLDLコレステロールの肝内取り込みを増やし、その結果血中のLDLコレステロールや総コレステロールの値が低下します。さらに、善玉のHDLコレステロールの合成を促進する作用もあります。
その他にも多彩な機序でコレステロールや中性脂肪を低下させ、また、血管の内皮細胞や平滑筋細胞やマクロファージなどにも作用して動脈硬化抑制作用を示すことが知られています。
したがって、エストロゲンの分泌が盛んな閉経前にはコレステロールは高くなりにくく、閉経後はエストロゲンの減少によって、高脂血症が起こり、動脈硬化が進行しやすくなるのです。
抗がん剤治療を受けると卵巣機能が低下して閉経が早く起こります。しかも、抗がん剤治療で血管もダメージを受けるので、動脈硬化が起こりやすくなります。
ホルモン依存性(エストロゲン受容体陽性)の乳がんの場合は、薬で閉経状態にしたり、アロマターゼ阻害剤によって体内のエストロゲン産生を低下させる治療(ホルモン療法)が行われます。
このようなエストロゲンの産生を阻害する乳がんのホルモン療法を受けている乳がんサバイバーの場合は、特にコレステロールの上昇や動脈硬化の進行が問題になります。
このような閉経後高脂血症の場合、コレステロールの少ない食事や運動などによってある程度は改善できますが、血中コレステロール値を正常値に維持することが困難な場合も多いようです。
それは、食事からのコレステロールは3割程度で、7割くらいは糖質や脂肪酸を材料にして体内(肝臓や皮膚、腸粘膜、副腎、卵巣、精巣など)で合成されているからです。つまり、いくら食事からのコレステロール摂取を減らしても、体内で合成される量の方が多いので、食事療法や運動では限界があるのです。
コレステロールが多少高めの方が長生きするという意見もあるので放置しても良いのですが、高コレステロール血症の治療薬のスタチン(特に脂溶性のシンバスタチン)が乳がんの再発を予防するという報告が複数あるので、再発リスクの高い場合は、シンバスタチンの併用も考慮するのが良いという意見もあります(後述)。
【スタチンは肝臓でのコレステロールの合成を抑制する】
コレステロールは、アセチルCoA(グルコースや脂肪酸やグルタミンなどの分解によって生成される)から生成されるメバロン酸(Mevalonic acid)を経て生合成されます。この生合成経路をメバロン酸経路と言い、この経路の律速酵素である3-ヒドロキシ-3-メチルグルタリルCoA還元酵素(3-hydroxy-3-methylglutaryl-CoA reductase ;HMG-CoA還元酵素)を阻害すると肝臓でのコレステロール生合成を抑制することができるため、多くのHMG-CoA還元酵素阻害剤が開発され高脂血症治療薬として臨床で使われています。
このようなHMG-CoA還元酵素の働きを阻害することによって血液中のコレステロ-ル値を低下させる薬(HMG-CoA還元酵素阻害剤)の総称をスタチン(Statin)といいます。
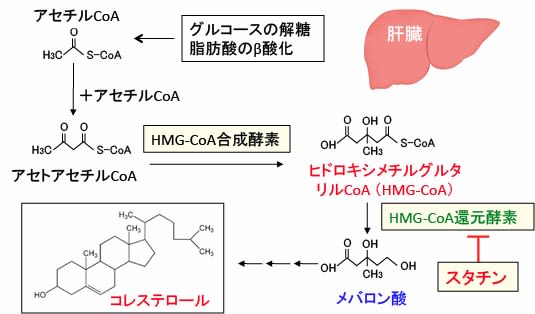
図:スタチンは肝臓においてヒドロキシメチルグルタリル-CoA(HMG-CoA)からメバロン酸に変換するHMG-CoA還元酵素を阻害することによってコレステロール合成を阻害する。
最初のスタチンであるメバスタチンは1973年に青カビの一種から発見され、それ以降、様々な種類のスタチンが開発され、高コレステロール血症の治療薬として世界各国で使用されています。近年の大規模臨床試験により、スタチンは高脂血症患者での心筋梗塞や脳血管障害の発症リスクを低下させる効果があることが明らかにされています。
スタチンのHMG-CoA還元酵素に対する親和性(affinity)は本来の基質であるHMG-CoAの1000倍以上であるため、HMG-CoA還元酵素を強力に阻害します。
【スタチンはがん細胞の増殖を抑える】
メバロン酸はコレステロールの合成に必要なだけでなく、GTP結合タンパク質(Gタンパク質)のイソプレニル化に必要な物質(geranylpyrophophateやfarnesylpyrophosphate)を作ります。(下図)

図:ヒドロキシメチルグルタリル-CoA(HMG-CoA)からメバロン酸に変換するHMG-CoA還元酵素を阻害すると、コレステロール合成の抑制だけでなく、増殖を促進するG結合タンパク質の活性化阻害などを介してがん細胞の増殖を抑える効果も得られる。
GTP結合タンパク質(Gタンパク質)は内在性のGTP加水分解活性をもつタンパク質の総称で、この内、低分子量Gタンパク質群(Ras, Rho,など)は分子量が2万~3万のタンパク質として、これまで100種類以上報告されており、イソプレニル化を受けた後に細胞膜に移行することで、GTP結合型(on)/GDP結合型(off)として細胞内シグナル伝達に関与しています。RasやRhoはがん遺伝子として知られています。
HMG-CoA還元酵素を阻害してイソプレノイド生成が低下すると、低分子量Gタンパク質の活性が低下して、増殖活性が低下します。(イソプレノイドはRasなどの低分子Gタンパク質が細胞膜の脂質に接着するときに必要が生体分子で、それができないと活性化できないので、がん細胞の増殖が抑制されることになります。)
スタチンの抗がん作用については多くの基礎研究が行われており、スタチンによるメバロン酸経路の阻害は、がん細胞のシグナル伝達に影響し、がん細胞の増殖や転移の抑制、血管新生阻害、アポトーシス誘導などの抗がん作用が、培養細胞を使った実験や動物実験で報告されています。
【スタチンのがん予防効果】
スタチンの服用とがんの発生率を検討した大規模臨床試験が多数行われていますが、その結果は肯定と否定の両方があります。
スタチンを長期間服用している人はがんの発生が少ないという報告は多数あります。たとえば、イギリスの研究では、スタチンを服用している人は服用していない人に比べて大腸がんの発生率が43%に減少することが報告されています。スタチンの服用量と服用期間は大腸がんの発生率と逆相関することが示されています。(BMC Gastroenterol 2012 Apr 24; 12:36)
また、20万人以上を対象にしたイスラエルの研究でも、スタチンを服用しているグループではがん全体の発生率が低く、とくに血液腫瘍の発生率が低いことが報告されています。(Prev. Chronic Dis 2012 Aug 9: E137, doi: 10.5888/pcd9.120005)
しかし最近のメタ解析の論文によると「スタチンの服用はがんの発生リスクを低下させる効果は無い」という結論になっています。(PLoS ONE 7(1): e29849 )
がんの種類(前立腺がんなど)によってはスタチン単独でがん予防効果が認められていますので、スタチンのがん予防効果はがんの種類によるようです。また、スタチンの種類によっても抗腫瘍効果が異なるようです。
抗がん剤とスタチンを併用すると抗腫瘍効果が相乗的に高まることが培養細胞や動物を使った実験で示されています。例えば、培養がん細胞を使った実験で、スタチン(lovastatin)とドセタキセルの併用で相乗的に抗腫瘍効果が増強することが報告されています。
しかし、抗がん剤にスタチンを併用した場合の効果を検討した臨床試験では、スタチンが抗がん剤治療の奏功率や生存期間を向上させる効果は認められていません。(抗がん剤自体の効果が限定的なので、上乗せ効果や相乗効果が得られない可能性もあります)
【脂溶性スタチンは乳がん治療後の再発率を低下させる】
細胞内でメバロン酸経路は、コレステロールだけでなく細胞の増殖や機能に重要な働きを持つ多くの物質を産生し、その結果、メバロン酸経路の律速酵素であるHMG-CoA 還元酵素の阻害はがん治療への利用が検討されています。
しかし、スタチンによる抗腫瘍効果は薬剤の種類によって異なる可能性があります。つまり、スタチンには水溶性のものと脂溶性のものがあり、がん細胞に対する効果を期待するには脂溶性のものを使う必要があるようです。
水溶性スタチンは肝臓細胞膜に存在する有機アニオン輸送担体によって細胞内に取り込まれるので、肝細胞に選択的に取り込まれます。
脂溶性スタチンは細胞膜透過性が良いので、あらゆる臓器・組織の細胞内へ移行し得えます。
つまり、肝臓におけるコレステロール産生を抑制する目的では、他の細胞に影響が少ない点で水溶性スタチンの方が良いのですが、がん細胞に取り込まれて、メバロン酸経路を阻害して増殖抑制効果を期待するには脂溶性のものである必要があるようです。
スタチンの中で最も脂溶性の高いのがシンバスタチン(simvastatin)で、乳がんの患者さんがシンバスタチンを服用すると再発率が顕著に低下することが報告されています。
以下のような報告があります。この研究では、水溶性スタチンには再発予防効果は認めなかったという結果でした。
Statin Prescriptions and Breast Cancer Recurrence Risk: Danish Nationwide Prospective Cohort Study (スタチン処方と乳がん再発リスク:デンマークにおける全国規模の前向きコホート研究)J Natl Cancer Inst 2011;103:1461–1468
(要旨)
研究の背景:スタチンが循環器疾患だけでなく、がんを含めた多くの疾患に治療効果を示し、そしてこのような効果がある特定のスタチンの脂溶性の程度に依存する可能性が指摘されている。乳がんの発生率とスタチン服用との関連については多くの研究結果が報告されているが、乳がんの再発に及ぼすスタチンの効果については十分に検討されていない。
方法:1996年から2003年の間にデンマークの乳がん登録(Danish Breast Cancer Cooperative Group registry)に報告されたステージIからIIIの浸潤性乳がんの患者18,769人を対象にしたデンマークの全国規模の前向きコホート研究をした。乳がん診断後の追跡期間の平均は6.8年間であった。脂溶性と水溶性のスタチンの内服状況を調査し、乳がんの再発率との関連を統計的に検討した。
結果:このコホートで最も処方された脂溶性スタチンはシンバスタチンであった。シンバスタチンを服用した乳がん患者では再発率の有意な低下を認め、その再発予防効果は100人の乳がん患者を10年間追跡して、スタチンを服用しない場合に比較して10人の再発を防ぐ効果に相当した。水溶性スタチンを服用した患者では再発率はスタチンを服用しないグループと差を認めなかった。
結論:ステージIからIIIと診断されたデンマークの乳がん患者において、最も脂溶性の高いスタチンであるシンバスタチンの服用は再発率の低下と関連していた。しかしながら、水溶性スタチンを服用していた群においては再発率の低下は認めなかった。
この研究では、デンマークで1996年から2003年に診断された18,769人の乳がん患者を対象に平均6.8年間追跡して3,419人の再発を認めています。6.8年間で18%の再発率です。
シンバスタチンを服用していた乳がんサバイバーはスタチンを服用していない群に比べて再発リスクが70%に減っていました。
この値は、スタチンを服用しない場合に比べて、シンバスタチンを服用すると10年間の追跡で100人あたり10人の再発患者を減らすのに相当するようです。
脂溶性スタチンが乳がんの予後の改善に有効であることはメタ解析でも指摘されています。以下のような報告があります。
Impact of statin use on cancer recurrence and mortality in breast cancer: A systematic review and meta-analysis.(乳がんの再発と死亡に対するスタチンの効果:系統的レヴューとメタ解析)Int J Cancer. 2016 Sep 15;139(6):1281-8.
【要旨】
前臨床試験においてスタチンが乳がんに対して抗腫瘍効果を示すことが報告されている。スタチンは3-ヒドロキシ-3-メチルグルタリルCoA還元酵素(HMG-CoA還元酵素)を阻害する。乳がん細胞におけるHMG-CoA還元酵素の発現は、乳がん患者の予後に関連する因子として知られている。
2015年11月までのMEDLINEとEmbaseの検索後、スタチンの使用と乳がんの転帰との関連を記述した研究を特定するため、817の要約を検討した。
その結果、トータルデ75,684人の女性を含む14件の研究を同定した。10件の臨床試験のメタ解析で、スタチン使用は無再発生存の改善と関連していた(ハザード比0.64; 95%信頼区間 0.53-0.79)。
さらに、親水性スタチンの使用は、無再発生存の改善と関連していないため(ハザード比0.80; 95%信頼区間 0.44-1.46)、この無再発生存の改善は親油性スタチン(ハザード比 0.72; 95%信頼区間 0.59-0.89)の使用に限定されるようであった。
スタチンの使用は全生存期間を改善した(8試験、ハザード比 0.66; 95%信頼区間 0.44-0.99)。
この関係はあまり正確ではないが(6件の研究、ハザード比 0.70; 95%信頼区間 0.46-1.06)、スタチン使用はがん特異的生存率を改善した。
結論として、スタチン、特に親油性スタチンの使用は、乳がん患者の無再発生存率の改善を示す。スタチンの使用者は全生存期間およびがん特異的生存率も改善した。
これらの研究結果は、前向き無作為化コホートで検証されるべきであり、スタチンの種類や用量や薬剤の有効性を予測し得るバイオマーカーを明らかにする必要がある。
【スタチンが乳がんの再発を予防する十分なエビデンスがある】
以下のような報告があります。
Statins and risk of breast cancer recurrence(スタチンと乳がん再発リスク)Breast Cancer (Dove Med Press). 2016; 8: 199–205.
手術と補助化学療法を受けたステージI, II, IIIの乳がん患者610人を対象にした臨床試験です。610人のうち83人(13.6%)が高脂血症の治療目的でスタチンを服用していました。
無再発生存期間の平均は、スタチン服用群が16.5年、対照群が10.2年で、統計的有意な無再発生存期間の延長をみとめました(P=0.028)。若年者のみを比較すると、スタチンによる再発予防効果はさらに顕著でした(スタチン服用群が20年に対して対照群は10年、P=0.006)。
この論文の結論は「比較的早期の乳がん、特に若い患者において、スタチンの服用は再発予防に有効である」となっています。
スタチンの乳がん再発予防効果は十分なエビデンスがあるという報告もあります。
Statins and breast cancer prognosis: evidence and opportunities(スタチンと乳がんの予後:証拠と機会)Lancet Oncol. 2014 Sep; 15(10): e461–e468.
【要旨】
多くの前臨床および疫学的証拠は、HMG-CoA還元酵素阻害剤(スタチン)の抗がん作用を支持している。 疫学的研究では、スタチン使用が乳がん発症率を低下させる証拠はない。しかし、スタチン、特にシンバスタチンが乳がん治療後の予後を良くすることは疫学的証拠がある。
スタチンによる乳がんの補助療法の有効性を検証する臨床試験を実施することを正当化する十分なエビデンスがある。我々は、そのような臨床試験ができるだけ早く実施されることを提唱する。
乳がんの再発に対するスタチンの予防効果が臨床試験によって証明されれば、安全で、耐容性があり、安価な治療法によって、乳がん患者の予後を改善することができる。
私たちは、スタチンの安全性と有効性の予測バイオマーカーの候補などについて考察し、そのような試験の登録、フォローアップ、分析の重要な課題に対する解決策を提示する。
「スタチンが乳がん治療後の再発を予防することを示す疫学的証拠があるので、前向きの臨床試験で、スタチンの乳がん再発予防効果を早く検証すべきだ」という趣旨の論文です。Lancet Oncologyという超一流のがん専門の学術雑誌に掲載されているので、「スタチンの乳がん再発予防効果」はかなり可能性が高いことを示唆しています。
大規模な前向き臨床試験でその有効性が証明されるまでは、まだエビデンスが十分とは言えませんが、疫学研究の結果の段階で「乳がん患者が再発予防の目的でスタチンを服用する価値はありそうだ」とは言えます。
スタチンが乳がん細胞の増殖や進行を抑制することは、培養細胞を使ったin vitro実験や動物実験で多数報告されています。
人間の研究では、スタチンが乳がんの発症率を低下することは示されていませんが、乳がんの再発率を低下させることは、前述のように多くの研究で支持されています。
このエビデンスを強化するためには、ランダム化比較試験の実施が必要だという意見です。
【ホルモン療法中のスタチン併用は再発予防効果を高める】
閉経後ホルモン受容体陽性乳がんに対しタモキシフェン、タモキシフェンからレトロゾールへのスイッチ、レトロゾールの治療法を比較する第III相臨床試験(BIG1-98)が米国で行われています。
このBIG1-98試験において、コレステロール値,高脂血症治療薬内服の有無,試験治療中の高脂血症治療薬の内服開始の有無と再発との関係が検討されています。以下のような論文が最近報告されています。
Cholesterol, Cholesterol-Lowering Medication Use, and Breast Cancer Outcome in the BIG 1-98 Study.(BIG 1-98研究におけるコレステロール,コレステロールを低下させる薬剤の使用,および,乳がんの転帰)J Clin Oncol. 2017 Apr 10;35(11):1179-1188.
【要旨】
目的:コレステロールを低下させる薬剤(Cholesterol-lowering medication:CLM)が乳がんの再発を防ぐ作用があることが報告されている。
CML(コレステロールを低下させる薬)がエストロゲン作用のあるコレステロール代謝産物の27-ヒドロキシコレステロール(27-hydroxycholesterol)の血中レベルを低下させることによってエストロゲン受容体を介するシグナルを減弱する可能性がある。
また、血清中のコレステロール値や高コレステロール血症自体に対するホルモン療法の作用が、アロマターゼ阻害剤の抗腫瘍効果を妨げている可能性もある。
患者と方法:Breast International Group(BIG)が、ランダム化第III相二重盲検試験(BIG 1-98)を実施した。このBIG1-98試験では、1998~2003年にかけて診断された早期ステージのホルモン受容体陽性の浸潤性乳がんのある閉経後女性8,010名が参加した。
血清中の総コレステロール値とCLM使用の有無を、調査開始時および6ヶ月ごとに5.5年間測定しホルモン療法中のCLM開始と転帰との関係を調査した。
評価項目は、無病生存期間、乳がん無再発期間、無遠隔転生存期間であった。
結果:コレステロール値はタモキシフェン療法中に減少した。内分泌療法中にCLMを開始した患者789名の内訳は,レトロゾールのみ318名,タモキシフェン+レトロゾール189名,レトロゾール+タモキシフェン176名,レトロゾールのみ106名であった。
内分泌療法中のCLM開始は、無病生存期間(HR 0.79,95% CI 0.66~0.95,P=0.01)、乳がん無再発期間(HR 0.76,95% CI 0.60~0.97,P=0.02)、無遠隔転移期間(HR 0.74,95% CI 0.56~0.97,P=0.03)の改善と関係があった。
結論:ホルモン受容体陽性の早期のステージの乳がんのホルモン療法中のコレステロールを低下する治療薬の併用は、乳がんの再発を予防する効果が期待できる。この観察研究の結果を確認するために前向きのランダム化試験の実施が必要である。
この研究は、スタチンに限定したものでなく、その他の高脂血症治療薬も含まれています。コレステロールの代謝物である27-hydroxycholestrolはエストロゲン受容体のリガンドとして作用し,腫瘍増殖に関与している考えられているので、コレステロールを低下させること自体に乳がん再発抑制効果があります。
HMG-CoA還元酵素は乳がんに発現し,予後関連因子であることが同定されています。したがって、HMG-CoA還元酵素阻害剤のスタチン(特に脂溶性のシンバスタチン)は、乳がん細胞の増殖を抑制する効果があります。
この研究は観察研究であるため,今後前向き試験で真に高脂血症治療薬が乳がんの予後を改善するかを検証する必要があります。しかし、ホルモン受容体陽性乳がんの術後補助内分泌療法中の患者において,高脂血症の治療が予後を改善する可能性が高いので、ホルモン療法中にコレステロールが高くなった場合は、高脂血症の治療を積極的に受けた方が良いというエビデンスはあると言えます。特に、シンバスタチンによる治療が推奨されます。
一般に,アロマターゼ阻害薬は高脂血症となることから,高脂血症治療薬によるメリットが高いと想定されます。
一方,タモキシフェンはコレストレール値を下げるため,高脂血症の効果はさほどでないと考えられます。
つまり、アロマターゼ阻害剤によるホルモン療法中で、コレステロール値が高い場合は、シンバスタチンを使うエビデンスは高いと言えます。
スタチンのがん再発予防効果はがん全体に適用できるようです。最近の研究で以下のような報告があります。
Effects of statins on cancer mortality and progression: A systematic review and meta-analysis of 95 cohorts including 1,111,407 individuals.(がん死亡とがん進展におけるスタチンの効果:1,111,407人を含む95件のコホート研究の系統的レヴューとメタ解析)Int J Cancer. 2017 Mar 1;140(5):1068-1081.
がん細胞の増殖やアポトーシスや悪性進展の制御におけるスタチンの作用が知られており、がんの発生予防や再発予防にスタチンが有効であることが多数の臨床試験で報告されています。
この論文では、2015年5月までに報告された「がん患者におけるスタチン使用とがんの予後」に関して行われた95件のコホート研究の結果をまとめています。
非使用群に比べてスタチン使用群の全死因死亡率のハザード比は0.70 (95%信頼区間:0.66-0.74)と有意な死亡率減少を認めています。
がん死亡率のハザード比は0.60(95%信頼区間:0.47-0.77)、無進展生存率のハザード比は0.74(95%信頼区間:0.65-0.83)、無再発生存率のハザード比は0.53(95%信頼区間:0.40-0.72)といずれも非使用者に比べてリスクの低下を認めています。
がんの診断前からのスタチン服用群の無再発生存率のハザード比0.86(95%信頼区間:0.77-0.96)に比べて、がん診断後の無再発生存率のハザード比0.65(95%信頼区間:0.54-0.79)の方が低く、がん診断後のスタチン服用開始はより再発予防効果が高いことが示されています。
この論文の結論は「Statin therapy has potential survival benefit for patients with malignancy. (がん患者においてスタチン治療は生存期間を延ばす可能性がある)」となっています。
乳がんサバイバーの人はホルモン療法の関係や、更年期に入るとコレステロールが高くなるので、保険でシンバスタチンを処方してもらうこともできます。
高コレステロール血症に対するスタチン治療には反対意見も多くあります。コレステロールはやや高めの方が寿命が延びるという意見もあります。
しかし、乳がん再発リスクが高い場合や血清コレステロール値が高い場合は、乳がんの再発予防の目的でスタチンを服用するメリットはあるように思います。
再発リスクの高い乳がんサバイバーがビタミンD3(394話)、ドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)などのω3系多価不飽和脂肪酸(314話)、メトホルミン(384話)、大豆製食品(340話)、今回のシンバスタチンを服用すると、乳がんの再発リスクをかなり低減できると思います。
なお、シンバスタチンによる再発予防効果は前立腺がんでも報告されています。
また、スタチンとメトホルミンの併用によってスタチン単独の場合よりも死亡率が低下することが前立腺がんで報告されています。
スタチンを服用しているときは、コエンザイムQ10の体内産生が阻害されるので、コエンザイムQ10をサプリメントか医薬品で補充することが推奨されます。
画像をクリックするとサイトに移行します。
| « 547) がん検診... | 549)肝機能改... » |





