がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
536)超高齢者はがんにならない(その1):抗老化とがん予防の共通のメカニズム
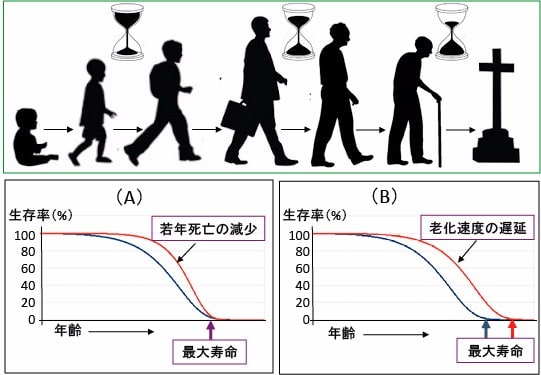
図:寿命(生まれてから死ぬまでの時間)には限界がある。人間の最大寿命(生理的寿命、限界寿命)は120歳前後と言われている。公衆衛生や栄養状態の改善や、医療の進歩によって若年での死亡を減らせば平均寿命を延ばすことができる。しかし、この場合は最大寿命を延ばすことはできない(A)。老化速度を遅延できれば、平均寿命と最大寿命の両方を延長できる(B)。老化抑制と発がん抑制の共通のメカニズムを理解すると、がんにならずに長寿を達成できる。
536)超高齢者はがんにならない(その1):抗老化とがん予防の共通のメカニズム
【寿命には限界がある】
人間が生まれてから死ぬまでの時間を寿命と言います。
その長さには非常に個人差がありますが、不慮の事故やがんなどの生命に関わる病気に罹らなければ、現在の日本では80歳以上の寿命が期待できる状況です。
2015年の日本人の平均寿命は女性が87.05歳で、男性が80.79歳というデータが発表されています。
世界一の高齢者は、過去には122歳164日生きたフランス人女性(ジャンヌ・カルマン)や、男性では120歳238日の日本の泉重千代さんがいますが、最近では115歳~117歳が世界一になっています。人間の寿命の限界は120歳前後だと考えられています。
寿命は個人差があり、遺伝的な要因も関与していますが、生活環境の改善や医療によって平均寿命を延ばすことは可能です。
個体の寿命は生活環境や病気などによって影響を受けます。
自然界に生活する生物は,他の生物に捕食されたり、感染症や怪我によって生命を奪われることがあります。このように、その生物が実際に生活している場で見られる寿命を生態的寿命と言います。
一方、条件を整えてやった場合に実現する寿命を生理的寿命といいます。天寿を全うして老衰によって死亡する場合の寿命です。生理的寿命は最大寿命や限界寿命とも言います。
動物園の動物の寿命が長いのは、生活環境や餌や医療によって、寿命を延ばす条件が整っているためです。生態的寿命の平均が5年くらいの動物でも、条件を良くすれば、20年以上生きることもできます。
人間も、開発途上国よりも先進国の方が寿命が長いのは、豊富な食糧や衛生的な生活環境や進歩した医療の恩恵によることは確かです。
過去1世紀において、工業先進国では経済の発展に伴い、医療の進歩と、栄養状態や生活環境や公衆衛生の改善によって寿命は顕著に延長しました。
Lancet誌オンライン版2017年2月22日号には、先進工業国はいずれも余命が延長し続け、2030年までに50%以上の確率で韓国女性の寿命が90歳を超えるとの研究結果が報告されています。この論文では、日本人女性の平均余命は2030年までに、35%の確率で伸びが留まるか短縮すると報告しています。つまり、限界に近づきつつあるということです。
諸々の理由で寿命には限界があると考えられています。
【ヒトの細胞の分裂回数は50回が限界】
私達の体の中では毎日約200分の1の細胞がアポトーシス(プログラム細胞死)で死んで、組織幹細胞が分裂して補っています。新しい細胞に交代することによって組織や臓器の若返りを行なっているのです。
細胞にはキズを修復する機能があるのですが、時間が経つとつぎはぎだらけの古い(老化した)細胞になって機能が落ちます。ある程度古くなると自分で細胞死のスイッチをいれて自殺(自滅)し、新しく生まれた若い細胞にまかせたほうが組織全体の機能を良い状態に維持する上では都合がよいので、アポトーシスの仕組みが生物の進化の過程で発達したようです。「細胞交代型の若返り」といえます。
しかし、体の正常な細胞は分裂できる回数に限りがあります。
1960年代にアメリカの生物学者ヘイフリックは、培養した正常の細胞には寿命があることを発見しました。
人間の胎児から取り出した線維芽細胞を培養すると次第に分裂の速度が落ちて、約50回の分裂回数が限界で、いくら栄養物質や増殖を促進する物質を加えても分裂することはできずに最後は死んでしまいます。
一方、成人の人間から取り出した線維芽細胞の分裂できる回数はその年齢に応じて減少していることも明らかになっています。
すなわち、細胞の中には細胞の分裂した回数をきちんと数える装置があって、ある回数を過ぎると細胞は死を向かえるプログラムが働き出すのです。
このように、正常な細胞が分裂できる回数には限界があることを「ヘイフリックの限界」と言います。
ヒトの正常細胞の分裂回数は約50回が限界ということで、それ以上は分裂できないので、寿命があるということになります。

図:ヘイフリックの実験。赤ん坊や成人や老人の皮膚から線維芽細胞を採取してシャーレで培養すると、年齢が若い個体から採取した細胞ほど多く分裂できる。赤ん坊の細胞も細胞分裂の回数には限界があり、やがて細胞分裂を停止して死滅する。細胞の分裂回数はヒトの場合は50回くらいが限界で、これ以上は分裂できない。これをヘイフリック限界という。
さらに、哺乳動物の種の生理的寿命(最大寿命)とその動物から採取した皮膚線維芽細胞の分裂回数の限界(ヘイフリック限界)は正の相関関係が認められています。これは正常細胞の分裂回数に限界があることが、動物の最大寿命に限界がある理由であることを意味しています。

図:哺乳類の種の生理的寿命とヘイフリック限界の関係
出典:Clin Transl Oncol 2003;5:249-65(Exploring cellular senescence as a tumor suppressor mechanism)
【細胞分裂のたびに染色体の末端が短くなる】
細胞の分裂回数を記録する機構としてテロメアという染色体の末端にある特殊な構造が関与しています。
染色体とは細胞が分裂するときに核の中にみられる棒状や糸状の構造体で、DNAと蛋白質からできています。
DNAにはA,G,C,Tという4種類の成分(塩基)が並んでいて蛋白質を作り出す情報が書き込まれています。一つの細胞核に約30億塩基対からなるDNAが存在します。これは1本に引き伸ばすと約2mの長さになります。
DNAは遺伝物質の本体であり、細胞が機能するための命令を出す指令塔のようなものです。細胞が分裂する前には、DNAのコピー(複製)が作られて子の細胞に同じものがわたされます。
その染色体DNAの末端部分にはTTAGGGという配列が多数繰り返された構造がみつかりテロメアと名付けられました。この6塩基のリピート部分には遺伝情報が入っていないので、なくなっても遺伝子の発現には問題ない部分です。
しかし、テロメアは染色体の安定化に役立っていると考えられており、テロメアがないと、染色体どうしの癒着がおこったりします。さらに、テロメアが無くなると細胞はDNAの複製ができなくなります。
DNAは2本の鎖状で、それぞれの鎖を鋳型にして新しいDNA鎖を合成します。新しい鎖を作るとき、DNAポリメラーゼという酵素が鋳型のDNA上を移動しながら、新生DNAを作ります。
この酵素が鋳型のDNAに結合するためには、まずプライマーとよばれるRNAが鋳型のDNAの末端に結合する必要があります。
DNAポリメラーゼはRNAプライマーに結合し、そこから新生DNAの複製を開始します。その際、プライマーが結合した鋳型DNAの末端部は複製されません。そのため、細胞分裂でDNAを複製するたびに、染色体のDNA末端は少しづつ切れて短くなっていきます。
短くなっても問題ないように、遺伝情報とは関係なく必要のないDNA配列(TTAGGGの繰り返し配列)がテロメアとして存在しているのです。しかし、テロメアの長さに限界があるので、いずれはテロメアが無くなると、もはや細胞分裂ができなくなります。
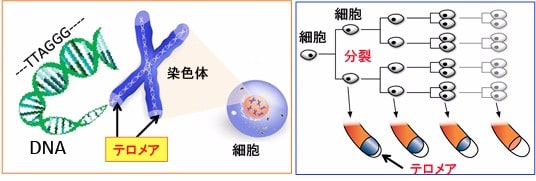
図:染色体の末端にはテロメアという構造があり、この部分のDNAはTTAGGGという配列が多数繰り返されている。細胞分裂するたびに、このテロメア部分のDNAは短くなり、テロメアが無くなった時点で、細胞はそれ以上に分裂することができなくなり死滅する。
テロメアの長さには限りがあるのでやがて使い尽くされると、細胞老化のシグナルが発動してしまいます。
つまり、テロメアとは「命の回数券」のようなものであり、分裂する度に回数券を一枚づつちぎって使い、やがて使い切ってしまうと細胞の寿命がくるというわけです。
体の新陳代謝のためには細胞の若返りが必要ですが、それが次第にできなくなることが老化の原因となるのです。
ちなみに生殖細胞や幹細胞(骨髄細胞や消化管粘膜上皮細胞のように細胞回転が早い細胞を供給している細胞)やがん細胞のように無限に分裂できる細胞もありますが、これはテロメアを延ばすことができるテロメラーゼという酵素が働いて、テロメアの長さを維持しているからです。普通の細胞にはテロメラーゼ活性はほとんどありません。
がんの治療においては、がん細胞のテロメラーゼ活性を阻害する薬の開発が行われています。
一方、抗老化の領域では、細胞のテロメラーゼ活性を高める研究が行われています。組織の細胞を供給する組織幹細胞のテロメラーゼ活性が低下しなければ、永久に若い細胞を供給できることになります。運動や食事やサプリメントなどで細胞のテロメラーゼ活性を高めることができる可能性が報告されています。
例えば、運動している人たちのほうがテロメラーゼ活性が高く、テロメアも長いという報告があります。
漢方で人参と並んで補気薬(気の量を増す)の代表のオウギ(黄耆)は欧米でもアストラガルス(Astragalus)と呼ばれてサプリメントとして人気がありますが、このアストラガルスのある成分が、がんの発生率を高めることなく、正常細胞のテロラーゼ活性を刺激してテロメアの長さを伸ばすという報告があります。
この成分はAT-65という名称で米国で販売されており、日本のアマゾンでも並行輸入で販売されています。ただ、結構高額です。
漢方的発想では、黄耆に含まれるある単一の活性成分をカプセルに入れて飲むより、黄耆そのもの、あるいは他の生薬と組み合せて、煎じ薬として摂取するのが良いように思います。黄耆には、アディポネクチンを増やすなど、他の成分による抗老化作用もあるからです。(黄耆のアディポネクチン産生刺激作用については292話参照)
がんの漢方治療を長く実践してきて、がんを予防し寿命を延ばす漢方薬は現実的に可能だと考えています。

図:細胞分裂するたびにテロメアが短縮して、その結果、細胞は分裂を停止する。テロメアの長さを維持するテロメラーゼの活性を亢進すると細胞を不死化できる。
【フリーラジカルが老化を促進する】
老化を促進する要因として「老化のフリーラジカル説」あるいは「障害蓄積説」というのがあります。1956年、Harmanが生体内で生じる活性酸素などのフリーラジカルが老化に関与するという考えを提唱しています。
フリーラジカルは他の原子や分子と反応して、相手から電子を奪い取り、相手の物質を酸化する力が強い分子です。DNA・蛋白質・脂質など細胞を構成する成分の活性酸素による障害の蓄積が老化を促進する原因として重要であるというのが「老化のフリーラジカル説(エラー蓄積説)」です。
フリーラジカルの害を抑えることができれば、老化のスピードを遅くして、いろんな病気の発生を防ぐことができることが明らかになってきました。
ぼけの原因である脳細胞の変性疾患(アルツハイマー病など)の発病には、活性酸素による神経細胞の障害が重要な役割を果たしています。私達の脳は高度不飽和脂肪酸を多く含み、非常に酸化されやすい組織です。老化した動物の脳を潰してみると、老化のパラメーターになる過酸化脂質の量が増加している、つまり活性酸素による酸化が進んでいることが知られています。
高齢者の視力障害の原因として頻度が高い白内障は、その発症機序に関与している最も重要な因子としてフリーラジカルがあげられています。紫外線が水晶体内でスーパーオキシドなどのフリーラジカルを産生し、水晶体蛋白を酸化変性させ、その結果水晶体の透過性が低下し、白内障が発症すると考えられています。
このように多くの成人病や老化性疾患の原因にフリーラジカルの害が存在します。がん・心筋梗塞・脳血管疾患は日本人の3大死因といわれ、死亡原因の3分の2以上を占めていますが、いずれもフリーラジカルの害が関連しています。
フリーラジカルを消去する体内の防御機能は歳とともに低下し、がん年令といわれる40歳台にはピーク時(20歳前後)の半分以下に減っているといわれています。生体成分の酸化障害が進行すると免疫組織を初めとする多くの臓器や組織の働きが悪くなり、血液循環が低下すると新陳代謝も低下して、ますます病気をおこしやすい体になります。
体内の抗酸化力を高める方法としてホルミシス(504話)や転写因子のFoxOの活性化(339話)が重要なターゲットになります。
【寿命はプログラムされている】
一般的に、多細胞生物では寿命がプログラムされています。
例えば、1年草は花をつけて実がなると、直ぐに枯れます。
ほとんどの昆虫類は産卵すると一生を終えます。
魚類ではサケは排卵後にあるホルモンを分泌して死ぬようにプログラムされています。
ほ乳類や鳥類の場合は、子供を産んでもすぐ死なずに子育ての期間を生きますが、子育ての期間を終了するころには死を迎えるようになっています。
成長に必要な内分泌系や免疫システムも、子育てが終わる頃、あるいは生殖能力を失うころ(更年期)には、体を壊す方法に作用しだします。
たとえば、女性ホルモンや男性ホルモンは乳がんや前立腺がんの発生や進展を促進し、様々な成長因子はがん細胞の増殖を促進し、免疫細胞は自己の細胞を攻撃して自己免疫疾患を起こすようになります。
また前述のように、細胞には分裂の回数に限界を設けるテロメアが存在し、酸素呼吸をすることにより発生する活性酸素が遺伝子や脂質や蛋白質を酸化し、がんや動脈硬化の原因となります。
したがって、年令とともに老化が進み、がんや心臓病などの病気に罹らなくても、多くは90~100歳で老衰によって亡くなる運命にあります。
生物に寿命があるのは、固体が無制限に増えると食糧の確保などで生存が困難になることや、変化する環境に適するように種を進化させて繁栄させるためには、子孫(新しい種)を残したら親(古い種)は消滅させた方が有利だからです。
環境の変化に適応し、種全体の利益のため自ら死ぬという利他的なプログラムが存在し、そのために個体は老化し最終的に死ぬと考えられています。
食糧の枯渇や飢餓など生存に厳しい状況において、個々の細胞や個体が他の細胞や個体のために利他的に死ぬことができる集団は、全ての細胞や個体が利己的な集団よりも進化の過程でのメリットがあります。
例えば、酵母を使った実験で、プログラム細胞死が働く通常の酵母(利他的なグループ)と、プログラム細胞死が起こらなくした酵母(利己的なグループ)を培養するとどうなるかという実験があります。
プログラム細胞死が起こらない利己的グループは個体数を増やす速度が早いので、種の繁栄に有利ですが、そのうち、過剰に増殖するとスペースも食糧も無くなって、生存と繁栄ができなくなります。
集団から老化した個体が死ぬことは、若い世代や適応した世代を生き残らせる作用があります。
医学が発達する前は、ヒトは生殖年齢を終えると歯が弱り視力が低下して、次第に生活が困難になって早めに死を迎えます。しかし、医学の進歩によって生殖年齢を超え、子育てを終えても、さらに30年以上も生存することが可能になっています。
寿命が延びることは、人類の種としての繁栄にはマイナスに作用することになりますが、人類(正確には「脳」)は寿命を延ばすことを夢見てきました。
【人類は老化を抑え寿命を延ばすことを夢見てきた】
生物の寿命は必然的に老化の過程を伴います。
この老化の過程では、生体機能は次第に低下し、様々な慢性疾患が発症し、最終的には死亡します。
そこで、人類は健康状態を高め、寿命を延ばす方法を見つけることを夢見てきました。これが人類が医療を発展させている重要な動機になっています。
人類が不老不死の望みを抱いた一つの現れとして、古代中国では神仙思想という民間信仰が発達しました。東洋の歴史の中には「仙人」と呼ばれるような人たちが現れます。山奥に住み、白髪白髯で、霞を食べて生きている不老不死の超越者、といったイメージで表現されています。
神仙思想は、仙人のように不老不死になりたいという現世利益の実現を追求する点が多くの民衆にも受け入れられ、二千年以上前の中国の戦国時代末期から秦・漢代にかけて広まりました。
紀元前217年に中国を始めて統一した秦の始皇帝も、不老不死の薬(仙薬)を求めて奔走した一人です。始皇帝の命を受けた徐福が、数千人をつれて不老不死の仙薬を求めて航海に出たという話しが『史記』や『漢書』に記載されています。始皇帝は49歳で死亡していますが、皮肉にも仙薬として飲んでいた水銀の中毒だったと言われています。
このような時代に、現在の漢方の考え方の基本が芽生え、中国医学の古典が記されています。このような考え方を基盤に持つ中国医学では、日頃の食事による病気の予防法や、命を養い穏やかに効く滋養強壮薬の良さを追求してきました。
西洋でも16〜18世紀には錬金術師が不老不死の秘薬を盛んに作っていました。
近代医学においても、老化を抑える研究は極めて重要な位置を占めています。
老化というのは生命を脅かす多くの病気の最大のリスク要因だからです。
このような老化関連の疾患の患者数は今後20年間で2倍になるとWHOは推定しています。
老化過程を遅くできる薬や方法は、一般の人々のみならず、科学者や医療関係者も多くの興味を持っています。
「健康寿命や寿命を延長する」という効果が少なくとも3種類以上の種(線虫、ショウジョウバエ、マウス、サルなど)で確認され、少なくとも3カ所以上の研究グループで確認されているという基準を満たす抗加齢法として、断食、カロリー制限、運動、スペルミジン、メトホルミン、レスベラトロール、ラパマイシンなどが報告されています。
これらの分子メカニズムとして、遺伝子発現のエピジェネシス制御(ヒストンのアセチル化やメチル化)、インスリン/TOR経路、Rasシグナル伝達系、ミトコンドリア機能、たんぱく質恒常性、オートファジー、ストレス抵抗性などが指摘されています。
近代医学は、老化のメカニズムを明らかにし、抗加齢医療の実現を目指しています。
つまり、古代から続く不老不死の願いをかなえるために医学や医療を発展させているといっても過言ではないと言えます。
【若返りは可能か?】
私たちは加齢とともに体力や内臓の機能の衰えを自覚しますが、これは「老化現象だから仕方ない」とあきらめてしまいます。確かに「老化を止める」ことも「若返り」も生物学的には不可能です。
しかし、老化のスピードを緩めることは可能ですし、さらに、体の組織や臓器の働きを高めることによって、体力年齢を実年齢より若くすることはできます。
例えば、加齢とともに血管の動脈硬化が進み、脳や心臓など多くの臓器の働きが低下していきます。既に存在する動脈硬化の程度を低下させることができれば、体をより若い状態に戻すことができます。
そこで、動脈硬化の程度や血管の柔軟性を測定して「血管年齢」という指標で血管の若々しさを評価し、この血管年齢を低下させる治療法(キレート剤や抗酸化剤を使った治療など)がアンチエイジングの領域では実施されています。
血管年齢の若返りは、組織や臓器の機能低下を防ぎ、虚血性心疾患や脳梗塞や認知症の予防に効果があります。したがって、血管の動脈硬化を改善すれば体の若返りに役立つことは十分に納得できます。
しかし、内分泌系や免疫系の老化に伴う機能低下は、遺伝子によってプログラムされているため、血管を若くするだけでは改善できません。漢方薬に使われる生薬の中には、内分泌系や免疫系の働きや運動能力を高めるようなものが多く知られています。このような滋養強壮効果や生理機能を活性化する効果をもった生薬や薬草の利用は、抗老化に役立ちます。
がんは体の老化とともに発生率が高まります。したがって、老化予防はがん予防の究極の方法とも言えます。日頃から、体力や免疫力や血液循環を良い状態に維持することが、がん予防の基本になります。がんの発生を予防することは最大寿命を延ばす目的でも重要です。
漢方医学の神髄は「未病を治す」ことであり、「病気にさせない」ことです。その目的を達成するために「不老長寿」の考えが漢方医学の中核になっており、老化防止のための薬が多く用意されています。老化のメカニズムと漢方薬の効果を理解すると、漢方治療によって老化のスピードを遅くし、体を若返らせることが可能であることが納得できます。さらに、漢方薬による老化予防ががん予防にも役立つことが納得できます。
【抗加齢医療は脳と遺伝子の戦い】
私たちの体は不死の能力を持っています。
私たちの子供が、母親や父親と同じ年齢で生まれないという事実から判るように、私たちの配偶子(卵と精子)を継続的に生み出している生殖系幹細胞(germ line stem cells)の分子時計は常にゼロに保たれています。
親が30歳でも、子供は0歳で生まれます。
つまり、遺伝子にとって体は単なる乗り物(リチャード・ドーキンスの利己的遺伝子の考え方)であって、老化した体から若い子供に乗り移ることによって、遺伝子は不死を維持できます。
しかし、体が死ぬと困るのが脳です。脳にとって体は単なる乗り物ではなく、脳を存続させる生命維持装置のようなものです。医療を発展させて病気を治療するのは脳が存続したいためです。人工臓器や臓器移植することを考えるのは脳です。
そして脳は体の老化を阻止して不老長寿を達成したいと考えています。
医学や医療を発展させているのは脳であって、それは脳が死にたくないと考えているためです。体が死ぬと脳も死ぬからです。
体は遺伝子の乗り物であるというリチャード・ドーキンスの利己的遺伝子の考え方では、生殖年齢を超えた生き物は積極的に排除される方がその種の繁栄には有利です。
糖尿病や動脈硬化やがんや認知症や骨粗鬆症のような生活習慣病あるいは老化関連疾患と呼ばれる病気は生殖年齢を超えた50歳あたりから増えてきます。このような疾患が増えてきたのは、わずかここ100年にも満たない最近のことです。例えば、日本では昭和初期まで男女の平均寿命は50歳前後です。それが80年足らずの間に平均寿命は30年も延びています。この寿命の延びと並行して様々な老化関連疾患や生活習慣病が増えてきました。
さて、生存に不適当な疾病は、それが生殖年齢内に発症する場合は、個体が世代を重ねるごとにその疾病遺伝子は次第に人類の遺伝子プールから淘汰されていきます。その原因遺伝子が次の世代に移行しないからです。
しかし、生殖年齢を超えてから発症する老化関連疾患の場合は、その原因遺伝子は淘汰できません。すでにその原因遺伝子は次の世代(子供)に移行しているからです。
生殖年齢期間までには発症せず、生殖年齢を超えた後から発症してくるような致命的な疾患が遺伝的に存在すれば、そのような疾病遺伝子は淘汰されるどころか人類の遺伝子プールの中で広がることになります。
生殖年齢を超えた生き物は積極的に排除される方がその種(正確には遺伝子)の繁栄には有利に働くからです。
したがって、老化関連疾患の発症に関連する遺伝子の多くは、進化の過程で淘汰されることはなく、むしろ維持され広がることになります。つまり、老化関連疾患の発症率は上昇します。
遺伝子は「老化関連遺伝子を広めて老化した個体を早く排除したい」と思っています。一方、脳は「医学や医療を進歩させて老化を阻止しよう」と考えています。
老化は遺伝子によってプログラムされています。老化にプログラムが存在するということが、抗加齢治療が実現できる可能性を示唆しています。プログラムを変更できれば老化を阻止できるからです。そのプログラムの変更を脳は考えています。
抗加齢医療は遺伝子と脳の戦いになっています。老化を促進する遺伝子の企み(老化のメカニズム)を脳が気づき始めたため、脳が勝つ可能性が出て来ているというのが、最近の抗加齢医学の状況です。
しかし、死なない利己的な個体(脳)が増えると、人類という種(遺伝子)が無くなるリスクは増大します。
【老化抑制とがん抑制には共通点が多い】
分子標的薬の中にはがん細胞の増殖と同時に老化の進行を遅らせる作用をもったものがあります。その理由は、がん治療のターゲットになっているシグナル伝達系と老化に関連する因子に共通のものが多くあるからです。
老化の研究者はがん治療で開発された分子標的薬は抗老化治療の宝庫だと言っています。つまり、老化予防や寿命延長の効果を持ったがん治療が可能ということです。(例えば、mTORC1を抑制するラパマイシンやその誘導体など)
正常細胞に様々なダメージを与える通常の抗がん剤治療は老化や寿命に対してマイナスに作用しますが、老化や寿命に対してプラスの作用をもつ抗がん剤で治療すれば、それは理想のがん治療になります。
老化を遅らせ寿命を延ばす最も確実な方法はカロリー制限です。
カロリー制限とは、栄養障害を起こさずに食事からの摂取カロリーを30~40%程度減らす食事を行うことで、カロリー制限には老化を遅延して寿命を延ばし、老化関連疾患の発症を遅らせる効果が認められています。カロリー制限ががんの発生を抑制することも明らかになっています。
このカロリー制限による老化遅延や寿命延長やがん抑制のメカニズムには長寿遺伝子と言われるサーチュインなど様々な因子の関与が指摘されていますが、その因子の中に、インスリン、インスリン様成長因子-1(IGF-1)、PI3K/Aktシグナル伝達系、mTORC1(哺乳類ラパマイシン標的タンパク質複合体1)、AMP活性化プロテインキナーゼ(AMPK)、転写因子のFOXO(Forkhead box O)などがあります。そして、これらはがんの予防や治療における重要なターゲットになっています。
例えば、カロリー制限はATPの量を減らすことによってAMPKを活性化します。インスリン/IGF-1シグナル伝達系で活性化されるPI3K/Ak/mTORC1は老化を促進しがん細胞の増殖を促進します。AMPKはこのシグナル伝達系を抑制します。
ネズミに30~40%のカロリー制限を行うとIGF-1濃度が30~40%減少し、がんの発生率が低下し、寿命が延びるという結果が報告されています。
線虫の研究では、カロリーを制限しなくても、カロリー摂取で応答するインスリンの信号伝達系に欠陥がある変異体は普通にエサを食べていても長生きすることが明らかになっています。
細胞には古くなったタンパク質を分解してリサイクルするオートファジー(自食作用)というメカニズムがあります。飢餓状態になったときに、自分の細胞を分解して栄養源にするのが本来の目的ですが、細胞内の老化したタンパク質を除去する作用もあります。
一時的飢餓あるいは軽度の飢餓はオートファジー亢進を通じて細胞内をきれいにして、細胞を若返らせる効果があり、さらにがんを予防することもできます。オートファジーの抑制は細胞内に異常タンパク質や不良ミトコンドリアが蓄積することが引き金になって細胞のがん化が促進されるからです。
カロリー制限は完全な絶食ではなく、普通の食事の60〜70%程度のカロリーに抑えるのですが、この程度の弱い飢餓でもオートファジーが誘導されます。
インスリンやインスリン様成長因子-1(IGF-1)によって活性化されるmTORC1はオートファジーを抑制することによって細胞の老化とがん化を促進する作用が指摘されています。
FOXOは「Forkhead box O」の略で、DNA結合ドメインFOX(Forkhead box)をもつForkheadファミリーのサブグループ“O”に属する転写因子で、栄養飢餓時に活性化されます。
FOXOはインスリン-PI3K-AKTシグナルによって負に制御されています。つまり、PI3K-AKTシグナルが活性化されるとAKTによって直接的にリン酸化され、FOXOの核外移行を促進することでその転写活性は抑制されます。
一方、栄養飢餓状態ではPI3K-AKTの不活性化に伴いFOXOの活性化が誘導されることになります。つまり、カロリー制限による寿命延長や抗がん作用に関与する転写因子として重要な役割を担っています(下図)。

図:様々な増殖刺激によってPI3k/Aktシグナル伝達系が活性化されるとFOXO(Forkhead box O)という転写因子の活性が抑制される。FOXO転写因子が活性化されると酸化ストレスが軽減し、細胞老化が抑制される。Aktの活性化はmTORC1を活性化して細胞の老化やがん化やがん細胞の増殖を促進する。したがって、PI3k/Aktシグナル伝達系を抑制すると、FOXO転写因子の活性化とmTORC1の抑制の2つの機序で寿命延長とがん抑制の効果が得られることになる。
以上のように、インスリン/IGF-1シグナル伝達系で活性化されるPI3K/Ak/mTORC1の抑制、AMPKの活性化、FOXOの活性化は、がん細胞の発生や増殖を抑制する作用があり、しかも老化を抑制し寿命を延ばす作用があります。
したがって、これらをターゲットにしたがん治療は副作用のない理想的ながん治療法なり得ると言えます。
がん治療で開発された分子標的薬が抗老化治療薬の候補として研究されています。
がんの場合は、そのシグナル伝達系に次々に変異や異常が発生してくるので、治療に抵抗性になってくる可能性があります。
しかし老化予防の目的ではそのような耐性はできないので、これらのがん治療薬をそのまま抗老化薬に使用すると有効性が維持できるというメリットがあると考えられています。
このような薬を低用量で服用すると老化を遅延させ寿命を延ばせると考えられています。薬による寿命延長は線虫やショウジョウバエやマウスなどでは実証されています。霊長類ではカロリー制限による老化遅延と寿命延長は実証されていますが、薬での実験はまだ結果は出ていません。
老化予防は究極のがん予防法と言われています。つまり、がんは老化性疾患の一つであり、老化の過程を抑制することはがんの発生を予防することになります。このような薬ががん予防薬(循環器疾患の予防や寿命延長にも効果がある)として期待されています。
そのような目的で、糖尿病治療薬のメトホルミンを老化予防効果と寿命延長効果を期待して服用している人は多くいます。DNAの構造の解明でノーベル賞を受賞したジェームズ・ワトソンも抗老化の目的でメトホルミンを服用しているとある講演で言っています。(356話参照)
がんと老化の両方に関与しているシグナル伝達系や因子をターゲットにすれば、「寿命を延ばすがん治療」が実践できます。
参考:The search for anti-aging interventions: From elixirs to fasting regimens(抗老化法の探索:不老不死の霊薬から断食療法まで)Cell. 2014 Jun 19; 157(7): 1515–1526.
| « 535)ビタミンD... | 537)超高齢者... » |



