がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
360) 転写因子Nrf2を阻害するとがん細胞は死にやすくなる
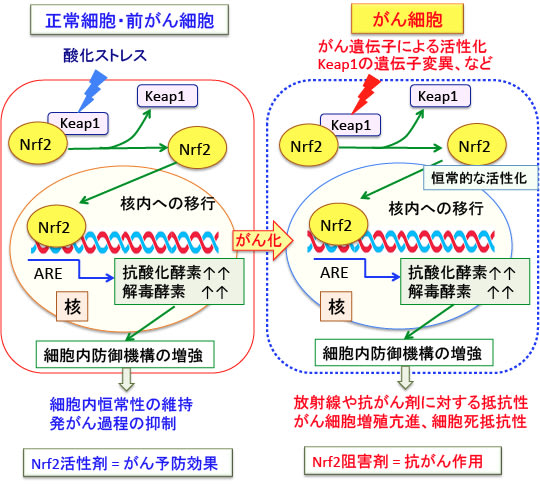
図:Keap1-Nrf2システムは酸化ストレスや有害物質に対する防御機構において重要な役割を担っている。転写因子のNrf2は細胞質でKeap1によって分解が促進されることによって活性が抑制されている。正常細胞では酸化ストレスが加わると、Keap1の構造が変化してNrf2から離れ、フリーになったNrf2が核内に移行して、抗酸化酵素や解毒酵素の遺伝子の上流に存在する抗酸化剤応答配列ARE(antioxidant response element)に結合して、これらの遺伝子の発現を亢進する。その結果、正常細胞では活性酸素や発がん物質を解毒することになるので、Nrf2の活性を促進するもの(=Nrf2活性剤)はがん予防効果がある。
一方、がん細胞においては、KRasやcMycなどのがん遺伝子の活性化やKeap1の遺伝子変異などによってNrf2は恒常的に活性化しており、抗酸化酵素や解毒酵素の産生や活性が亢進している。そのため、がん細胞は酸化ストレスや細胞傷害性物質に対する抵抗性が亢進しており、これが抗がん剤や放散線治療に対する抵抗性の原因になっている。したがって、がん細胞においては、Nrf2の活性を阻害するもの(=Nrf2阻害剤)ががん治療に役立つ。このように、正常細胞(前がん細胞も含む)とがん細胞とではNrf2に対する対応は全く異なる。
360)転写因子Nrf2を阻害するとがん細胞は死にやすくなる
【細胞内防御システムを利用してがん細胞は強くなる】
人間の社会に例えれば「国民を守るべき警察や軍隊がギャングやテロ集団を守る」ような出来事が、がん細胞の社会では日常的に起こっています。
細胞には、活性酸素や有毒物質による害から細胞自身を守る手段や仕組みが備わっています。
例えば、炎症などによって活性酸素の発生量が増えると、細胞は活性酸素を消去する酵素(スーパーオキシド・ディスムターゼ、カタラーゼ、グルタチオン・ペルオキシダーゼなど)の発現や活性を高めたり、フリーラジカルを消去するグルタチオンなどの抗酸化物質の合成を高めたりして、活性酸素の害(酸化ストレス)を軽減しようとします。
また、グルタチオンSトランスフェラーゼ(GST)などのフェースII(第2相) 解毒酵素と言われる代謝酵素は、様々な発がん物質や有害物質を無毒化する作用があります。
細胞が活性酸素や発がん物質や有害な成分(抗がん剤や放射線も含む)によって攻撃を受けると、これらの活性酸素消去酵素やグルタチオンやフェースII解毒酵素が細胞内に誘導され(遺伝子発現が増えたり産生量が増える)、細胞を守るシステムが働きます。
このような細胞内の防御システムの活性化に中心的な働きを行っているのがNrf2(Nuclear Respiratory Factor 2)という転写因子です。
転写因子というのは特定の遺伝子の発現(DNAの情報を蛋白質に変換すること)を調節している蛋白質です。抗酸化酵素やグルタチオンの産生に関する酵素やフェース2解毒酵素の遺伝子の発現調節領域には、抗酸化反応エレメント(antioxidant response element:ARE)という領域があって、この部分にNrf2が結合するとこれらの遺伝子の転写が促進されるのです。
ホルミシス(hormisis)効果というものがあります。体に有害と思われている放射線や活性酸素やある種の発がん物質も、微量であれば体を刺激する方向で働いて、これらの害に対する抵抗力が高まるという効果です。刺激やストレスがくり返されると、生体はそれらに対して適応するように体が反応するため、その刺激やストレスに対して抵抗性になると考えられるのですが、抗酸化力や解毒力の増強のメカニズムに関しては転写因子のNrf2の活性化が関与しています。
化学発がん物質の研究でもホルミシス効果が認められています。体内で活性酸素を発生させて発がん作用を示すような物質を、少量だけ投与すると、かえって発がんが抑えられることがあります。これは、軽度の酸化ストレスに対して、適応反応として体の中の抗酸化酵素が増加するためであると考えられています。この場合も、Nrf2の活性化が重要な役割を担っています.
さて、このNrf2は様々なストレスや有害物質から細胞を守っているので、細胞にとっては「正義の味方」や「市民を守る警察や軍隊」のような存在です。
しかし、最近の研究によると、がん細胞ではNrf2の活性が非常に高くなっており、しかもNrf2の活性が高いがん細胞ほど治療に抵抗性で予後が悪いという結果が得られています。
つまり、がん細胞は、抗がん剤や放射線治療から自分を守るためにNrf2を利用しているということです。
Nrf2にとっては、それが存在する細胞が正常細胞であろうががん細胞であろうが、その細胞に忠誠を尽くして働いているだけなので、Nrf2に罪は無いわけです。ただ、Nrf2は細胞を守る兵士のようなものなので、がん細胞内に強い兵士が多数増えていると、抗がん剤や放射線で攻撃しても死ににくくなります。
がん細胞におけるNrf2の働きを阻害することができれば、抗がん剤や放射線治療の効き目を高めることができます。まだ培養細胞や動物実験の段階ですが、抗がん剤治療や放射線治療にNrf2阻害剤を併用すると抗腫瘍効果が高まることが報告されています。
【がん予防に有効なものががん治療を妨げる場合もある?】
抗酸化作用や解毒力のような細胞に備わった防御システムを活性化する薬や治療法があれば、がんの予防に役立ちます。
そのような薬の開発のターゲットになっているのがNrf2です。細胞のNrf2を活性化すれば、抗酸化酵素や解毒酵素やグルタチオンが増え、活性酸素や発がん物質によって引き起こされるがんを防ぐことができます。
ブロッコリーなどのアブラナ科植物に含まれるスルフォラファン (sulforaphane)は抗酸化酵素やフェースII解毒酵素の活性を高めて、強いがん予防効果を発揮することが知られています。そして、スルフォラファンは転写因子のNrf2を活性化することによって、このような作用を示すことが明らかになっています。
スルフォラファンがNrf2を活性化するメカニズムは十分には解明されていませんが、mitogen-activated protein kinases (MAPK)の活性化を介する機序や、Nrf2を直接的に活性化する機序など複数のメカニズムが報告されています。
いずれにしても、スルフォラファンは多くの実験でNrf2活性化のpositive controlの試薬としても使われくらい、Nrf2活性剤として作用は確立されています。
さて、細胞の発がん過程を抑える目的ではNrf2の活性化はメリットがあるのですが、一人前のがん細胞になった段階では、Nrf2の活性化は逆効果になる可能性があります。
つまり、がん細胞がある状態でスルフォアファンを多く服用すると、がん細胞のNrf2の活性が亢進して、がん細胞が抗がん剤や放射線治療に抵抗性を強める可能性があるからです。
本当にスルフォラファンがヒトのがんの治療を妨げるという証拠があるわけではなく、まだ可能性の段階です。
「がん細胞では、がん遺伝子の作用やKeap1の構造異常などによってNrf2が恒常的に活性化しているので、スルフォラファンでさらに活性が高まることはなく、逆に、正常細胞のNrf2活性を誘導すると、抗がん剤や放射線治療の副作用を軽減できるので、がん治療中にスルフォラファンを摂取するメリットの方が高い」という可能性はまだ否定できません。
しかし、最近のがん研究領域では、「がんの治療効果を高めるためにがん細胞のNrf2活性を阻害することが重要である」という認識が強まっています。
357話で紹介したジェームズ・ワトソンの論文でも、がん細胞が抗がん剤や放射線治療に抵抗性を示すのはがん細胞では活性酸素種を消去する抗酸化物質の量が極めて多いからであり、多くの抗酸化性物質の合成を調節している転写因子のNrf2の活性を阻害する治療法の有効性を示唆しています。
ブロッコリーの新芽(スプラウト)には、成長したブロッコリーの10- 100倍近いスルフォラファンが含まれており、強いがん予防効果が期待できる食材して知られています。しかし、進行がんの状態や、抗がん剤治療中や放射線治療中は食べない方がよいのかもしれません。ただし、この意見には前述のような反論もあります。
いずれにしても、「がんの予防や治療のターゲットとしての転写因子Nrf2には二面性があり、発生予防の段階とがん治療の段階では全く異なる対処が必要」という注意点は頭に入れておく必要があります。
つまり、「がんの発生予防に有効なものががん治療中にも効果があるとは限らない」「むしろ、逆の効果になる可能性もあるかもしれない」という点です。
漢方治療も、がんの発生や再発の予防とがん治療中では処方が異なるべきです。
発生予防や再発予防の目的であれば、抗酸化作用のある成分や、グルタチオンの産生増加やNrf2の活性化の作用がある成分を含む生薬を主体にした処方はがんの発生や再発を予防する効果を高めると思われます。
しかし、抗がん剤治療や放射線治療を行っている時は、逆に、Nrf2活性を阻害する成分の利用を主体に考える必要があります。
食事も同じです。スルフォラファンによる抗酸化力や解毒力を高める目的で、ブロッコリー(特にブロッコリースプラウト)やその他のアブラナ科野菜を推奨する意見もありますが、再発予防の段階ならメリットがあるかもしれませんが、がん治療中は本当に効果があるのか(少なくとも抗がん剤や放射線治療の効き目を高めるという目的では)怪しい気がします。
【Nrf2の活性化は発がん過程を抑制する】
転写因子Nrf2(Nuclear respiratory factor 2)は、抗酸化機能や解毒機能を持つ様々な遺伝子の転写を誘導します。
活性酸素種や食物に含まれる親電子性物質によりもたらされる酸化ストレスは,DNAやタンパク質や脂質などの生体高分子を酸化することで傷害を与え、がんや糖尿病や腎臓疾患や神経変性疾患など様々な疾患を引き起こす原因になります。
このような酸化ストレスに対する防御機構において重要な機能を担っているのが、Keap1-Nrf2システムです.
正常細胞において酸化ストレスの無い状況では、Nrf2はKeap1(Kelch-like ECH-associated protein 1)というタンパク質に結合することによりユビキチン化を受け、分解しています。
しかし、酸化ストレスにさらされるとKeap1のシステイン残基が修飾を受けて構造が変化し、Keap1からNrf2が離れて核へ移行し、遺伝子上流に存在する抗酸化剤応答配列ARE(antioxidant response element)に結合することによって、このARE配列をもつ様々な遺伝子(抗酸化酵素やグルタチオンの合成に関与する酵素やフェースII解毒酵素など)の発現を誘導し、抗酸化や解毒に関するタンパク質や因子の合成を高めます。
このような作用によって、正常細胞や前がん細胞においては、Nrf2の活性を亢進するNrf2活性剤は発がん過程を抑制するので、がん予防物質として認識されています。(トップの図の左側)
このようなNrf2の活性化を介したがん予防物質としてスルフォラファンやクルクミンやレスベラトロールなどが報告されています。
【Nrf2の活性化を阻害するとがん細胞は死にやすくなる】
ヒトの肺がんなど多くの固形腫瘍でNrf2機能の異常亢進が見つかっています。そして、Nrf2の活性が高いと治療に抵抗性で予後が不良であることが報告されています。
Nrf2は解毒酵素、抗酸化タンパク質、薬剤排出トランスポーターなどの遺伝子を統括的に活性化することにより、がん細胞の抗がん剤耐性と放射線耐性をもたらします。
さらに、Nfr2はグルコースやグルタミンの代謝を変化させて細胞増殖に有利な同化反応を促進します。
Nrf2はがん細胞のペントースリン酸経路を活性化して、核酸とNADPHの産生を増やすことで細胞増殖を亢進します。NADPHはグルタチオンの合成にも必要です。
多くのがん細胞では、酸化ストレスの有無とは関係なくNrf2の発現量と活性が亢進しています。その理由は、RASやMYCなどのがん遺伝子がNrf2を活性化しているからです。Nrf2の活性を抑制するKeap1の遺伝子変異によってNrf2が活性化する場合も見つかっています。
恒常的に安定化したNrf2は酸化ストレスや抗がん剤/放射線治療に対する抵抗性を増強し、さらに積極的に細胞増殖を促進することになります。
抗がん剤治療や放射線治療によって活性酸素が増えると、がん細胞はさらにNrf2の量を増やして抵抗性を獲得してきます。
このようにNrf2の活性化はがん細胞が治療に対する抵抗性を獲得するメカニズムとして重要です。したがって、がん細胞のおけるNrf2の機能阻害は、抗がん剤治療の有効な戦略となります。(トップの図の左側)
糖尿病性腎症や慢性閉塞性肺疾患など多くの酸化ストレスと関連する疾患の予防や治療のためにNrf2の活性化剤が臨床応用に向けて開発されています。
一方、がんの治療になるとNrf2の阻害剤が有益になる可能性が高いと考えられています。
がん細胞のNrf2を阻害すると、
①がん細胞内での活性酸素種の蓄積によってアポトーシス(細胞死)が誘導できる。
②抗がん剤治療や放射線治療の効き目を高めることができる。
③がん細胞での物質合成(同化反応)を阻害することによって増殖を阻害できる。
などの効果が期待できます。
ただし、全身投与の場合は、がん組織以外の正常組織での酸化ストレス応答を減弱させる欠点もあります。つまり、がん細胞特異的にNrf2を阻害できる方法があれば、がん治療に役立ちます。
【がん細胞特異的にNrf2活性を阻害する方法】
Nrf2の転写活性を介した抗酸化酵素や解毒酵素の発現にはグルコースの供給が必要であるという報告があります。
Glucose availability is a decisive factor for Nrf2-mediated gene expression.(グルコースの供給がNrf2を介した遺伝子発現のための決定的な要因である)Redox Biol. 2013 Jun 21;1(1):359-65.
この論文では、スルフォラファンでNrf2を活性化する方法や、Nrf2を阻害するKeap1遺伝子を機能欠損させる方法(遺伝子ノックアウト)でNrf2の活性を亢進する方法で実験しています。
Nrf2を活性化するとグルコースの取込みが増え、ペントースリン酸経路でのNADPHの産生が増えることが示されています。
そして、グルコースの供給や取込みを阻害するか、あるいはペントースリン酸経路を阻害してNADPHの産生を阻害すると、Nrf2を介した遺伝子発現が抑制され、抗酸化酵素や解毒酵素の発現が抑制されることが示されています。
つまり、糖質制限やケトン食や2−デオキシグルコースなどで、がん細胞におけるグルコースの取込みやペントースリン酸経路を抑制する方法は、グルコースの取込みが亢進しているがん細胞に選択的にNrf2の活性を阻害できる可能性があります。
ケトン食と2-デオキシグルコースと抗がん剤/放射線治療の相乗効果については337話、338話、341話、346話などで解説していますが、ケトン食と2-デオキシグルコース、およびその他のグルコース代謝を阻害する方法は、がん細胞におけるNrf2の活性抑制に有効だと言えます。(その他の方法については353話、355話参照)
メトホルミンがNrf2活性を抑制するという報告があります。
Metformin inhibits heme oxygenase-1 expression in cancer cells through inactivation of Raf-ERK-Nrf2 signaling and AMPK-independent pathways.(メトホルミンはRaf-ERK-Nrf2 シグナル伝達系とAMPK非依存的経路の阻害によってがん細胞のヘムオキシゲナーゼ-1を阻害する)Toxicol Appl Pharmacol. 2013 Sep 1;271(2):229-38.
ヘムオキシゲナーゼ-1は、ヘム(heme)をビリベルジン(biriverdin)と一酸化炭素(CO)と遊離鉄(Fe)に分解する酵素です。ビリベルジン(緑色の色素)は、ビリベルジン・リダクターゼ(biriverdin reductase)により、ビリルビン(bilirubin:黄疸の時の黄色の色素)に分解されます。このヘム分解により産生れるビリベルジンとビリルビンには強力な抗酸化作用があり、酸化ストレスによる細胞傷害を抑制します。
メトホルミンはRaf-ERKシグナル伝達系を抑制しNrf2の発現量を減らす効果があることを報告しています。
メトホルミンとケトン食と2-デオキシグルコースの組合せは抗腫瘍効果において相乗効果がありますが、Nrf2活性の抑制においても相乗効果が期待できそうです。(338話参照)
また、黄芩(おうごん)という生薬に含まれるクリシン(chrysin)というフラボノイドがNrf2活性を抑制するという報告があります。
Chrysin enhances sensitivity of BEL-7402/ADM cells to doxorubicin by suppressing PI3K/Akt/Nrf2 and ERK/Nrf2 pathway.(クリシンはPI3K/Akt/Nrf2 と ERK/Nrf2 経路を抑制することによってBEL-7402/ADM細胞のドキソルビシンに対する感受性を高める)Chem Biol Interact. 2013 Oct 25;206(1):100-8
この論文では、クリシンが増殖シグナル伝達系のPI3K-Aktと ERK経路を抑制することによってNrf2のmRNAとタンパク質の発現量を顕著に減少させ、抗がん剤に対する感受性(効き目)を高めることが報告されています。
クリシンにはグルタチオン濃度を低下させて抗がん剤の効き目を高める効果も報告されています。
Chrysin enhances doxorubicin-induced cytotoxicity in human lung epithelial cancer cell lines: the role of glutathione.(Chrysinはヒト肺がん細胞株におけるドキソルビシンによる細胞毒性を増強する:グルタチオンの役割)Toxicol Appl Pharmacol. 258(1):1-9.2012年
Chrysinがグルタチオンの細胞内からの排出を誘導してグルタチオン濃度を低下させて抗がん剤感受性を高める機序が報告されています。この論文では、4種類のヒト肺がん細胞株を用いた実験で、chrysinがドキソルビシンの殺細胞効果を増強することが報告されています。
黄芩は抗炎症作用や様々な抗がん作用が報告され、がんの漢方治療においても使用頻度が高く、その抗腫瘍作用は経験的に知られています。その抗がん成分としてバイカリン、バイカレイン、オーゴニンなどが知られていますが、クリシンの効果もあるのかもしれません。
(クリシンは米国などではサプリメントとしても販売されていますが、ヒトに対する効果に関しては証明されているわけではありません)
以上のことから、ケトン食+2−デオキシグルコース+メトホルミンの組合せや、その他のグルコース代謝(解糖系やペントースリン酸経路)を阻害する治療法と、ジクロロ酢酸ナトリウムやアルテスネイトやスルファサラジンなどがん細胞に酸化ストレスを高める方法(352話参照)を併用すると相乗効果が期待できそうです。
そして、このような方法でがん治療を行うときは、スルフォラファンを多く含むブロッコリースプラウトは避けた方が良いかもしれません。
| « 359)胃酸分泌... | 361) 膠芽腫に... » |





