がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
858)アブラナ科野菜の抗がん作用を強める調理法:40℃スープ
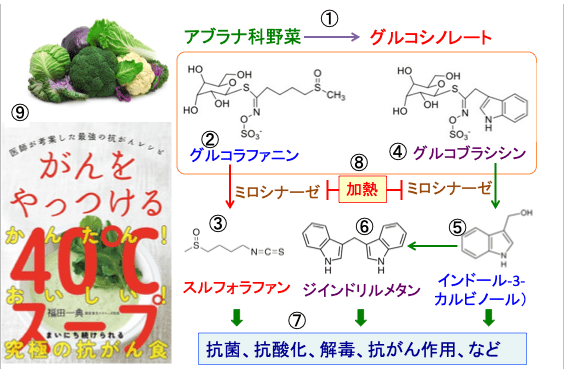
図:ブロッコリーやカリフラワーやキャベツなどのアブラナ科野菜にはグルコシノレートというイオウを含みグルコース(ブドウ糖)が結合した物質が含まれている(①)。グルコシノレートには複数の種類があり、そのうちのグルコラファニン(②)は、野菜の細胞が壊れるとミロシナーゼという酵素と反応してスルフォラファンを生成する(③)。別のグルコシノレートのグルコブラシシン(④)も、同様にミロシナーゼによって加水分解してインドール-3-カルビノールになり(⑤)、さらに胃の中の酸性の条件下では、インドール-3-カルビノールが2個重合したジインドリルメタンになる(⑥)。これらの物質は、抗菌、抗酸化、解毒、発がん抑制、がん細胞の増殖・浸潤・転移の抑制などの作用を持っており、がんの発生予防や治療に役立つ効果を発揮する(⑦)。酵素のミロシナーゼは熱で活性がなくなるので、加熱調理はミロシナーゼの働きを阻害してスルフォラファンなどの抗がん物質の産生を低下する(⑧)。40℃スープはミロシナーゼ活性を利用して抗がん作用を強める調理法として考案した。
858)アブラナ科野菜の抗がん作用を強める調理法:40℃スープ
【野菜はがん予防成分の宝庫】
がんの発生や再発を促進する要因としては、糖質や動物性脂肪や赤味の肉の取り過ぎ、喫煙、飲酒、運動不足や肥満が上げられます。
一方、野菜や果物や豆類など植物性食品、精製度の低い穀物、魚油や紫蘇油や亜麻仁油に多く含まれるω3不飽和脂肪酸は、がんの発生や再発を予防する効果が指摘されています。特に、野菜や豆類には、免疫力を高める成分、活性酸素やフリーラジカルの害を防ぐ成分、発がん物質を不活性化する成分、がん細胞の増殖を抑える効果をもつ成分などが多く見つかっており、これらの成分を多く摂取することががんの発生予防に寄与すると考えられています。
植物には、「免疫増強作用」「抗炎症作用」「抗酸化作用」「解毒作用」「がん細胞増殖抑制作用」などのがん予防に役立つ成分が多く含まれています。植物に含まれるこのような薬効成分をファイト・ケミカル(phyto-chemical)と呼んでいます。Phytoは植物、chhemicalは化学を意味する言葉で、したがって、ファイトケミカルとは植物に含まれる化学成分を意味しています。
これらのファイトケミカルから、がん予防効果をもった成分が多くみつかっており、それらはサプリメントとしても利用されるようになっています。例えば、大豆のイソフラボン、ゴマのリグナン、トマトのリコピン、ブロッコリーのスルフォラファン、お茶のカテキン、緑黄色野菜のカロテノイド、ブルーベリーのアントシアニン、赤ワインのポリフェノール、キノコのβグルカンなどが有名です。
【アブラナ科野菜は最強の抗がん食品】
1990年代に米国立がん研究所が中心となって「がん予防に重要な野菜や果物や香辛料」がまとめられました。そのトップはニンニクで、キャベツ、大豆、生姜、タマネギ、お茶などが上位にランクされています。キャベツはアブラナ科の野菜です。他のアブラナ科野菜のブロッコリー、カリフラワー、芽キャベツは、タマネギやお茶や柑橘類(オレンジ、レモン、グレープフルーツ)と同じランクになっています(下図)。

図:1990年から米国国立癌研究所を中心に行なわれた「デザイナーズフーズ・プログラム」における研究から得られた結果に基づく「がん予防効果が期待される野菜や果物」。アブラナ科野菜のキャベツ、ブロッコリー、カリフラワー、芽キャベツはがん予防に有効な野菜として上位にランクされている。
食事からのアブラナ科野菜の摂取量が多いほど、がんの発生率が低いことが、多くの疫学研究で明らかになっています。多くの報告をまとめると、アブラナ科野菜の摂取が少ない人に比べて摂取量の多い人のがん発症のリスクは50%から70%くらいに低下することが報告されています。
特に、生のアブラナ科野菜の摂取が多いほどがんの発生率が低下することが明らかになっています。それは、アブラナ科野菜は加熱調理すると抗がん成分が減少するからです。
【アブラナ科野菜は解毒力や抗酸化力を高める】
アブラナ(油菜)は「菜の花」とも呼ばれていて、3ー5月に黄色の十字架状の花が密集して咲く背丈が1ー2mの植物です。種には油が多くふくまれていて植物油の原料として栽培されていましたが、近年、野菜としてスーパーでも売られるようになりました。
アブラナと同じ仲間(アブラナ科)で野菜として食用されているものに、キャベツ、ブロッコリー、ケール、カリフラワー、芽キャベツ、ダイコン、ハクサイ、カブ、コマツナ、チンゲンサイ、ワサビなどがあります。茎の上部にある葉の基部の葉肉が張り出して耳状になり、茎を抱くのが特徴です。

図:いろいろなアブラナ科野菜
薬物や発がん物質などが体内に摂取されると、肝臓などの細胞内にある酵素の働きによって解毒されて体外に排泄されます。このような解毒酵素は大きくフェース1酵素群(phase 1 enzymes)とフェース2酵素群(phase 2 enzymes)に分類されています。
フェース1酵素(第1相酵素)は物質を酸化したり加水分解して物質を変換し、フェース2酵素(第2相酵素)は抱合反応などによって解毒する作用をもっています。このような薬物代謝酵素は多くの場合薬物の作用の消失を導くことから、解毒反応と呼ばれていますが、フェース1酵素群は場合によっては、発がん物質の前駆体を活性化し、発がん性を持たせるように働くこともあります。
一方、グルタチオン・S・トランスフェラーゼ(glutathione S-transferases)、 キノン還元酵素(quinone reductases)などのフェース2酵素は、DNAの変異を起こす発がん物質を不活化する作用を持っているので、フェース2酵素の量を増やす作用の食品や薬物のがん予防効果が注目されています。
アブラナ科の野菜にはがん予防効果が報告されていますが、その最も大きな理由は、アブラナ科の野菜に多く含まれているイソチオシアン酸塩成分にフェース2酵素の量を増やす作用があるからです。イソチオシアン酸塩はアブラナ科野菜に含まれる辛味成分です。
ジョンズ・ホプキンス大学のポール・タラレー博士らは、ブロッコリーに含まれるスルフォラファン(Sulforaphane)というイソチオシアン酸塩成分がフェース2酵素の合成を誘導する効果が強く、がん予防に効果があることを1994年に発見しました。その後も多くの研究でアブラナ科野菜に含まれるイソチオシアン酸塩成分のがん予防効果が確認され、そのメカニズムの研究が行われています。
【アブラナ科野菜は生で食べる方ががん予防効果が強い】
食事からのアブラナ科野菜の摂取量が多いほど、がんの発生率が低いことが、多くの疫学研究で明らかになっています。多くの報告をまとめると、アブラナ科野菜の摂取が少ない人に比べて摂取量の多い人のがん発症のリスクは50%から70%くらいに低下することが報告されています。
特に、生のアブラナ科野菜の摂取が多いほどがんの発生率が低下することが明らかになっています。それは、アブラナ科野菜は加熱調理すると抗がん成分が減少するからです。
アブラナ科の植物にはグルコシノレートという物質を含むのが特徴です。グルコシノレートは二次代謝産物の一種で、分子中にイオウ(硫黄)原子を多く含み、グルコースが結合しています。グルコシノレートにはグルコース以外の部分の構造が異なる多数の種類が知られています。
このグルコシノレートはミロシナーゼという酵素によって分解され、イソチオシアネートという非常に辛い物質に変化します。グルコシノレートは細胞内ではミロシナーゼと接触しないように安定して蓄えられていますが、昆虫などの捕食者にかじられると、細胞が壊れてグルコシノレートとミロシナーゼが接触して酵素反応が起こり、イソチオシアネートが生成するのです。
つまり、イソチオシアネートはアブラナ科植物が昆虫などの捕食者から身を守る防御物質なのです。ワサビや大根を擂り下ろすと辛みが出てくるのは、イソチオシアネートが生成するためです。

図:グルコシノレート(①)は分子中にイオウ(硫黄)原子を多く含み、グルコースが結合している。グルコシノレートは植物内でミロシナーゼ(②)と接触しないように安定して蓄えられているが、昆虫などの捕食者にかじられると、細胞が壊れてグルコシノレートとミロシナーゼが接触して酵素反応が起こり、イソチオシアネート(③)が生成する。
がん予防物質として有名なスルフォラファンは、グルコシノレートの一種のグルコラファニン(glucoraphanin)という物質がミロシナーゼによって分解されて生成します。つまり、スルフォラファンはイソチオシアネートの一種です。細胞が壊れてグルコシノレートとミロシナーゼが反応して生成するイソチオシアネートは昆虫などの捕食者を忌避させる効果を発揮します。
グルコラファニンはブロッコリーやカリフラワーやキャベツに多く含まれています。
スルフォラファンは抗酸化酵素やフェース2解毒酵素の活性を高めて、強いがん予防効果を発揮することが知られています。

図:グルコシノレートの一種のグルコラファニンがミロシナーゼで分解されるとスルフォラファンというイソチオシアネートが生成する。
別のグルコシノレートのグルコブラシシンも、同様にミロシナーゼによって加水分解してインドール-3-カルビノールになります。このインドール-3-カルビノールも植物の生体防御に働きますが、人間が摂取すると、胃の中の酸性の条件下では、インドール-3-カルビノールが2個重合したジインドリルメタンになります(図)。
ジインドリルメタンはがん細胞のシグナル伝達系に作用して、増殖や浸潤や転移を抑制し、細胞死(アポトーシス)を誘導し、抗がん剤感受性を高めるなどの抗がん作用を発揮します。

図:アブラナ科野菜に多く含まれるグルコシノレートの一種のグルコブラシシン(①)は、ミロシナーゼ(②)によって加水分解してインドール-3-カルビノール(③)になる。さらに胃の中の酸性の条件下では、インドール-3-カルビノールが2個重合し(④)、ジインドリルメタン(⑤)になる。
アブラナ科の植物に見られるグルコシノレートとミロシナーゼのシステムは、最もよく研究されている植物の化学的防御の1つです。
ミロシナーゼ(myrosinase)はβ-チオグルコシダーゼとも呼ばれ、グルコシノレートのグリコシド結合を加水分解して、硫酸基を離脱させることでイソチオシアネートを生成します。
グルコシノレートとその加水分解酵素であるミロシナーゼは、無傷の植物組織の別々の区画に保管されています。組織が破壊されると、グルコシノレートの生物活性化が開始されます。
つまり、ミロシナーゼはそのグルコシノレート基質にアクセスし、グルコシノレートの加水分解により、毒性のあるイソチオシアネートおよび他の生物学的に活性な生成物が形成されます。グルコシノレート-ミロシナーゼ系の防御機能は、さまざまな昆虫や草食動物を用いた多くの研究で実証されています。
このグルコシノレートとミロシナーゼによって生成されるスルフォラファンやインドール-3-カルビノールとその代謝産物が、アブラナ科野菜の抗がん作用のメカニズムになっています。

図:ブロッコリーやカリフラワーやキャベツなどのアブラナ科野菜にはグルコシノレートというイオウを含みグルコースが結合した物質が含まれている(①)。グルコシノレートには複数の種類があり、そのうちのグルコラファニン(②)は、野菜の細胞が壊れるとミロシナーゼという酵素と反応してスルフォラファンを生成する(③)。別のグルコシノレートのグルコブラシシン(④)も、同様にミロシナーゼによって加水分解してインドール-3-カルビノールになり(⑤)、さらに胃の中の酸性の条件下では、インドール-3-カルビノールが2個重合したジインドリルメタンになる(⑥)。これらの物質は、抗菌、抗酸化、解毒、発がん抑制、がん細胞の増殖・浸潤・転移の抑制などの作用を持っており、がんの発生予防や治療に役立つ効果を発揮する(⑦)。
【スルフォラファンは転写因子のNrf2を増やす】
体内に毒が入ってくると、体を守るために、それらの毒を解毒する必要があります。
通常、薬物や発がん物質などが体内に摂取されると、肝臓などの細胞内にある酵素の働きによって解毒されて体外に排泄されます。このような解毒酵素は大きくフェース1酵素群(phase 1 enzymes)とフェース2酵素群(phase 2 enzymes)に分類されています。
フェース1酵素(第1相解毒酵素)は物質を酸化したり加水分解して物質を変換します。フェース2酵素(第2相解毒酵素)は抱合反応などによって解毒する作用を持っています。このような薬物代謝酵素は多くの場合薬物の作用の消失を導くことから、解毒反応と呼ばれています。
フェース2酵素は、DNAの変異を起こす発がん物質を不活化する作用を持っているので、フェース2酵素の量を増やす作用がある食品や薬物はがんを予防する効果があります。
フェース2解毒酵素の遺伝子の発現調節領域には、抗酸化反応エレメントという領域があって、Nrf2という転写因子が結合するとフェース2解毒酵素の発現が誘導されます。
イソチオシアネートなどのフェノール性抗酸化剤はmitogen-activated protein kinases (MAPK)を活性化して、転写因子のNrf2が細胞核内に蓄積し、遺伝子の抗酸化反応エレメントへの結合を促進して、抗酸化に働く種々の遺伝子の発現を誘導して酸化ストレスを軽減させる作用があります。転写因子のNrf2は、抗酸化機能や解毒機能を持つ様々な遺伝子の転写を誘導します。
活性酸素種の産生によりもたらされる酸化ストレスは,DNAやタンパク質や脂質などの生体高分子を酸化することで細胞や組織に傷害を与え、がんや糖尿病や腎臓疾患や神経変性疾患など様々な疾患を引き起こす原因になります。
このような酸化ストレスに対する防御機構において重要な機能を担っているのが、Keap1-Nrf2システムです.
正常細胞において酸化ストレスの無い状況では、Nrf2はKeap1(Kelch-like ECH-associated protein 1)というタンパク質に結合することによりユビキチン化を受け、分解しています。
しかし、酸化ストレスにさらされるとKeap1のシステイン残基が修飾を受けて構造が変化し、Keap1からNrf2が離れて核へ移行し、遺伝子上流に存在する抗酸化剤応答配列(antioxidant response element: ARE)に結合することによって、このARE配列をもつ様々な遺伝子(抗酸化酵素やグルタチオンの合成に関与する酵素やフェースII解毒酵素など)の発現を誘導し、抗酸化や解毒に関するタンパク質や因子の合成を高めます。
このような作用によって、正常細胞や前がん細胞においては、Nrf2の活性を亢進するNrf2活性剤は発がん過程を抑制するので、がん予防物質として認識されています。このようなNrf2の活性化を介したがん予防物質としてスルフォラファンやクルクミンやレスベラトロールなどが報告されています。(下図)
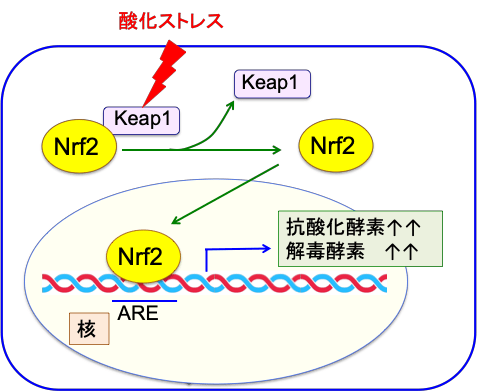
図:Keap1-Nrf2システムは酸化ストレスや有害物質に対する防御機構において重要な役割を担っている。転写因子のNrf2は細胞質でKeap1によって分解が促進されることによって活性が抑制されている。酸化ストレスが加わると、Keap1の構造が変化してNrf2から離れ、フリーになったNrf2が核内に移行して、抗酸化酵素や解毒酵素の遺伝子の上流に存在する抗酸化剤応答配列ARE(antioxidant response element)に結合して、これらの遺伝子の発現を亢進する。
【スルフォラファンはヒストン脱アセチル化酵素を阻害する】
スルフォラファンにはヒストン脱アセチル化酵素阻害作用が報告されています。例えば、以下のような報告があります。
A novel mechanism of chemoprotection by sulforaphane: inhibition of histone deacetylase.(スルフォラファンによる化学予防の新たなメカニズム:ヒストン脱アセチル化酵素の阻害)Cancer Res. 2004 Aug 15;64(16):5767-74.
スルフォラファンはヒストン脱アセチル化酵素を阻害する作用があるという報告です。
ヒストンはリシン(リジン)やアルギニンといった塩基性(プラスの電荷をもつ)のアミノ酸が多く、酸性(マイナスの電荷をもつ)のDNAと強い親和性を持っています。
ヒストンは、長いDNAをコンパクトに核内に収納するための役割と同時に、遺伝子発現の調節にも重要な役割を果たしています。ヒストンによる遺伝子発現の調節は複雑ですが、簡単にまとめると、「ヒストンとDNAの結合は転写に阻害的に働く」ということです。
遺伝子がmRNAに転写されるためには、転写因子やRNAポリメラーゼなどの他の蛋白質がDNAに結合する必要があり、ヒストンが結合していると転写に邪魔になります。したがって、転写の活発な遺伝子の部分ではヒストンとDNAの結合が緩くなっています。

図:細胞核内でDNAとタンパク質(ヒストンなど)の複合体をクロマチンという。クロマチンが凝集している部分はDNAが強く折り畳まれており遺伝子転写が抑制されている。一方、クロマチンが緩んでいる部分は、遺伝子の転写が活発になっている。
DNAとヒストンの結合を緩くする機序として、「ヒストンのアセチル化」という現象があります。アセチル化というのはアセチル(CH3CO)基が結合することです。
ヒストンのN末端領域のリシン残基のアミノ基(-NH2)がアセチル化という修飾を受けるとアミド(-NHCOCH3)に変換し、リシン残基の塩基性が低下して酸性のDNAとの親和性が無くなり、DNAからヒストンが離れ、DNAが露出することになります。
(下図)

図:ヒストン・アセチル基転移酵素によってヒストン・タンパク質のリシン(リジンとも言う)のアミノ基(-NH2)にアセチル(CH3CO)基が結合するとアミド(-NHCOCH3)に変換し、リシン残基の塩基性が低下して酸性のDNAとの親和性が無くなり、DNAからヒストンが離れ、DNAが露出することになる。その結果、遺伝子の転写が起こりやすくなる。
一般的に、ヒストンが高度にアセチル化されている領域の遺伝子は転写が活発に行われていることを示しています。すなわち、ヒストンのアセチル化は遺伝子発現を促進(正に制御)し、 反対に、ヒストンが脱アセチル化(低アセチル化)されることにより遺伝子発現は抑制(負に制御)されると考えられています。
ヒストンのアセチル化と脱アセチル化の反応は「ヒストンアセチル基転移酵素(=ヒストンアセチルトランスフェラーゼ)」と「ヒストン脱アセチル化酵素(=ヒストンデアセチラーゼ)」によってダイナミックに制御されており、遺伝子発現のON/OFFのメインスイッチになっていると考えられています。アセチル基はグルコースや脂肪酸の分解によって産生されるアセチルCoAが使われます(下図)。

図:ヒストンアセチル基転移酵素はヒストンをアセチル化することによってクロマチン構造を緩めて遺伝子転写を活性化する。一方、ヒストン脱アセチル化酵素はヒストンのアセチル化を減らすことによってクロマチン(DNAとヒストンの複合体)を凝集して遺伝子転写を抑制する。アセチル基はグルコースや脂肪酸が分解して産生されるアセチルCoAから供給される。
細胞のがん化の過程で、ヒストンや非ヒストンタンパク質の脱アセチル化が進むことが明らかになっています。そして、がん細胞ではヒストン・アセチル基転移酵素の発現や活性が低下し、逆にヒストン脱アセチル化酵素の発現と活性が亢進していることが明らかになっています。

図:ヒストンや非ヒストンタンパク質のアセチル化の状況はヒストン・アセチル基転移酵素(HAT)とヒストン・脱アセチル化酵素(HDAC)のバランスで決まる。がん細胞ではヒストン・アセチル基転移酵素(HAT)の発現や活性が低下し、ヒストン・脱アセチル化酵素(HDAC)の発現や活性が亢進して、タンパク質の脱アセチル化が亢進している。
以下のような報告があります。
A novel mechanism of chemoprotection by sulforaphane: inhibition of histone deacetylase.(スルフォラファンによる化学予防の新たなメカニズム:ヒストン脱アセチル化酵素の阻害)Cancer Res. 2004 Aug 15;64(16):5767-74.
スルフォラファンはがんを予防する効果があり、そのメカニズムとして第2相解毒酵素の強力な誘導作用が指摘されています。がんの発生予防だけでなく、スルフォラファンはがん細胞の増殖を抑制し、細胞死(アポトーシス)を誘導する作用も報告されています。この報告では、スルフォラファンがヒストン脱アセチル化酵素を阻害し、ヒストンのアセチル化を増やす効果を報告しています。
ヒストン脱アセチル化酵素の活性亢進は様々なヒストンアセチル化によって遺伝子発現に影響し、さらに非ヒストン・タンパク質の働きに影響し、これらの作用によって、がん細胞の脱分化、細胞増殖、浸潤・転移、細胞接着低下、アポトーシス抵抗性、血管新生を亢進し、がんの発生や悪性進展を促進する方向で作用しています。
したがって、ヒストン脱アセチル化酵素を阻害すること、あるいはヒストンのアセチル化の亢進はがん治療の有力な方法になります。

図:アブラナ科野菜の摂取で体内に吸収されるスルフォラファンは、ヒストン脱アセチル化酵素を阻害することによってヒストンのアセチル化を促進して、遺伝子発現状態に変化を及ぼす。その遺伝子発現の変化は抗がん作用と関連している。
【スルフォラファンは寿命を延ばす】
前述のように、スルフォラファンはNrf2の活性化によって抗酸化力や解毒力を高め、さらにヒストン脱アセチル化酵素の阻害によって遺伝子発現を制御しています。これらの作用はがんを予防し、寿命を延ばす効果があります。
さらに、インスリンやインスリン様成長因子-1(IGF-1)のシグナル伝達を阻害して寿命を延ばす効果が報告されています。以下のような報告があります。
Sulforaphane promotes C. elegans longevity and healthspan via DAF-16/DAF-2 insulin/IGF-1 signaling(スルフォラファンは、DAF-16/DAF-2 インスリン/IGF-1 シグナル伝達を介して C. elegansの寿命と健康寿命を促進する)Aging (Albany NY). 2021 Jan 20;13(2):1649-1670.
【要旨の抜粋】
ブロッコリー由来のイソチオシアネートのスルフォラファンは、炎症、酸化ストレス、がんを抑制するが、寿命への影響は不明である。
野生型と 9 つの変異株の線虫(C. elegans)にスルフォラファンを投与して老化や寿命に対する効果を検討した。
スルフォラファンは、可動性、食欲、および食物摂取量を増加させ、リポフスチンの蓄積を減らすことにより、寿命を延ばし、健康関連の表現型を促進した. メカンズム的には、スルフォラファンは、DAF-2 を介したインスリン/インスリン様成長因子シグナル伝達と、その下流の標的である AGE-1、AKT-1/AKT-2 を阻害した。これは、FOXO 転写因子ホモログ DAF - 16の核移行の増加と関連していた。一方、ストレス耐性と寿命を高めることが知られている標的遺伝子sod-3、mtl-1、およびgst-4の発現が亢進した。
これらの結果は、スルフォラファンがインスリン/IGF-1 シグナル伝達の抑制を介して、C. elegansの全寿命と健康寿命を延ばすことを示している。私たちの結果は、健康的な老化と病気の予防を促進するための栄養豊富なスルフォラファン戦略の基礎を提供する。
線虫のDAF-2という遺伝子は哺乳類のインスリン受容体に相当します。線虫のDAF-16は哺乳類のFOXOという遺伝子に相当します。
線虫やショウジョウバエを使って寿命に関わる遺伝子の研究が行われています。すなわち、線虫やショウジョウバエの突然変異系統(ミュータント:変異体)の中から寿命が延びた変異体を見つけ、どの遺伝子に突然変異が起きているかを解析すれば、寿命に関連する遺伝子を見つけることができます。
そのような研究によって寿命に関わる遺伝子が多数見つかっていますが、見つかった線虫やショウジョウバエの遺伝子の哺乳類の相同体を解析すると、それがインスリやインスリン様成長因子-1(IGF-1)の受容体やそのシグナル伝達系に関与する遺伝子だということが明らかになっています。
例えば、線虫の遺伝子でins-7とdaf-2と名付けられた遺伝子に突然変異がある変異系統の線虫は寿命が延びていました。そして、これらの遺伝子は哺乳類では、それぞれインスリンとインスリン受容体に相当するものでした。そして、インスリン受容体の下流に存在するシグナル伝達系に関与する遺伝子の突然変異も寿命を延長することが明らかになったのです。
このメカニズムはやや複雑なので、詳細は省きますが、簡単にまとめると「インスリン/IGF-1シグナル伝達系の活性化はがんを促進し、寿命を短縮する」そして「スルフォラファンはインスリン/IGF-1シグナル伝達系を阻害して寿命を延ばす」ということです。
スルフォラファンが抗酸化作用と抗炎症作用などによって循環器疾患やがんを予防し、寿命を延ばすという研究結果は多数報告されています。
【アブラナ科野菜を加熱調理するとスルフォラファンができない】
アブラナ科野菜の中にはスルフォラファンは存在しません。アブラナ科野菜に多く含まれるグルコシノレートという物質に、ミロシナーゼという酵素が作用してこれらの抗がん物質が生成します。生の野菜を噛んだり、ミキサーなどで細切して野菜の細胞を壊さないとスルフォラファンは生成しないのです。
生の野菜を噛んだり、ミキサーなどで細切して野菜の細胞を壊さないとスルフォラファンやインドール-3-カルビノールは生成しないのです。ミロシナーゼは酵素でタンパク質であるため、加熱調理するとタンパク質が変性して、酵素活性は消失します。
つまり、ブロッコリーやカリフラワーやキャベツを加熱調理するとそのがん予防効果や抗がん作用は低下することになります。したがって、アブラナ科野菜は生で食べたり、ジュースにして摂取するのがベストということになります。
ブロッコリーやカリフラワーやキャベツは生でも食べられますが、加熱調理しても、一つの工夫で抗がん作用を高めることができます。それは、「ミロシナーゼ活性を含む生のアブラナ科野菜を一緒に摂取する」という方法です。
加熱調理したブロッコリーでも、ミロシナーゼを含む食品と一緒に食べれば、ブロッコリーの抗がん作用が保たれるということを米国のイリノイ大学の食品化学・人間栄養学部門の研究グループが報告しています(Br J Nutr. 2012 May;107(9):1333-8)。
スルフォラファンは、ブロッコリーに存在するミロシナーゼによるグルコラファニンの加水分解に由来します。ブロッコリー粉末がサプリメントとして販売されていますが、ミロシナーゼが不活性化しているため、スルフォラファンの供給サプリメントとしての有効性が疑問視されています。実際、サプリメントとして販売されているブロッコリー粉末だけを摂取してもスルフォラファンの体内吸収はわずかです。
グルコラファニンを多く含むブロッコリー粉末を摂取しても、ミロシナーゼが不活性化していると、スルフォラファンは生成しないので、血中や尿中のスルフォラファンの量は上がりません。腸内細菌のミロシナーゼ活性によってスルフォランができる分しか体内に吸収しないということになります。
しかし、この研究では、ミロシナーゼ活性を有する生のブロッコリースプラウトを一緒に摂取すれば、スルフォラファンが十分に生成されるという臨床試験の結果を報告しています。その後多くの研究で追試され、同様の結果が報告されています。
ブロッコリーを茹でて、その煮汁を捨てるとグルコラファニンをロスします。煮汁にグルコラファニンが多く溶出しています。ブロッコリーやカリフラワーを茹でたときは、その煮汁を捨てないことです。
ミロシナーゼの活性の至適温度は 35〜40℃です。つまり、煮汁が40℃以下になってから、ミロシナーゼ活性をもつブロッコリースプラウトや大根おろしを混ぜれば、スープの中にスルフォランやインドール-3-カルビノールなどの抗がん成分が増えます。ミロシナーゼはビタミンCの存在で活性が顕著に亢進します。したがって、レモン汁などビタミンCの多い柑橘類を絞って混ぜるのも有用です。
私は、がん予防の料理として、「大根おろしぶっかけアブラナ科野菜スープ」というレシピを勧めています。
ブロッコリーやカリフラワーやキャベツを少量の水で煮て、少し冷まして40℃以下にして、それに大根おろしをたっぷり加えた料理です。このとき、煮汁は捨てないのがポイントです。
煮汁の中のグルコラファニンやグルコブラシシンと、大根おろしの中のミロシナーゼが反応して、スルフォラファンやインドール-3-カルビノールなどの抗がん作用のある成分が生成します。一緒に食べることによって、胃や小腸内でもこれらの抗がん成分が生成します。
生のブロッコリー・スプラウトや擂り下ろしたワサビなども同様な効果が期待できます。ライムやレモンなどのビタミンCの多い柑橘類を絞って加えるとさらにスルフォラファンの生成量が増えます。
ブロッコリーやカリフラワーやキャベツを全て生で食べるより、加熱調理してスープを捨てないで、大根おろしやブロッコリー・スプラウトのミロシナーゼ活性でイソチオシアネートやインドール-3-カルビノールを生成する方が効果が高いように思います。それは加熱調理することによって、他の植物成分も多く利用できるようになるからです。

図:ブロッコリーやカリフラワーを加熱してスープを作ると煮汁にグルコシノレート(グルコラファニン、グルコブラシシンなど)が多く含まれるが、加熱によってミロシナーゼは不活性化し、イソチオシアネート(スルフォラファン、インドール-3-カルビノールなど)は分解している(①)。このスープを40℃くらいに冷やした後に、大根おろし(②)や生のブロッコリースプラウト(③)や擦り下ろしたワサビ(④)を加えるとミロシナーゼの作用によってイソチオシアネート(スルフォラファン、インドール-3-カルビノールなど)が生成する。レモン(⑤)などビタミンCの多い食材を加えると、ミロシナーゼ活性を高めることができる。
食品成分の中には抗がん作用のあるものは多くあるのですが、調理法によってその摂取量に大きな差が出てくるのが、アブラナ科野菜です。アブラナ科の野菜の辛味成分には体内の解毒酵素の働きや抗酸化力を高める効果が知られています。
この辛味成分はアブラナ科野菜の調理の過程で生成します。すなわち、アブラナ科野菜に含まれるグルコシノレートがミロシナーゼという酵素によって分解され、イソチオシアネートという非常に辛い物質に変化します。このイソチオシアネートに強い抗がん作用と生体防御力を高める作用があります。
イソチオシアネートの産生を増やす調理法が、アブラナ科野菜の抗腫瘍効果を高めることができると言えます。がんの食事療法においては「何を食べるか」という点だけでなく、「どのように調理するか」という観点も重要であるということです。
大根おろしやブロッコリースプラウトなど、アブラナ科野菜をスルフォラファンが多く産生する調理法で食べると、がんを予防し、寿命を伸ばすことができます。
書籍紹介:
画像をクリックすると動画が始まります。
| « 857)SGLT2阻害... | 859)GPR109A(... » |





