がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
796)オメガ3系不飽和脂肪酸の抗がん作用(その1):食事中のオメガ3:オメガ6比の重要性

図:ω6系(n-6系)多価不飽和脂肪酸のアラキドンサンはプロスタグランジンE2やロイコトリエンなど炎症性メディエーターを産生して炎症や組織のダメージを悪化させ、がん細胞の増殖を促進する作用を持つ。一方、ω3系(n-3系)多価不飽和脂肪酸であるEPA(エイコサペンタエン酸)とDHA(ドコサヘキサエン酸)は代謝されて抗炎症作用を示す多様な脂質メディエーターを産生することによって、慢性炎症や組織のダメージを軽減する効果や、がん細胞の増殖を抑える効果を発揮する。この抗炎症作用や組織保護作用は抗がん剤や放射線治療による正常組織のダメージの軽減や悪液質の改善にも役立つ。食事から摂取したDHAやEPAは細胞膜に取り込まれ、細胞膜脂質二重層中のアラキドン酸と入れ替わるので、DHAやEPAの摂取が多いと炎症やがんの進行を抑制する効果が得られる。
796)オメガ3系不飽和脂肪酸の抗がん作用(その1):食事中のオメガ3:オメガ6比の重要性
【食べたものが体を作る】
私たちは、食物から摂取した栄養素(タンパク質・脂肪・糖質・ビタミン・ミネラルなど)から、細胞や組織を作る材料や体を動かすエネルギーを産生しています。細胞は下図のような脂質二重層から成る細胞膜によって細胞外と細胞内が分けられています。

図:リン脂質は親水性のリン酸部分の頭部に、疎水性の脂肪酸が2本の尾部がついた構造をしており、これが2重の層を形成して細胞膜が構成されている。水溶性の物質は脂肪の膜を通過できないので、細胞膜を貫通するようにタンパク質が存在し、物質を通す通路や外界の刺激を細胞内に伝える受容体として働いている。
食事から摂取された脂肪は代謝されてエネルギー源となり、また分解されて生成した脂肪酸は細胞膜などに取り込まれます。
細胞膜の構成成分として使われる場合、その脂肪酸自体は変化せず、それぞれの構造や性質を保ったまま使われます。
つまり、細胞膜をつくるとき脂肪酸の違いを区別せず、手当たり次第にあるものを使用するのです。その結果、食事中の脂肪酸の種類によって細胞の性質も変わってきます。
さらに、その細胞膜の脂肪酸から作られるプロスタグランジンやロイコトリエンなどの化学伝達物質の種類も違ってきて、炎症やアレルギー反応や発がんに影響することが明らかになっています。
例えば、リノール酸のようなω6系不飽和脂肪酸を多く摂取すると、血栓ができやすくなり、アレルギー反応を増悪させ、がんの発生頻度を高めます。ω6系不飽和脂肪酸を多く取り込んだがん細胞は増殖が早く転移をしやすくなります。
一方、魚油に多く含まれるドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)のようなω3不飽和脂肪酸を多く摂取すると、炎症やアレルギーを抑え、血栓の形成や動脈硬化やがん細胞の発育を抑える作用があります。DHAやEPAを多く摂取するとがん細胞が抗がん剤で死にやすくなることも報告されています。その理由は、食事から摂取されたω3不飽和脂肪酸ががん細胞の膜の脂質組成を変えることによって細胞シグナル系に影響して増殖を抑えるからです。
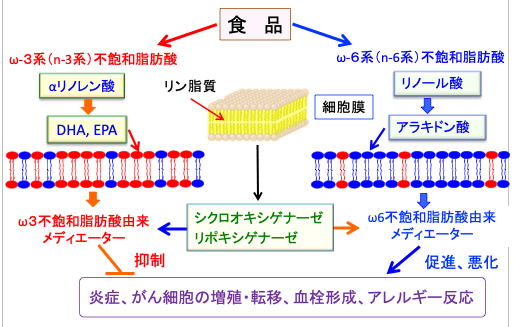
図:食品から摂取される脂肪酸はそのまま細胞膜の脂質二重層に組み込まれる。食事からのリノール酸やアラキドン酸の摂取が多いと細胞膜のアラキドン酸(細胞膜の図の青で示す)の量が増え、ω6不飽和脂肪酸由来のメディエーターの産生量も増える。一方、ω3系不飽和脂肪酸のドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)の摂取量が多いと、DHAやEPA(細胞膜の図の赤で示す)がアラキドン酸と置き換わるので、ω6不飽和脂肪酸由来のメディエーターの産生は低下し、ω3不飽和脂肪酸由来のメディエーターが増える。炎症やがん細胞の増殖・転移、血栓形成、アレルギー反応はω6不飽和脂肪酸由来メディエーターで促進・悪化され、ω3不飽和脂肪酸由来のメディエーターは抑制する。不飽和脂肪酸のω6:ω3の比を低下させると、がん細胞の増殖抑制、抗がん剤や放射線治療による正常組織のダメージの軽減や悪液質の改善の効果が増強する。
人間を含め哺乳動物は体内でオメガ6とオメガ3の不飽和脂肪酸を合成できないので、食事から取り入れています。つまり、体内で自分でつくることができないので、食事の変更による生体機能の変更を行うときの重要なターゲットになります。食事中の脂肪酸の種類によるがん細胞への影響の違いを知ることは、がんを抑える食事療法の実践において、極めて重要です。
【脂肪(油脂)はグリセリンと脂肪酸が結合している】
私たちは食物から様々な種類の「あぶら」を摂取しています。一般に、常温で液体のあぶらを油(oil)、個体のあぶらを脂(fat)と表記し、両方を総称して油脂と言います。ほとんどの植物性油や魚油は常温で液体の油になります。一方、多くの陸上動物(牛脂、豚脂、人間の脂肪など)と熱帯植物(ヤシ油、パーム油、ココアバターなど)のあぶらは常温で個体の脂です。
油脂は3価のアルコールであるグリセロール(グリセリンとも言う)1分子に3分子の脂肪酸 が結合した構造をしています(下図)。グリセロールには手(-OH)が3本あり、それに脂肪酸が結合して脂肪(油脂)になります。一般的には脂肪酸が3個ずつ結合してトリグリセリド(中性脂肪)と呼ばれます。脂肪の種類による違いは、グリセロールは全て共通するため、脂肪酸の形態で説明されます。
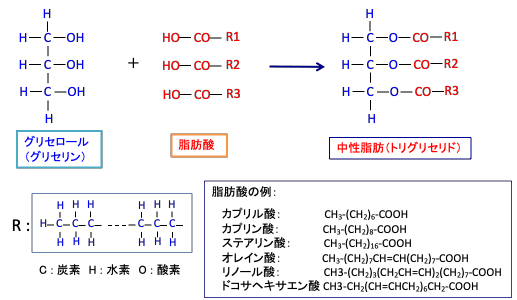
図:脂肪(油脂)は3価のアルコールであるグリセロール(グリセリン)1分子に3分子の脂肪酸が結合した構造をしている(図の上)。グリセロールには手(-OH)が3本あり、それに脂肪酸が結合して脂肪(油脂)になる。 R1,R2,R3と示す脂肪酸は1 個ないし複数個の炭化水素(CH2)の連結した鎖 (炭化水素鎖)からなる。脂肪酸の鎖(R1,R2,R3)の構造の違い(飽和脂肪酸や不飽和脂肪酸など)によって油脂の性状が違ってくる。脂肪の種類による違いは、グリセロールは全て共通するため、脂肪酸の形態で説明される。
脂肪酸は1 個ないし複数個の炭化水素(CH2)の連結した鎖(炭化水素鎖)からなり、その鎖の両末端はメチル基(CH3)とカルボキシル基(COOH)で、基本的な化学構造はCH3CH2CH2・・・CH2COOHと表わされます。
脂肪酸には、飽和脂肪酸と不飽和脂肪酸があり、飽和脂肪酸では、炭化水素鎖の全ての炭素が水素で飽和しています。一方、不飽和脂肪酸では炭化水素鎖中に1個ないし数個の二重結合(CH=CH)が含まれます。不飽和脂肪酸中で二重結合の数が2個以上のものを多価不飽和脂肪酸と云い、5 個以上の二重結合を持つ脂肪酸を高度不飽和脂肪酸と呼びます。
脂肪は、それを構成している脂肪酸の構造の違いによって融点などの化学的性状が異なってきます。二重結合をもつ不飽和脂肪酸の多い脂肪は常温で液状になりますが、飽和脂肪酸になると固まりやすくなります。固まりやすい脂肪を多く摂取すると血液がドロドロになって動脈硬化が起こりやすくなります。

図:脂肪酸は飽和脂肪酸と不飽和脂肪酸に分けられ、多価不飽和脂肪酸にはオメガ3系とオメガ6系がある。
【ω3 系とω6 系の不飽和脂肪酸はその働きに大きな違いがある】
リノール酸 CH3(CH2)3 CH2CH=CHCH2CH=CH(CH2)7COOH では、CH3 に最も近い二重結合は、CH3から6番目のCにあります。この位置に二重結合を持つ全ての脂肪酸をω6系不飽和脂肪酸に分類します。
α-リノレン酸CH3CH2CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH では、CH3に最も近い二重結合はCH3から3番目のC にあります。この位置に二重結合を持つ全ての脂肪酸をω3系不飽和脂肪酸に分類します。
最近ではω6の代わりにn-6 を用いてn-6系不飽和脂肪酸、そしてω3の代わりにn-3を用いてn-3系不飽和脂肪酸と呼ぶことが多くなっています(下図)。

図:CH3 に最も近い二重結合がCH3から3番目のCにある脂肪酸をω3系不飽和脂肪酸、CH3から6番目のCに最初の二重結合がある脂肪酸をω6系不飽和脂肪酸という。
動物(人を含む)はリノール酸とα-リノレン酸を合成できません。これら2種類の不飽和脂肪酸は動物にとって不可欠であり、動物はこれらを食物として摂取する必要がありますのでこれらを必須脂肪酸と言います。
ω6 系不飽和脂肪酸はリノール酸 → γ-リノレン酸 → アラキドン酸のように代謝されていき、アラキドン酸からプロスタグランジン、ロイコトリエン、トロンボキサンなどの重要な生理活性物質が合成されます。
アラキドン酸はリノール酸から体内で合成されますが、体内で十分な量が生成されないためアラキドン酸も必須脂肪酸になっています。
ω3系不飽和脂肪酸はα-リノレン酸 → エイコサペンタエン酸(EPA) → ドコサヘキサエン酸(DHA)と代謝されていきます。α-リノレン酸から体内でEPAとDHAが産生されますが、その量は少ないので、食事やサプリメントでEPAとDHAを積極的に摂取する意味はあります。
【DHAとEPAは抗炎症性メディエーターの前駆体】
DHAやEPAには抗炎症作用や鎮痛作用があります。実際に関節炎などの痛みを緩和し、CRP(C反応性たんぱく)などの炎症マーカーを低下させる作用もあります。そのメカニズムとしては、プロスタグランジンE2などの炎症を引き起こす物質を生み出すω6系のアラキドン酸がω3系のDHAやEPAに置き換えられ、したがって炎症物質ができにくくなるからといわれていました。すなわち、ω3系不飽和脂肪酸を多く摂取すると、細胞膜中のω3系不飽和脂肪酸が増加して、アラキドン酸濃度が低下するので、その結果アラキドン酸由来の炎症促進性物質の産生が抑制されるという機序です。
しかし、最近の研究では、ω3系不飽和脂肪酸のDHAとEPAが炎症を抑える物質を生成することによって能動的に炎症を抑制することが明らかになっています。外傷や感染などに反応して急性炎症反応が起こりますが、異物の排除が完了すると炎症反応は速やかに消散し、組織の修復過程に移行します。炎症反応が終了することを「炎症の収束」と言います。
炎症の収束は、これまで起炎反応の減弱化によると考えられてきましたが、最近の研究で、受動的なものではなく、能動的な機構であることが明らかになっています。急性炎症の特徴(症状)は白血球の組織への浸潤に伴う浮腫、発赤、発熱、痛みなどで、これらの反応にはアラキドン酸から生成されるプロスタグランジンやロイコトリエンなどの脂質メディエーターが関与します。これらの物質によって好中球の浸潤や活性化、血管透過性の亢進などの炎症反応が起こります。
炎症の収束過程においては炎症性サイトカインの産生が抑制され、血管透過性が正常に戻り、好中球の遊走阻止や浸出液中のリンパ球の除去や、マクロファージによる死滅した細胞の除去などが起こります。この炎症の収束過程には、EPAやDHAなどのオメガ3系不飽和脂肪酸から体内で生成されるレゾルビンやプロテクチンという抗炎症性メディエーターが関与します。

つまり、DHAやEPAはアラキドン酸と競合することで炎症性ケミカル・メディエーターの産生を阻害するだけでなく、抗炎症性(炎症収束性)の脂質メディエーターを生成することによって積極的に炎症を抑制する作用があるということです。
EPAやDHAの抗炎症作用やがん予防効果や心血管保護作用や脳神経系保護作用など多くの作用に、EPAやDHAから代謝されて生成される抗炎症性の脂質メディエーター(レゾルビンやプロテクチン)が関与しているようです。
【ω6系不飽和脂肪酸/ω3系不飽和脂肪酸の比を下げるとがん細胞はおとなしくなる】
プロスタグランジンE2(PGE2)という生理活性物質が増えすぎるとがん細胞の増殖や転移が速まることがわかっています。PGE2は細胞の増殖や運動を活発にしたり、細胞死が起こりにくくする生理作用があるため、がん細胞の増殖や転移を促進します。
PGE2はω6 系不飽和脂肪酸のリノール酸から合成され、ドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)などのω3 系不飽和脂肪酸はPGE2が体内で増えるのを抑える働きがあります。
脂肪酸の代謝産物は細胞内のシグナル伝達系に作用してがん遺伝子やがん抑制遺伝子の働きに影響を及ぼします。そして一般的に、DHAやEPAのようなω3系脂肪酸はがんの発育を抑制し、アラキドン酸のようなω6系脂肪酸はがんの発育を促進するので、摂取するω6系不飽和脂肪酸とω3系不飽和脂肪酸の比が腫瘍の発育に影響することになるのです。
つまり、肉や食用油はアラキドン酸などω6不飽和脂肪酸が多く、プロスタグランジンE2の産生を増やして、がん細胞の増殖・転移や血管新生を促進し、がん細胞のアポトーシス(細胞死)を抑制して再発促進に働きますが、一方、魚に含まれるDHAやEPAや、亜麻仁油や紫蘇油に含まれるα-リノレン酸などのω3不飽和脂肪酸は逆の作用でがんの発生や再発を抑制するのです。
DHAやEPAががんの予防や治療の効果を高めることは、多くの臨床的研究や実験的研究で 明らかになっています。毎日魚を食べている人は、そうでない人に比べ大腸がんや乳がんや前立腺がんなど欧米型のがんになりにくいという研究結果があります。特に前立腺がンを予防する効果は大規模な疫学研究で証明されています。
ニュージーランドのオークランド大学のNorrish博士らは、317症例の前立腺がんの患者と480人の対照とを比較し、EPAやDHAの豊富な魚油を多く摂取すると前立腺がんのリスクを半分程度まで減らせることを報告しています。
米国における47,882名の男性の食事の解析では、1週間に3回以上魚を食べるグループは、月に2回以下のグループと比較して、前立腺がんの発生頻度は7%の低下、進行した前立腺がんは17%の低下、転移のリスクは44%の低下を認めています。
スウェーデン人の6272名の男性を30年以上にわたって追跡調査した研究では、魚をほとんど食べないグループの前立腺がんの発生頻度は、魚を良く食べるグループの2~3倍でした。
魚を多く食べるエスキモーのイヌイット人27人の死者の解剖では、潜在的な前立腺がんは認められませんでした。前立腺の潜在がんは、アジアを含めて多くの国の男性では25~35%に発見されるという事実を考えると、前立腺の潜在がんが27例中1例も認められなかったことは特異なことであり、魚油の効果が示唆されています。
多くの基礎研究で、ω3脂肪酸は前立腺がん細胞の増殖を抑制することが報告されており、マウスに移植した前立腺がんの実験モデルでも、魚油による前立腺がんの増殖抑制作用が示されています。
DHAががん細胞の増殖速度を遅くしたり転移を抑制し、腫瘍血管新生を阻害し、がん細胞に細胞死(アポトーシス)を引き起こすことなどが多くのがん細胞で示されています。例えば、米国健康財団のローズ博士らは、ヒト乳がん細胞をヌードマウスに移植した動物実験で、DHAは腫瘍血管の新生を阻害して増殖を抑制し、がん細胞の肺への転移を防ぐことを報告しています。プロスタグランジンE2は血管新生を促進するので、プロスタグランジンE2産生を阻害するDHAには腫瘍血管の新生を阻害するようです。その他にも、抗がん剤の効果を増強し副作用を軽減する効果も報告されています。
がんの治療においてはDHAやEPAをサプリメントで多く摂取すると、体重減少が防げたり、がんの増殖速度が低下してがん組織が縮小するような例も報告されています。食事中の脂肪酸のω6:ω3の比が低いと、血管新生に必要な血管内皮細胞増殖因子(VEGF)の血中濃度が低下し、炎症反応も抑制されることが報告されています。
血管新生は微小転移巣が成長するときに必要で、炎症は発がんや再発のリスクを高めます。したがって、血管新生や炎症を抑えることは、がんの発生や再発を抑えることができるのです。
肉類にはアラキドン酸が多く含まれているので、肉を多く食べる人はがんになる危険が高いといわざるを得ません。リノール酸そのものは体に必須な物質ですが、大豆や米など植物性食品のほとんどに含まれているので、どうしても過剰摂取になりがちです。したがって、肉の替わりに魚を食べる回数を増やせば、がん細胞の増殖や血管新生を促進するプロスタグランジンE2ができにくくなって、がん増殖や再発が抑えることができることになるのです。
【ω3系不飽和脂肪酸を増やす食生活】
食事中の不飽和脂肪酸のオメガ6:オメガ3比は、狩猟採取で食品を確保していた旧石器時代の人類の食事では1〜2程度でしたが、近代における西洋型食事ではオメガ6:オメガ3比は20程度まで上昇しています。さらに動物性の飽和脂肪酸の摂取量も増えています。このような食事中の脂肪酸の組成の変化が、がんや心臓病、メタボリック症候群、炎症性疾患、自己免疫疾患の発症を促進していると考えられています。
アメリカ人の食事はω6:ω3の比が10~20になると報告されています。一方、伝統的な日本食(大豆と魚の豊富な食事)ではその比は1~2.8にあると言われています。しかし、日本でも食事の欧米化によってω6:ω3の比が高くなっています。
ω6:3の比を減らすとがんの発生や増殖や転移を減らすことができることが、大腸がん、乳がん、前立腺がんなどで確かめられています。
ω6:ω3の比を1~2以下にする食生活は、進行がんの食事療法として試してみる価値があります。肉類は極力控え、野菜はバランス良く摂取し、ω3不飽和脂肪酸の多い青背の魚(いわし・あじ・さば・さんま・まぐろなど)を食べます。野菜にはリノール酸などのω6脂肪酸が多いので、ω3不飽和脂肪酸のα-リノレン酸の豊富なシソ油か亜麻仁油をドレッシングとして使用するのが有効です。DHAやEPAは高熱で酸化しやすいので、魚は揚げ物や焼き魚は避け、生(刺身)か煮付けで食べることが大切です。
さらに、DHA/EPAのサプリメントを1日2~4グラム摂取すれば、ω6とω3の比をかなり下げることができます。免疫力が低下して生の食品摂取が危険な場合や魚が苦手な人もDHAやEPAのサプリメントを利用します。極端にω3脂肪酸を多くとると、血液が固まりにくくなるという副作用が出ますが、DHA/EPAのサプリメントを1日2~4グラム程度で、食事の内容を変えてω3不飽和脂肪酸を増やすのであれば、問題はありません。
【DHAは青い魚に含まれている】
DHAは、いわし、あじ、さば、さけ、にしん、などの「青みの魚」の脂肪に多く含まれます。がんの発生や再発予防には1日に1から2グラムが適量です。1グラム取るのにイワシなら二尾、アジやサンマなら一尾、マグロの中トロで4~5切れで十分で、毎日魚を食べる習慣にしておけば必要量は摂取できます。
不飽和脂肪酸は酸化されやすいので、新鮮な魚を生か煮て食べるのが理想です。フライや焼き魚にすると、 EPA や DHA を損失するだけでなく、高度不飽和脂肪酸が 酸素 と反応すると過酸化脂質となって発がんを促進することになります。また、焼き魚の焼け焦げは発がん物質になり、フライは揚げ油のリノール酸を魚が吸収するという問題もあります。
魚が苦手な人はサプリメントを利用するのも一つの方法です。DHAを補給するためのサプリメントが市販されています。魚の重金属汚染の問題や、高度不飽和脂肪酸は長期保存や加熱処理により酸化されやすという問題もあり、DHAをサプリメントで補給することの意義はあるようです。
また、養殖した魚は餌によってオメガ3:オメガ6の比が低下していると言う報告もあります。魚のDHAやEPAはプランクトンに由来します。天然のプランクトンの摂取が少ない養殖の魚はオメガ3が少ないという指摘もあります。
がん治療においては、サプリメントでDHAやEPAを1日3から4グラム程度摂取してオメガ6:オメガ3の比を1前後まで低下させると、がんは消滅するかもしれません。
【培養した微細藻類由来DHAが注目されている】
がんや認知症や循環器疾患の予防や治療にDHAやEPAが有効であることは確立しています。従って、DHAやEPAの多い脂の乗った魚を多く食べることが推奨されています。しかし、魚のメチル水銀やマイクロプラスチックなど海洋汚染に由来する有害物質の魚への蓄積の問題が、魚食を安易に推奨できない事態になっています。
メチル水銀は毒性が強く、血液により脳に運ばれ、やがて人体に著しい障害を与えます。母親が妊娠中にメチル水銀を体内に取り込んだことにより、胎児の脳に障害を与えることもあります。
魚は自然界に存在する水銀を食物連鎖の過程で体内に蓄積するため、日本人の水銀摂取の80%以上が魚介類由来となっています。魚摂取が増えるとメチル水銀の体内摂取が増え、胎児の脳の発育に悪影響を及ぼすことが明らかになり、厚生労働省は平成15年(2003年)に妊婦の魚摂取に関する注意事項を公表しています。つまり、妊婦や小児は魚を多く食べてはいけないと言っています。
海洋でDHAとEPAを作っている微細藻類を培養して、培養した微細藻類からDHAとEPAを取り出せば、汚染物質がフリーのDHA/EPAを製造できます。閉鎖環境での培養のため、汚染の心配がありません。植物由来なので菜食主義者も抵抗なく摂取できます。(下図)

図:オメガ3系多価不飽和脂肪酸のエイコサペンタエン酸(EPA)やドコサヘキサエン酸(DHA)は微細藻類が合成している(①)。プランクトン(②)が微細藻類を食べ、小型魚(③)がプランクトンを食べ、大型魚(④)が小型魚を食べるという食物連鎖によって、魚油にEPAやDHAが蓄積している。人間は魚油からDHAとEPAを摂取している(⑤)。環境中の水銀(⑥)が魚に取り込まれてメチル水銀になって魚に蓄積する(⑦)。DHAとEPAを産生している微細藻類をタンク培養して油を抽出すると(⑧)、汚染物質がフリーで、植物由来のDHA/EPAが製造できる(⑨)。
がん治療には1日3から5グラムのDHAの摂取が有効であることが多くの研究で示されています。通常の魚油の場合、DHA含有量は10%から20%程度です。1日5グラムのDHAを摂取するには25gから50gの魚油の摂取が必要になります。
そこで、微細藻類の中でもDHA含有量が極めて多いシゾキトリウム(Schizochytrium sp.)をタンク培養して製造したDHA(フランス製)を原料にした「微細藻類由来オイル(DHA含有量51%)」を製造してがん治療に使用しています。
詳細は以下のサイトで紹介しています。
| « 795)再利用医... | 797)オメガ3... » |




