がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
771)新型コロナウイルス感染症と肥満細胞(その1):抗ヒスタミン剤はサイトカインストームを抑制する?
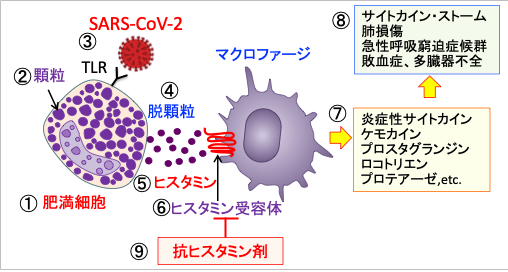
図:肥満細胞(①)は中身の詰まった顆粒(②)を多数有しており、この顆粒の中にはヒスタミンなどの炎症性メディエーターが含まれている。新型コロナウイルス(SARS-CoV-2)が肥満細胞のトル様受容体(TLR)に結合すると(③)、肥満細胞が活性化され、「脱顆粒」と呼ばれるプロセスを経て(④)、顆粒内部のヒスタミンをはじめとする炎症性メディエーターが遊離する(⑤)。ヒスタミンはマクロファージのヒスタミン受容体(⑥)に結合してマクロファージを活性化する。活性化したマクロファージは炎症性サイトカインやケモカインなどを産生・分泌し、炎症を引き起こす(⑦)。炎症や免疫応答が過剰になるとサイトカイン・ストーム、肺損傷、急性呼吸窮迫症候群(ARDS)、敗血症、多臓器不全が起こる(⑧)。抗ヒスタミン剤はヒスタミンによるマクロファージの活性化の過程を阻害して、過剰炎症を抑制し、重症化を予防する。
771)新型コロナウイルス感染症と肥満細胞(その1):抗ヒスタミン剤はサイトカインストームを抑制する?
【サイトカインストームがCOVID-19の病状悪化に関連する】
新型コロナウイルス感染症のCOVID-19(Coronavirus Disease 2019)はコロナウイルスのSARS-CoV-2(Severe Acute Respiratory Syndrome CoronaVirus 2)の感染によって発症します。
一般的に、約8割の患者は自然に軽快して治癒していますが、約2割の患者は肺炎を合併しています。肺炎に進展した患者のさらに⼀部が、重症化して集中治療や⼈⼯呼吸を要する状態になります。
新型コロナウイルス感染症(COVID-19)で死亡する場合は、肺と全身で重度の炎症反応が起こって、急性肺損傷、急性呼吸窮迫症候群(ARDS)、敗血症、多臓器不全が起こることが主な原因となっています。
体内に細菌やウイルスが侵入すると、体に備わった免疫システムが、これらの病原菌を排除するために働きます。このとき、サイトカインやケモカインというタンパク質が免疫細胞や炎症細胞から産生され、免疫細胞が活性化され、病原菌を排除します。敵が打倒されれば、免疫システムは自らオフになるように制御する仕組みがあります。
しかし、一部の人では、炎症反応や免疫応答が過剰に発現し、サイトカインが過剰に産生され、そうしたサイトカインがあやまって肺や肝臓など複数の臓器を傷害し、急性呼吸窮迫症候群(ARDS)や多臓器不全を引き起こします。
このようにサイトカインが過剰に産生される状態がサイトカイン・ストーム(cytokine storm)です。ストーム(Storm)は嵐という意味です。
急性呼吸窮迫症候群は、サイトカインストームの結果として生じることが多いと考えられています。したがって、サイトカイン・ストームの発生を予防できれば、重症化を防ぐことができます。

図:ウイルスは肺胞上皮細胞(①)や肺胞内のマクロファージ(②)に感染し、細胞内で増殖して数を増やし放出される(③)。感染した上皮細胞からサイトカインやケモカインが産生される(④)。マクロファージはT細胞にウイルス抗原を提示し(⑤)、活性化されたT細胞(⑥)や活性化したマクロファージ(⑦)からも炎症性サイトカインやケモカインが産生される。このような炎症応答が過剰に起こりサイトカイン産生抑制の制御が不能な状態になるとサイトカインストームが起こる(⑧)。サイトカインストームは、敗血症や急性呼吸窮迫症候群(ARDS)を引き起こす(⑨)。
【肥満細胞はヒスタミンを放出してサイトカインストームの発生を促進する】
最近の研究では、肥満細胞から分泌されるヒスタミンがサイトカインストームの早期の段階で関与している可能性が指摘されています。以下のような論文があります。
Mast cells activated by SARS-CoV-2 release histamine which increases IL-1 levels causing cytokine storm and inflammatory reaction in COVID-19(SARS-CoV-2によって活性化された肥満細胞はヒスタミンを放出し、IL-1レベルを上昇させ、COVID-19でサイトカインストームと炎症反応を引き起こす)J Biol Regul Homeost Agents. 2020 Sep-Oct,;34(5):1629-1632.
【要旨の抜粋】
SARS-CoV-2ウイルスは、COVID-19の患者に重度の急性肺損傷を引き起こし、死亡につながる場合もある。このような重度の病状は、ウイルスによって活性化されたマクロファージや肥満細胞などの免疫細胞の過剰反応が関連している。
SARS-CoV-2が感染後に発生する肺の局所炎症反応は、活性化された炎症性細胞と、気管支上皮細胞、内皮細胞、線維芽細胞などの肺組織細胞の複雑なネットワークによるものである。
SARS-CoV-2によって活性化された気管支上皮細胞および線維芽細胞は、炎症性サイトカインの発現を亢進し、肥満細胞の活性化を引き起こす。
さらに、接着分子の発現を介して白血球の移動を制御する内皮細胞は、インターロイキン(IL)-1、IL-6、およびケモカインを産生することによって白血球の活性化を増幅する。
このような病的環境では、肥満細胞の活性化により、ヒスタミン、プロテアーゼ、サイトカイン、ケモカイン、およびプロスタグランジンD2やロイコトリエンなどのアラキドン酸化合物が放出される。これらはすべて炎症ネットワークに関与している。
ヒスタミンは肥満細胞の分泌顆粒内に内因的に貯蔵され、細胞刺激後に血管内に放出される。ヒスタミンは、ケモカインIL-8およびサイトカインIL-6の発現を促進し、その効果はヒスタミン受容体拮抗薬によって阻害される。
IL-1は、主に炎症と免疫に活性を示す多彩は機能を持つサイトカインである。
トル様受容体(TLR)を介してSARS-CoV-2によって活性化された肺胞マクロファージはIL-1を産生し、これが肥満細胞を刺激してIL-6を産生する。 IL-1とIL-6の組み合わせは、致命的となる可能性のある過度の炎症を引き起こす。
数年前に発表された興味深い研究(E. Vannier et al、1993)では、ヒスタミンとIL-1が、微生物免疫細胞の活性化後の肺の炎症反応の病因に関与していることが示された。
ヒスタミンと組み合わせたIL-1は、IL-1レベルの大幅な増加を引き起こし、その結果、より高度な炎症を引き起こす可能性がある。しかし、ヒスタミン単独ではIL-1産生に影響を及ぼさないことが報告されている。
さらに、ヒスタミンは末梢単球のH2受容体を介してIL-1誘導性IL-6遺伝子の発現とタンパク質合成を増強する。
したがって、肥満細胞は炎症反応におけるヒスタミンの大規模な産生細胞であるため、この血管作用性アミンのヒスタミンは、IL-1の産生を増加させることにより、SARS-CoV-2に感染した肺の炎症過程を増幅する。ここでは、IL-1と組み合わせてウイルス感染SARS-CoV-2によって誘発される肺の炎症の増加を引き起こす可能性がある肥満細胞によって放出されるヒスタミンの新たな役割を初めて提案した。
ヒスタミン受容体拮抗薬は、ヒスタミンが受容体に結合することを妨げる作用を持つ薬剤です。
H1受容体拮抗薬はアレルギー疾患の治療に使われます。
H2受容体を阻害するH2受容体拮抗薬は特に薬剤は胃潰瘍や逆流性食道炎に対して治療効果を発揮します。胃の壁細胞にH2受容体が存在し、ヒスタミンが結合すると胃酸分泌が促進されますが、H2受容体拮抗薬が胃酸分泌を抑える働きをします。
この論文では、「ヒスタミンは末梢単球のH2受容体を介してIL-1誘導性IL-6遺伝子の発現とタンパク質合成を増強する。」と言っています。実際、H2受容体拮抗薬の胃薬のファモチジン(ガスター)もCOVID-19に対する治療効果が検討されています(後述)。
【抗ヒスタミン剤はCOVID-19のサイトカインストームの発生を抑制する?】
以下のような総説論文があります。
Could Histamine H1 Receptor Antagonists Be Used for Treating COVID-19?(ヒスタミンH1受容体拮抗薬はCOVID-19の治療に使用できるか?)Int J Mol Sci. 2021 Jun; 22(11): 5672.
【要旨】
COVID-19は急速に世界的大流行になり、広範囲にわたる長期的な健康問題を引き起こしている。SARS-CoV-2感染を制限し、COVID-19患者の転帰を改善する治療法を特定する緊急の必要性がある。過剰な肺の炎症は、重度のCOVID-19患者に共通する特徴である。したがって、肺の炎症を軽減することは、間違いなく臨床症状に利益をもたらす可能性がある。
ヒスタミンH1受容体(H1受容体)拮抗薬は、アレルギー性疾患を治療するために広く処方されている薬であるが、最近、抗SARS-CoV-2剤として大きな期待が寄せられている。
ここでは、SARS-CoV-2感染との闘いにおけるH1受容体拮抗薬の新しい使用法を簡単に要約する。 また、SARS-CoV-2におけるH1受容体拮抗薬の潜在的な抗ウイルスメカニズムについても考察する。 最後に、COVID-19の管理におけるH1受容体拮抗薬の使用の機会と課題について解説する。
SARS-CoV-2感染は、重度の呼吸器疾患や肺損傷を引き起こす可能性があります。肺損傷の重症度は、SARS-CoV-2感染時のマクロファージによるサイトカインストームの発生と相関しています。
さらに、COVID-19患者の死後の病理検査で血管周囲および間質組織における肥満細胞の増加が認められています。肥満細胞は、ヒスタミンを含む炎症性メディエーターを合成して分泌します。SARS-CoVの-2感染における肥満細胞の役割は、しばしば議論されています。肥満細胞から放出されるヒスタミンの関与について言及されています。
ヒスタミンとその受容体は、さまざまなアレルギー性疾患の進行に重要な役割を果たしています。特に、ヒスタミンH1受容体(H1受容体)は喘息などのアレルギー性肺疾患の発症に重要な関与が明らかになっています。したがって、その拮抗薬(阻害薬)は気道のアレルギー性炎症を治療するために使用されてきました。
ヒスタミンH1受容体拮抗薬はヒスタミンとその受容体の作用を阻止することによってCOVID-19の治療に役立つ可能性が指摘されています。
さらに、抗ヒスタミン薬にはヒスタミンとは関係ないメカニズムで、RNAウイルスの感染を阻害する抗ウイルス作用も報告されています。
【オータコイドと肥満細胞】
傷害や病原体の感染などで体の組織に異常が発生すると、それに対応するために異常部位に様々な細胞が動員され、様々な生理活性物質が産生されます。このような生体内で局所的に生成されて作用する生理活性物質を総称してオータコイド(Autacoid)といいます。
オータコイドは、動物体内で産生され微量で生理・薬理作用を示す生理活性物質のうち、ホルモン(特定の器官で分泌され血液で輸送されて他の器官に作用する)および神経伝達物質(シナプス間での情報伝達に関わる)以外のものの総称です。
オータコイドにはヒスタミン、セロトニン、ブロスタグランジン、サイトカインなどが含まれます。 ヒスタミンやセレトニンは細胞内に貯蔵されていて刺激に応じて細胞外に放出されますが、プロスタグランジンやサイトカインは刺激に応じて合成されます。
肥満細胞(マスト細胞, mast cell)は全身の粘膜下組織や結合組織に存在する骨髄由来の細胞で、血管が分布する組織であればほぼ全ての組織で見いだすことができます。
肥満細胞の中にはヒスタミンや炎症性サイトカインなどの各種化学伝達物質(ケミカルメディエーター)を含む顆粒が多く存在し、膨れた形態が肥満に似ているため肥満細胞という名称になっています。
肥満細胞は細胞表面にIgE受容体が存在し、これに抗原が結合したIgEを介して受容体の架橋が成立すると、それがトリガーとなって細胞膜酵素の活性化がうながされ、内容物である顆粒からヒスタミンなどが放出されます。これを脱顆粒と言います。花粉症や蕁麻疹は抗原刺激による肥満細胞の脱顆粒によるヒスタミン放出によって発症します。
肥満細胞はこのような即時型アレルギー反応の中心となって働く細胞ですが、近年では、アレルギー以外の様々な免疫応答や炎症反応に関与することや、疼痛にも関与することが明らかになっています(下図)。

図:肥満細胞はヒスタミンなどの炎症性メディエーターを含む顆粒を多く持つ。肥満細胞はIgEに対する受容体を持ち、抗原が結合したIgEを介して受容体が架橋することにより活性化され、「脱顆粒」と呼ばれるプロセスを経て、顆粒内部の炎症性メディエーターが遊離する。その結果、炎症や免疫応答などに関与する。
【抗ヒスタミン剤はCOVID-19の発症リスクを低下する】
COVID-19の多くの患者は、無症候性か、あるいは軽度の症状で治癒します。しかし、一部の患者は肺炎に移行します。
ヒスタミンH1受容体(H1受容体)拮抗薬は、花粉症や喘息などのアレルギー性疾患を治療するために広く処方されている薬ですが、COVID-19の重症化を抑制する効果が注目されています。
最近の疫学研究では、H1受容体拮抗薬を服用している患者はSARS-CoV-2感染に対してより耐性があることが報告されています。以下の様な報告があります。
Identification of antiviral antihistamines for COVID-19 repurposing.(COVID-19転用のための抗ウイルス性抗ヒスタミン薬の同定)Biochem Biophys Res Commun. 2021 Jan 29;538:173-179.
【要旨の抜粋】
SARS-CoV-2感染を予防し、COVID-19患者の転帰を改善する治療法を特定することが緊急に必要である。安全性が高い転用薬の検討は大きな利益をもたらす可能性があるが、COVID-19の予防や治療に広く利用可能な転用薬はまだ特定されていない。
承認されている医薬品の中からSARS-CoV-2に対するin vitro活性を持つ薬剤を特定するスクリニーニングの結果、ヒスタミン-1受容体を阻害する抗ヒスタミン薬が特定された。
SARS-CoV-2の検査を受けた219,000人以上の被験者の集団での薬の使用に関する記録を解析することにより、抗ヒスタミン薬のジフェンヒドラミン(diphenhydramine)、ヒドロキシジン(hydroxyzine)、アゼラスチン(azelastine)の使用は、61歳以上の被験者におけるSARS-CoV-2陽性率の低下と関連していた。
ジフェンヒドラミン、ヒドロキシジン、アゼラスチンは、in vitroでSARS-CoV-2に対して直接的な抗ウイルス活性を示した。特定の抗ヒスタミン薬が抗ウイルス効果を発揮するメカニズムは明らかではないが、ヒドロキシジン、そしておそらくアゼラスチンは、アンジオテンシン変換酵素2(ACE2)とシグマ1受容体と結合する。ジフェンヒドラミン、ヒドロキシジン、アゼラスチンのCOVID-19の補助療法としての有効性を検討する臨床試験が必要である。
アレルギー疾患の治療のために抗ヒスタミン薬(H1受容体拮抗薬)を服用している人は新型コロナウイルス(SARS-CoV-2)の感染が少ないという疫学データです。
そのメカニズムとしてH1受容体拮抗作用以外に、SARS-CoV-2に対して直接的な抗ウイルス活性を示す可能性を指摘しています。
さらに、スペインのタラゴナ地域(50歳以上の79,083人)での観察研究は、H1受容体拮抗薬を服用している人ではSARS-CoV-2感染(PCR陽性率)リスクが有意に低いことが報告されています。以下のような報告があります。
Influence of prior comorbidities and chronic medications use on the risk of COVID-19 in adults: a population-based cohort study in Tarragona, Spain(成人のCOVID-19のリスクに対する併存疾患と慢性薬の使用の影響:スペイン、タラゴナでの人口ベースのコホート研究)BMJ Open. 2020; 10(12): e041577.
スペインのタラゴナ(Tarragona)の12ヶ所の診療所の50歳以上の受診者79083人(77,676人の地域住民と1407人のナーシングホーム居住者)を対象とした住民ベースの後ろ向きコホート研究です。
研究期間中、2324人のコホートメンバーがPCR検査を受け、1944人が陰性で380人が陽性でした。年齢(HR 1.02; 95%CI 1.01〜1.03; p = 0.002)、ナーシングホーム居住(HR 21.83; 95%CI 16.66〜28.61; p <0.001)、利尿薬の投与(HR 1.35; 95%CI 1.04〜1.76; p = 0.026)は、感染リスクの増加と独立して関連していました。
喫煙(HR 0.62; 95%CI 0.41〜0.93; p = 0.022)、ACE阻害薬(HR 0.68; 95%CI 0.47〜0.99; p = 0.046)および抗ヒスタミン薬(HR 0.47; 95%CI 0.22〜1.01; p = 0.052 )はより低いリスクと関連していました。地域在住の個人では、がん(HR 1.52; 95%CI 1.03〜2.24; p = 0.035)、慢性呼吸器疾患(HR 1.82; 95%CI 1.08〜3.07; p = 0.025)および心臓病(HR 1.53; 95%CI 06〜2.19; p = 0.021)はリスクの増加に関連していました。
ACE阻害薬(HR 0.66; 95%CI 0.44〜0.99; p = 0.046)およびインフルエンザワクチン接種(HR 0.63; 95%CI 0.44〜0.91; p = 0.012)の投与は、リスクの低下と関連していました。
以上から、この疫学研究では、年齢、ナーシングホームの居住者、および複数の併存疾患(がん、慢性呼吸器疾患、心臓病)がCOVID-19の感染リスクを高める要因となり、ACE阻害薬、抗ヒスタミン薬、インフルエンザワクチン接種は感染リスクを低下させる要因となることを示しています。
ナーシングホーム(Nursing home)は日常的な医療・介護やリハビリを必要とする人のための施設で、一般住民に比べてより多くの基礎疾患を有しているグループになります。高齢者や基礎疾患(がん、慢性呼吸器疾患、心臓病など)の存在がCOVID-19の発症や重症化のリスクを高めることはよく知られています。
利尿剤使用も、高血圧や心不全や腎臓病などの重症化リスクを高める疾患の存在を示唆します。
新型コロナウイルスSARS-CoV-2が細胞内に侵入するとき、ウイルスのスパイクの糖タンパク質と宿主細胞の細胞膜に存在するアンジオテンシン変換酵素2(ACE2)が結合する必要があります。ACE阻害薬を服用している人はSARS-CoV-2の感染リスクが低下することが報告されてます。
さらに、抗ヒスタミン剤を服用している人はSARS-CoV-2感染のリスクが低下する可能性があるということです。
【抗ヒスタミン剤はCOVID-19の重症化リスクを低下する】
H1受容体拮抗薬と抗生物質のアジスロマイシンによる治療は、SARS-CoV-2に感染した高齢患者の重症疾患への進行を防ぐ可能性が報告されています。
Antihistamines and azithromycin as a treatment for COVID-19 on primary health care – A retrospective observational study in elderly patients(プライマリヘルスケアにおけるCOVID-19の治療としての抗ヒスタミン薬とアジスロマイシン–高齢患者を対象とした遡及的観察研究)Pulm Pharmacol Ther. 2021 Apr; 67: 101989.
2020年3月から4月の間に、スペインのトレド(Toledo)の2つの老人ホームに住んでいるCOVID-19が疑われる84人の高齢患者が、抗ヒスタミン薬(デクスクロルフェニラミン、セチリジン、またはロラタジン)で早期に治療され、COVID-19の症状を呈した25人にはアジスロマイシンが追加されました。
主要評価項目は、COVID-19の致死率で、副次的評価項目は、病院とICUの入院率でした。この患者集団では、入院、死亡、または薬物の副作用は報告されませんでした。 6月末までに、住民の100%がCOVID-19に対して陽性を示しました。
COVID-19の治療における両薬剤の有効性を決定するために臨床試験が必要ですが、この研究では、抗ヒスタミンおよび選択された症例のアジスロマイシンによる併用治療がCOVID-19を治療し、重篤な疾患への進行を防ぐ可能性があることを示唆しています。
アジスロマイシンはマクロライド系抗菌薬で、COVID-19に対する有効性が報告されています。H1受容体拮抗薬と併用すると、COVID-19に対する治療効果が高まる可能性を示唆しています。
この研究で使用されているセチリジン(cetirizine)は、第二世代抗ヒスタミン薬のひとつで、日本ではジルテックの商品名が販売されています。適応はアレルギー性鼻炎や蕁麻疹、皮膚の発疹、湿疹です。
第2世代の抗ヒスタミン薬(ヒスタミンH1受容体拮抗薬)の特徴は、ヒスタミン受容体に対する選択性が高く、抗コリン作用などよけいな作用が減弱されているため、第1世代に多い口の渇きや排尿障害などの副作用がほとんどみられません。脂溶性が低く脳に入りにくいので、眠気の副作用も軽減されています。このような利点から、アレルギー性疾患に幅広く用いられるようになりました。
ヒスタミンH1受容体拮抗薬(H1ブロッカー)はアレルギー疾患に使われます。
ヒスタミンH2受容体拮抗薬(H2ブロッカー)は胃の壁細胞のヒスタミンH2受容体を遮断することにより胃酸分泌を抑制するため、胃酸抑制薬として使用されます。
H1ブロッカーのセチリジンとH2ブロッカーのファモチジンを併用してH1 / H2受容体を二重遮断するとCOVID-19患者の肺症状が緩和されることが報告されています。肺症状の緩和は、ヒスタミンを介したサイトカインストームを抑えるためと考えられています。以下のような報告があります。
Dual-histamine receptor blockade with cetirizine - famotidine reduces pulmonary symptoms in COVID-19 patients(セチリジンとファモチジンによるヒスタミン受容体の二重遮断はCOVID-19患者の肺症状を軽減する)Pulm Pharmacol Ther. 2020 Aug; 63: 101942.
【要旨】
背景:
SARS-CoV-2感染によるCOVID-19は、肺のサイトカインストームの結果として急性呼吸窮迫症候群を引き起こす可能性がある。抗ヒスタミン薬は、炎症とサイトカイン放出を減らすための安全で効果的な治療法である。
ヒスタミン1およびヒスタミン2受容体拮抗薬の組み合わせは、蕁麻疹に効果的であり、COVID-19におけるヒスタミン媒介性肺サイトカインストームを軽減する可能性がある。ヒスタミン1とヒスタミン2受容体遮断薬の組み合わせは、COVID-19入院患者の転帰を改善する可能性がある。
方法:
医師主導の臨床試験が、重度から重篤な肺症状のある入院患者を対象に実施された。110人の重症患者を標準治療に加えてセチリジン10 mgを1日2回およびファモチジン20mg を1日2回投与した。
結果:
蘇生禁止指令のある患者を含め、ヒスタミン受容体二重遮断療法を少なくとも48時間受けたすべての患者の挿管率は16.4%であった。48時間の治療後の挿管率は7.3%であった。入院患者の死亡率は15.5%、入院期間は11.0日であった。この薬剤の組み合わせは、COVID-19入院患者の公表された報告と比較した場合、入院患者の死亡率と症状の進行の有益な減少を示した。併用薬が評価され、ヒドロキシクロロキンはより悪い結果と相関していた。
結論:
セチリジンとファモチジンのこの医師主催のコホート研究は、おそらくヒスタミンを介したサイトカインストームを最小限に抑えることによって、症状の重症度の進行を軽減するための安全で効果的な方法の有効性を示唆している。
ファモチジンの商品名はガスターです。一般用医薬品としてドラッグストアでも購入できるガスター10と同じで、安全性の高い薬です。ジェネリックもあります。第1類医薬品として薬局でも購入できます。
ヒスタミンは、炎症反応や胃酸分泌、アレルギー反応など様々な生理反応に関与しています。ヒスタミンは細胞表面にある受容体に結合することによって細胞にヒスタミンの刺激を伝えます。
ヒスタミンの主な産生場所は、体内では神経と胃の一部の細胞や肥満細胞(マスト細胞)、好塩基球などです。ヒスタミンを介して指令を受け取る受容体は、H1からH4までの4つの型が存在し、それぞれ体内で存在する場所が異なります。
臨床的に重要なH1受容体は主に血管内皮細胞や平滑筋、神経細胞に分布し、H2受容体は消化管、心臓、神経細胞に分布します。
ヒスタミン受容体拮抗薬は、ヒスタミンが受容体に結合することを妨げる作用を持つ薬剤です。
H1受容体拮抗薬はアレルギー疾患の治療に使われます。
血管内皮細胞に存在するH1受容体はヒスタミンと結合すると末梢の血管を拡張させたり、血管透過性を亢進させる働きがあるため、粘膜を充血させたり腫脹させたりします。また、神経に存在するH1受容体が作用するとかゆみとして認識されます。このような不快な症状を抑えるために投与されるのがH1受容体拮抗薬です。
H2受容体を阻害するH2受容体拮抗薬は特に薬剤は胃潰瘍や逆流性食道炎に対して治療効果を発揮します。
胃の壁細胞にH2受容体が存在し、ヒスタミンが結合すると胃酸分泌が促進されますが、H2受容体拮抗薬が胃酸分泌を抑える働きをします。
第一世代抗ヒスタミン薬はイタリアの薬理学者Daniel Bovetにより1930から40年代に最初に開発され、多くの中枢神経系作用薬(抗精神病薬や抗うつ薬など)の原型になりました。Bovetはその業績によって1957年にノーベル医学生理学賞を受賞しています。
さらに、H2 受容体拮抗薬を開発した James Blackは1988年にノーベル医学生理学賞を受賞しています。
ヒスタミン受容体の発見と抗ヒスタミン薬の開発は医学的に非常に重要な業績だということです。
H2受容体拮抗薬のファモチジン(商品名:ガスター)のCOVID-19に対する治療効果はまだ議論があります。有効という報告もありますが、効果を認めなかった臨床試験の結果も多く報告されています。
新型コロナウイルス感染症の多くは発病して通常は7日から10日で自然に治りますが、肺炎が進行して重症化してサイトカインストームのリスクがあるときは、抗ヒスタミン薬の服用が治療効果が期待できるようです。
H1 受容体拮抗薬のセチリジンは鼻炎治療薬の「新コンタック鼻炎Z」などの一般用医薬品に入っており、H2 受容体拮抗薬のファモチジンは「ガスター10」などの一般用医薬品として販売されているので、薬局で購入できます。
COVID-19が発病して1週間経過しても軽快する気配がなく、肺炎症状がでかかってきても、自宅待機しかできない時は、セレイチジンとファモチジンの併用は、症状の改善とサイトカインストームへの進行を予防する方法として試してみる価値はあると思います。少なくとも、副作用の少ない薬の組み合わせです。
もちろん、実際に試す場合は、自己責任にんります。しかし、肺炎が進行しても入院できない状況になった時は、サイトカインストームの進行を抑える副作用の少ない方法だと思います。
| « 770)新型コロ... | 772)新型コロ... » |



