がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
815)高齢者の抗がん剤治療にエビデンスがあるのか?
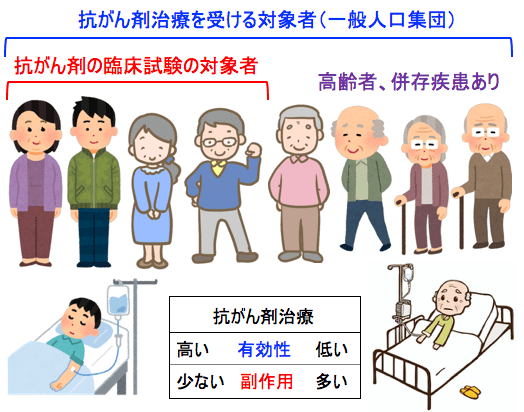
図:臨床試験の大多数は、全身状態が良く、がん以外に健康問題はほとんどないと言った理想的な患者を使って薬を検証している。 このような理想的な集団での試験は、治療薬の有効性が高く、副作用が少ない結果が得られる。抗がん剤治療を受ける一般人口集団には高齢者や併存疾患を有するがん患者も含まれる。高齢者や併存疾患を有する患者の場合は、臨床試験の結果と比べて、副作用は多く、利益(効果)は少なくなる可能性が高い。つまり、最高の条件で実施された臨床試験で承認された薬物は、高齢者や併存疾患を有する患者などを含む現実世界の集団を代表するものではない可能性がある。
815)高齢者の抗がん剤治療にエビデンスがあるのか?
【医者は抗がん剤治療を受けない】
週刊誌のアエラ(朝日新聞出版)の2018年2月12日号に「医師ががんになったら、どんな治療法を選択するのか」という内容の記事が載っています。内容の抜粋はネットで見れます。(こちらへ)
ステージ4(がんが他の臓器に転移している状態)の進行がんになったとき、医師がどのような治療法を選択するのかを、20代から60代までのがんの診療経験のある現役医師553人にアンケートで調査しています。
その結果、ステージ4のがんに対する治療として、抗がん剤治療を受けずに緩和ケアを選ぶ医師が40%前後という数字を報告しています。
具体的には、緩和ケアを選ぶ医師の割合は、胃がんが40%、大腸がんが35%、肝臓がんが43%、肺がんが40%、食道がんが39%、膵臓がんが56%、乳がんが32%、子宮がんが35%となっています。(詳しくはこちらのサイトへ)
がんの種類によって抗がん剤の有効性が異なります。
膵臓がんの場合、緩和ケアを選ぶ医師が56%と多い理由として、この記事では「効く薬がないから」「痛いのはいや」「治療がしんどい」「現時点で有効な治療手段がない」「治る見込みがないなら、好きに過ごしたい」と言う意見を紹介しています。
週刊誌の記事ですので、どの程度の信頼性があるかは不明ですが、ステージ4の進行がんに対して、抗がん剤治療の有効性が低いこと、副作用の割に得られるものが少ないことは、医師であれば十分に認識しています。したがって、「膵臓がんや肺がんや肝臓がんになったら、抗がん剤治療は積極的には受けない」という意見を持つ医師が40から50%というのは妥当な数字のように思います。
【米国食品医薬品局(FDA)承認の抗がん剤の半数以上は臨床的有益性がない】
米国では医薬品の承認は食品医薬品局(FDA)が行っています。 FDAによる新薬承認のハードルは日本に比べてかなり高く、臨床的なエビデンス(証拠)が十分になければ承認されないと一般的には考えられています。しかし、抗がん剤の場合は事情が異なるようです。
フランスと米国の疫学や統計学が専門の研究グループが、2000年から2015年の間にFDAによって承認された進行した固形がんを治療するための新しい抗がん剤および生物製剤の全てについて、臨床的有用性を総合評価しています。結論は、FADが承認している抗がん剤の多くが十分な臨床的有益性が認められないというものでした。
以下のような報告があります。
Clinical benefit, price and approval characteristics of FDA-approved new drugs for treating advanced solid cancer, 2000-2015. (進行した固形がん治療のためのFDA承認の新薬の臨床的利益、価格、承認特性、2000-2015)Ann Oncol. 2017 May 1;28(5):1111-1116.
【要旨の抜粋】
材料と方法:2000年から2015年の間にFDAによって承認された進行した固形がんを治療するための新しい抗がん剤および生物製剤をすべて含めて検討した。
医薬品の臨床的利点は、米国臨床腫瘍学会の臨床価値枠組み(ASCO-VF )の2016年更新版および欧州腫瘍学会の臨床利益スケール(ESMO-MCBS)を用いて、主要な臨床試験のFDA医学的レビューに基づいてグレード化した。
薬物の特性および承認は、公的に入手可能なFDA文書から得られ、価格は、米国メディケア、米国退役軍人健康管理および英国市場システムによって評価された。
結果: 2000年から2015年までの間に、FDAは固形がんの治療のための51個の新薬を承認した。 そのうち37個の薬物(73%)の価値を評価することができた。
ESMO-MCBSの指標では、5個(14%)がグレード1(最低)、9個(24%)がグレード2、10個(27%)がグレード3、11個(30%)がグレード4、2個(5%)がグレード 5(最高)と評価された。したがって、13の薬物(35%)は有意な臨床的有益性を示した(スケールレベル4および5)。
ASCO-VF(3.4-67の範囲を有する)による評価では、薬物評価の中央値は37(20-52)であった。臨床的利益と薬価との間には相関が見られなかった(P = 0.9)。 薬物および承認の特徴は、臨床的利益と有意に関連していなかった。
結論: FDAが最近認可した新しい抗がん剤の多くは、現在の評価スケールで測定されたように、高い臨床的利益をもたらさなかった。 薬物価格と社会および患者の利益との間には関係は認めなかった。
抗がん剤の有効性を評価する指標として、「生存期間の延長」と「生活の質(QOL)の改善」の両方が重要です。ある抗がん剤治療で生存期間が3ヶ月延長しても、副作用が強く、苦しんでの3ヶ月延長(苦しむ期間は抗がん剤治療期間全体なのでもっと長い)では、臨床的に意味のある有益性があるとは評価できません。副作用が少なく、1年間の生存期間の延長が得られる治療であれば、臨床的有益性はかなり高いと評価できます。
費用も評価の対象になります。平均生存期間が6ヶ月から8ヶ月に2ヶ月延長するときに8ヶ月間の薬剤費が2000万円だとしたら、私は受ける気がしません。
日本の場合は、国民皆保険制度と高額療養費制度などによって、1ヶ月に何百万円もする抗がん剤治療でも自己負担は数万円ですむので、気兼ねなく高額な新薬が使用されています。
このように、抗がん剤の有益性の評価は、生存期間の延長の程度や副作用やQOLの改善度や費用などを総合的に検討する必要があります。
この目的で、米国臨床腫瘍学会(ASCO)や欧州腫瘍学会(ESMO)は、がん治療の臨床的利益を定量化するための枠組み(Value Framework;VF)や臨床利益スケール(Magnitude of Clinical Benefit Scale;MCBS)を作成しています。
この論文では、米国臨床腫瘍学会の臨床価値枠組み(ASCO-VF)の2016年更新版および欧州腫瘍学会の臨床利益スケール(ESMO-MCBS)で、FDAが2000年から2015年の間に承認した抗がん剤を臨床的有益性の観点から分析しています。
SCO-VFとESMO-MCBSはいずれも生存率改善や毒性やQOLを定量化し、ASCO-VFでは130点満点のスコアで、ESMO-MCBSでは5段階のグレードで評価しています。
その結果、ESMO-MCBSではグレード評価では、評価できた37個の抗がん剤のうち有意な臨床的有益性(スケールレベル4および5)が認められたのは13個(35%)で残りの65%の薬は有意な臨床的有益性があるとは評価されないという結果でした。
また、臨床的利益と薬価との間には相関が見られないことも明らかになっています。高い薬が効くわけでも無いということで、臨床的に有益でないのに極めて高価な薬剤が承認されていることを示唆しています。
同様の内容の論文は数多く報告されています。承認されている抗がん剤の有効性に多くの研究者が疑問を持っていることを示唆しています。
【臨床試験において抗がん剤の毒性(副作用)は軽視されている】
以下のような論文があります。
Efficacy, safety and tolerability of drugs studied in phase 3 randomized controlled trials in solid tumors over the last decade.(過去 10 年間に固形腫瘍を対象とした第 3 相ランダム化比較試験で研究された薬剤の有効性、安全性、忍容性)Sci Rep. 2021; 11: 10843.
【要旨】
新しく承認された抗がん剤の臨床試験において、その安全性と忍容性が対照群よりも悪いことが示唆されている。第3相ランダム化比較試験で研究された薬剤の有効性と毒性のバランスについては、あまり注目されていない。
Clinicaltrials.gov を検索して、2005 年 1 月から 2016 年 10 月までに完了した進行性の乳がん、結腸直腸がん、肺がん、または前立腺がんの患者を対象とした第3相ランダム化比較試験を特定した。
論文のデータから有効性と安全性のデータを抽出した。無増悪生存期間および全生存期間の有効性ハザード比が抽出された。
安全性に関しては、毒性による死亡、がんの悪化を伴わない治療中止、グレード 3/4 の有害事象について、オッズ比と95% 信頼区間 (CI) を計算した。その後、メタ分析でデータがプールされた。
最初に特定された 377 件のランダム化比較試験のうち、88,603 人の患者を含む 143 件のランダム化比較試験が分析に含まれた。
これらのうち、79 件 (57%) の試験が主要評価項目を達成した。対照群と比較して、無増悪生存期間(ハザード比 0.80; 95% CI 0.78–0.82) と全生存期間 (ハザード比 0.87; 95% CI 0.85–0.89) の両方が実験薬で改善された。
毒性による死 (オッズ比 1.14; 95% CI 1.03–1.27)、がんの悪化を伴わない治療中止 (オズ比1.64; 95% CI 1.56–1.71)、およびグレード 3/4 の 有害事象も、それぞれの対照群と比較して、実験薬でより多く発生した。
一般的な固形がんを対象とした第3相ランダム化比較試験の半数以上が主要評価項目を達成したが、半数近くで実験的治療は対照群と比較して安全性が劣っていた。
つまり、固形腫瘍を対象にした治療薬の第3相ランダム化比較試験において、治療薬は無増悪生存期間や全生存期間においてある程度の有効性を認められていますが、毒性による死亡や治療中止やグレード 3/4 の 有害事象は治療薬で多いということです。
この場合、無増悪生存期間や全生存期間が年単位で延長するのであれば、多少の毒性は許容できるかもしれません。しかし、実際は数ヶ月、多くは2ヶ月前後です。
以下のような報告があります。
Risks and benefits of anticancer drugs in advanced cancer patients: A systematic review and meta-analysis.(進行がん患者における抗がん剤のリスクと利点:系統的レビューとメタ分析)EClinicalMedicine. 2021 Oct; 40: 101130.
【要旨】
背景:標準治療の選択肢を使い果たした患者を対象に、実薬対照を用いない抗がん剤の無作為化臨床試験における抗がん剤の安全性と有効性を定量化することを目的とした。
方法:2000 年 1 月 1 日から 2021 年 1 月 7 日までの英文出版物の体系的な文献検索は、MEDLINE (PubMed) を使用して実行された。進行性固形がんの成人患者における抗がん剤治療を評価する臨床試験で、対照抗がん剤を使用しない緩和ケアのみを対照群とする全てのランダム化比較試験が含まれていた。
2 名の著者が独立して研究をレビューして選択した。公開された論文からのデータは、調査員によって抽出された。無増悪生存期間と全生存期間の全体的なハザード比を推定した。重度の毒性と有効性の相関関係が評価された。
結果:スクリーニングされた 3,551 件の研究のうち、47,432 人の患者を対象とした 128 件の臨床試験が基準を満たしていた。無増悪生存期間 および全生存期間の ハザード比は 0.58 [95%CI: 0.53–0.63] および 0.82 [95%CI: 0.78–0.85] であった。しかし、絶対的な利益は限られており、無増悪生存期間と全生存期間の増加は 2.1 か月と 0.5 か月であった。2つのアーム間のすべてのグレード、重度のグレードIIIとIV、およびグレードV(死亡)の有害事象における絶対過剰は、+13.9%、10.2%、および+0.5%であった。重篤な毒性と有効性との間に弱い相関関係が認められた。
解釈: ランダム化比較試験で評価された抗がん剤は、積極的な治療を受けていない患者にくらべて、試験参加者に利益をもたらした。重度の毒性は有効性と有意な相関は認めなかった。
この臨床試験では標準治療を使い果たした進行がん患者に対して、抗がん剤治療を受けた群が無増悪生存期間が2.1ヶ月と全生存期間が 0.5 か月延長したので、患者に利益をもたらしたと評価しています。0.5ヶ月は15日です。15日間の延命で臨床的有効性を認めるのが標準治療です。有害事象(副作用)は増えますが、あまり重視されていません。
【抗がん剤の臨床試験は高齢者や他の疾患のある患者は除外している】
臨床試験の結果を全ての患者に当てはめることはできません。製薬企業が主導しているランダム化比較試験は、高齢患者や併存疾患および特定の併用薬を有する患者を除外しています。
これは、実際の診療と比較して、ランダム化比較試験の参加者はパフォーマンスステータス(全身状態の指標)が高く、併存疾患が少なく、治療の忍容性が高いと予想されます。
このような利益(効果)が出やすく、リスク(副作用)が出にくい最高の条件で実施された臨床試験で承認された薬物は、高齢者や併存疾患を有する患者などを含む現実世界の集団を代表するものではない可能性があります。
つまり、高齢者や併存疾患を有する患者の場合は、臨床試験の結果と比べて、副作用は多く、利益(効果)は少なくなる可能性が高いことは常識的に推測できます。
さらに、臨床試験の実施法や評価法にも問題が存在します。
米国食品医薬品局や欧州医薬品庁が最近承認した50以上の抗がん剤うち、『半数以上は延命効果が証明されていない』『臨床的に意味のある生存期間の延長は16%』という事実が報告されています。
この原因の一つは、承認までの期間を短縮させるために、全生存期間の延長というエンドポイントの代わりに、奏功率(腫瘍の縮小の度合い)や無増悪生存期間という代用エンドポイントを用いて臨床試験を評価していますが、この代用エンドポイントと真のエンドポイント(全生存期間の延長)の相関が低いからです。
腫瘍が縮小したり、増悪するまでの期間が延びても、抗がん剤の副作用が強いために、全生存期間が延びないことが明らかになっています。
もう一つの理由は、前述した「臨床試験の対象は患者全体を代表していない」点です。
臨床試験の大多数は、体力があり、がん以外に健康問題はほとんどない、と言った理想的な患者を使って薬を検証しています。
理想的な集団での試験は、治療薬の効果が誇張される可能性があります。
臨床試験で2ヶ月の延命が認められても、高齢者や体力の低下した患者や合併症をもった患者全体で検証すると、意味のある臨床効果が得られない場合も多いのです。
以下のような報告があります。
Assessment of Outcomes Associated With the Use of Newly Approved Oncology Drugs in Medicare Beneficiaries.(メディケア受益者における新たに承認された抗がん剤の使用に関連する転帰の評価)JAMA Netw Open. 2021 Feb; 4(2): e210030.
メディケア(Medicare)は、65才以上の高齢者と65才未満の障害者向けの米国の公的医療保険プログラムです。 米国の65才以上の高齢者のほぼ全員がメディケアに加入しています。
この研究では、最近承認された抗がん剤を投与されている転移を有する進行がんのメディケア患者の実際の結果(有効性)と薬の承認の根拠になった臨床試験の結果と比較しています。
この後ろ向きコホート研究では、29の適応症について米国食品医薬品局(FDA)によって承認された22の抗がん剤について、臨床試験参加者と治療を受けたメディケア患者の間で結果を比較しました。
治療を受けたメディケア患者の治療期間の中央値と全生存期間は、一般的に試験参加者よりも短く、抗がん剤の減量はメディケア患者の間で多く見られました。
具体的には、試験参加者(合計11828人)平均年齢は61.8歳で、メディケア患者の平均年齢は72.7歳でした。
メディケア患者の全生存期間の中央値は、29の適応症のうち28で、臨床試験介入群の患者よりも短かく、その差の中央値はマイナス6.3か月(範囲、-28.7〜2.7か月)でした。
メディケア患者の治療期間の中央値は、利用可能なデータがある27の適応症のうち23で短かく、差の中央値はマイナス1.9か月(範囲、-12.4〜1.4か月)でした。
副作用がでれば投与量を減らします。このように抗がん剤の減量が必要だったのは、臨床試験介入群では3416人中734人(21.5%)でしたが、メディケア患者では1032人中600人(58.1%)でした。
つまり、この結果は、抗がん剤の承認の根拠になった臨床試験の結果は、メディケア加入者のような高齢集団には適用できないことを示唆しています。
医療は、基本的には「臨床試験のエビデンス」に基づいて行われています。臨床試験のエビデンスに基づいて治療のガイドラインが作成され、これが標準治療として確立され、患者の治療に使われています。
日本の厚生労働省や米国の食品医薬品局や欧州医薬品庁など世界各国で新薬を承認する規制機関は、有効な薬だけを市場に出していると、私たちは信じています。
しかし実際は、これらの規制機関が承認している薬の中には、生存に関する有効性が証明されていない薬、臨床的に意味のある有用性が認められない薬が多いことが指摘されています。
特に高齢者の場合は、「臨床試験のエビデンス」は当てはまらないことが多いと言えます。
【抗がん剤は生存期間を長くすることを目標にすると、毒性が強くなる傾向がある】
最近は、以前よりも抗がん剤による副作用に苦しむがん患者さんが増えているように思います。20年くらい前は抗がん剤の種類も少なく、がん治療をする医師も抗がん剤治療の専門性が低かったため、効果が無いと諦めが早く、比較的早く匙を投げる印象がありました。
最近は、抗がん剤の種類も増え、抗がん剤治療を専門にする腫瘍内科医が増えたために、かなり無謀な抗がん剤治療を長期に渡って実施する例が増えています。
副作用が強いので抗がん剤治療をやめたいと主治医に相談しても、主治医から治療の継続を主張されて断れないので困っているというような相談が最近増えています。抗がん剤専門の腫瘍内科医のいる病院ほど、この傾向が強いと思っています。
腫瘍内科医が抗がん剤治療以外の治療法の選択肢を示さないことが問題だと思います。むしろ、抗がん剤以外の選択肢を否定する傾向にあります。ガイドラインに記載されていないものははっきりと否定します。
私が専門に行っているがんの食事療法や漢方治療やサプリメントや再利用薬を用いた治療は、10年以上前までは比較的受け入れてくれる医師が多かったのですが、最近は積極的に否定します。抗がん剤治療を専門とする腫瘍内科医は、抗がん剤以外の選択肢を認めないからです。
問題は新薬が必ずしも有用とは言えないことです。無増悪生存期間は伸びても、全生存期間は伸びない抗がん剤が多く使われています。3ヶ月程度の延命に、副作用が極めて強い抗がん剤が使用されています。
生存期間の延長の引き換えに毒性(副作用)が強くなることは抗がん剤治療においては多く経験されます。以下のような報告があります。
The Price We Pay for Progress: A Meta-Analysis of Harms of Newly Approved Anticancer Drugs(進歩の対価:新たに承認された抗がん剤の有害性のメタ分析)J Clin Oncol. 2012 Aug 20;30(24):3012-9
【要旨の抜粋】
目的:新しい抗がん剤の承認は、ランダム化比較試験によって、それまでの標準治療と比較して有効性が向上している結果を示すことが必要である。この際、毒性(副作用)に関してはあまり重視されていない。新たに承認された抗がん剤の毒性を分析する。
患者と方法:2000年から2010年の間に米国食品医薬品局(FDA)によって承認された固形腫瘍の治療薬を評価するランダム化比較試験を特定した。安全性と忍容性の3つのエンドポイント(治療に関連する死亡、毒性に関連する治療中止、グレード3または4の有害事象)について検討した。
結果:38 件のランダム化試験が分析された。対照群と比較して、毒性による死亡のオッズ比(OR)は新しい薬剤の方が高かった(OR、1.40; 95%CI、1.15〜1.70; P <.001)。毒性による治療中止のオッズ比も同様に新しい薬剤の方が高かった(OR、1.33; 95%CI、 1.22〜1.45、P <.001)。
グレード3または4の有害事象のオッズ比(OR、1.52; 95%CI、1.35〜1. 71; P <.001)も、新薬の方が高く、特に下痢、皮膚反応、神経障害などの非血液学的有害事象で発現が高かった。安全性エンドポイントと全生存期間または無進行生存期間の間に有意な相関関係は認めなかった。
結論:全生存期間や無増悪生存期間というエンドポイントの改善につながる新しい抗がん剤は、有害事象(副作用)の発生率と治療関連の死亡率も増加させる。
新薬の多くは、全生存期間や無増悪生存期間は延長しても、有害事象(副作用)の発生率と治療関連の死亡率も増加させているという論文です。
つまり、抗がん剤の新薬は、延命効果と引き換えに、副作用による苦しみも増えているということです。
「The Price We Pay for Progress(進歩に対して我々が支払う対価)」というのは、抗がん剤治療の進歩に我々は副作用の苦しみの増加という代償を支払っているということです。
分子標的薬は当初、通常の抗がん剤のような毒性作用を持たずにがん細胞を特異的に標的とする最適な方法であると考えられていました。しかし残念ながら、これらの新しい抗がん療法が従来の治療法よりも毒性が高いことを示しています。
この論文の研究者らは、「乳がん治療に使われるアロマターゼ阻害剤はタモキシフェン(エストロゲン受容体拮抗薬)よりも特定の重篤な毒性の頻度が高い」ことに気づき、したがって、新薬は古い薬よりも毒性が高いかもしれないという仮説を検証するために研究を開始しました。
彼らの仮説を検証するために、2000年から2010年の間にFDAによって固形腫瘍の治療に承認された新規抗がん剤をそれぞれ評価した38件のランダム化臨床試験を特定しました。安全性と忍容性は、治療に関連する死亡、毒性に関連する治療の中止、およびグレード3または4の有害事象で評価しています。
この研究は、評価されたすべての安全性と毒性のエンドポイントについて、新薬のパフォーマンスが旧薬よりも大幅に悪いことを示しました。彼らの論文記事の中で、著者はこれらの毒性は「進歩のために支払う代償」であると述べています。
【高齢者の抗がん剤治療は死を早める可能性もある】
国立がん研究センターと厚労省、経済産業省が主体となり調査を実施しています。平成19年から20年に同センター中央病院を受診したがん患者約7000人のうち、70歳以上の高齢者約1500人が対象です。
がんの種類別に、抗がん剤による治療を中心に行った場合と、痛みを和らげる「緩和ケア」に重点を置いた場合とで、受診から死亡までの期間(生存期間)を比較しました。
その結果、主に肺がん・大腸がん・乳がんで末期(ステージ4)の高齢患者の場合、抗がん剤治療の有無にかかわらず、生存率は同程度であり、抗がん剤治療が明確な効果を示さない可能性があると言っています。
例えば肺がんの場合、生存期間が40カ月以上のグループは抗がん剤治療を受けなかった患者のみでした。同様に75歳以上で見た場合、10カ月以上生存した人の割合は、抗がん剤治療を受けなかった患者の方が高く、生存期間も長いという結果でした。(下図)

図:ステージ4の肺がんの生存曲線(国立がん研究センター2007年〜2008年)。75歳以上の高齢者では抗がん剤治療が生存率を高めない可能性がある。この解析では、75歳以上では、生存期間が40カ月以上であったのは、抗がん剤治療を受けなかった患者のみであった。(出典:https://www.ncc.go.jp/jp/information/pr_release/2017/0427/index.html)
「抗がん剤治療が明確な効果を示さない可能性がある」と控えめな表現になっていますが、「肺がんの場合、70歳以上では生存期間が40カ月以上のグループは抗がん剤治療を受けなかった患者のみだった。75歳以上では、10カ月以上生存した人の割合は、抗がん剤治療を受けなかった患者の方が高く、生存期間も長かった。」という結果は、「70歳以上の肺がんでは、抗がん剤治療を受けると早く死ぬ」と言っているのと同じです。
将来的に画期的な薬ができて、75歳以上でも副作用が少なく、有効性が高い治療ができれば、75歳以上でも抗がん剤治療を受けるメリットは出てきます。
問題は、現時点の抗がん剤治療は75歳以上には「メリットがない」、あるいは「死を早めている可能性がある」ということです。
現行の抗がん剤治療は、体力と回復力に依存した治療法と言えます。体力と回復力が高い若い人の場合は、副作用に耐えられる分、延命効果は得られます。副作用で苦しんでも少しでも長く生きたければ、若い人は現行の最大耐用量の抗がん剤治療は意味があります。
しかし、体力も回復力も低下している高齢者の場合は、副作用によるデメリットが、抗腫瘍効果によるメリットより大きいので、抗がん剤治療は意味が無いということです。
ただし、体の老化の程度(体力や臓器機能など)は大きな個人差があります。80歳でも肉体年齢が60歳以下のような人もいます。60歳でも多数の併存疾患を持って肉体年齢は80歳以上の人もいます。したがって、年齢だけでは抗がん剤治療を受けるべきかどうかは判断できません。これは、抗がん剤治療に体力や抵抗力を高めることの重要性の根拠です。適切な食事やサプリメントや漢方治療ががん治療に役立つ根拠でもあります。
しかし、西洋医学の標準治療は、体力や抵抗力や免疫力や回復力を高めるという視点も方法論も持っていません。むしろ、そのような補完医療を否定し拒否しています。体の治癒力を認めないことが西洋医学の大きな欠点だと思います。
| « 814)オールト... | 816)ドコサヘ... » |



