がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
560)mTORC1活性を阻害するラパマイシンとメトホルミンとビタミンD3とオーラノフィン
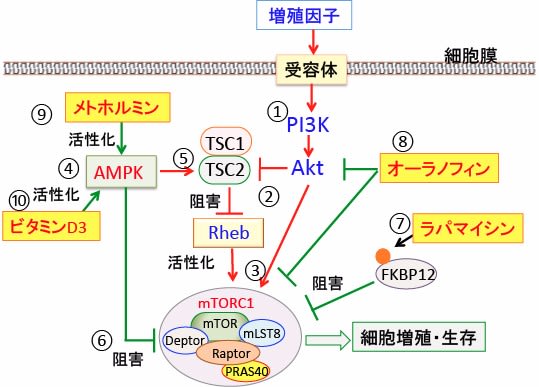
図:インスリンやインスリン様成長因子-1や成長ホルモンなどの増殖因子が細胞の受容体に作用するとPI3キナーゼ(PI3K)というリン酸化酵素が活性化され、これがAktというセリン・スレオニンリン酸化酵素をリン酸化して活性化する(①)。活性化したAktはTSC1/TSC2を阻害してRheb(Ras homolog enriched in brain)を活性し、mTORC1を活性化する(②)。AktはmTORC1を直接活性化する作用もある(③)。メトホルミンとビタミンD3はAMP依存性プロテインキナーゼ(AMPK)を活性化する(④)。活性化したAMPKは、TSC1/TSC2の活性化(⑤)やmTORC1の直接的な作用(⑥)によってmTORC1活性を阻害する。このようにmTORC1とAMPKは栄養状態と増殖シグナルを感知して細胞の増殖や生存を制御している。ラパマイシンはFKBP12(12kDa FK506 binding protein)と結合し、mTORC1の活性を阻害する(⑦)。オーラノフィンはPI3K/Akt/mTORC1経路を阻害する(⑧)。メトホルミン(⑨)とビタミンD3(⑩)はAMPKを活性化する。したがって、これらを組み合せるとTORC1の活性を強く抑制し、がん細胞の増殖を抑制できる。
560)mTORC1活性を阻害するラパマイシンとメトホルミンとビタミンD3とオーラノフィン
【がん細胞が増殖するには栄養とエネルギーが必要】
正常細胞は増殖や細胞死が厳密に制御されていて、無制限に増殖することはありません。
がん細胞は、遺伝子の変異や発現異常によって細胞周期やアポトーシス(細胞死)の制御に異常が起こって、無制限な自律増殖能を獲得しています。
がん細胞は栄養が十分に供給されれば、無制限に増殖できます。増殖を促進するために、がん細胞はグルコースやアミノ酸の取込みと消費が増加しています。
がん細胞が増殖するための2大栄養素はグルコースとグルタミンです。がん細胞では、グルコースとグルタミンの取込みが増えています。細胞の増殖を維持するために、物質合成とエネルギー産生のための栄養源が必要だからです。

図:増殖活性の高いがん細胞はグルコース(ブドウ糖)とグルタミンの取込みと代謝が亢進している。
栄養やエネルギーの供給が減少すれば増殖速度は低下し、栄養やエネルギーの供給が停止すれば細胞は増殖できません。栄養源の取込みを促進し、細胞の増殖を亢進する働きを担っているのが、哺乳類ラパマイシン標的タンパク質複合体1(mTORC1)です。mTORC1の活性を阻害すれば、がん細胞の増殖は抑制できます。
【ラパマイシンは哺乳類ラパマイシン標的タンパク質複合体1(mTORC1)を阻害する】
ラパマイシン(Rapamycin)は1970年代にイースター島(モアイ像で有名な南太平洋の島)の土壌から発見されたStreptomyces hygroscopicsという放線菌の一種が産生する有機化合物です。シロリムス(Sirolimus)という別名で呼ばれることもあります。
ラパマイシンは免疫抑制作用があり、米国では臓器移植の際の拒絶反応を防ぐために使用されています。さらに、平滑筋細胞増殖抑制作用や抗がん作用や寿命延長効果が知られています。
平滑筋細胞増殖抑制作用に関しては、狭心症や心筋梗塞の治療に使われる血管内ステントに冠動脈再狭窄予防効果を目的としてラパマイシンを配合したステントが製品化され、心臓カテーテル治療において使用されています。また、リンパ脈管筋腫症の治療薬としても使用されています。
ラパマイシンの生体内のターゲット分子が、哺乳類ラパマイシン標的タンパク質(mammalian target of rapamycin)、略してmTOR(エムトール)というタンパク質です。
mTORはラパマイシンの標的分子として同定されたセリン・スレオニンキナーゼ(タンパク質のセリンやスレオニンをリン酸化する酵素)で、細胞の分裂や生存などの調節に中心的な役割を果たすと考えられています。
酵母におけるラパマイシンの標的タンパク質が見出されてTOR(target of rapamycin)と命名され、後に哺乳類のホモログ(相同体)が見出されてmTOR(哺乳類ラパマイシン標的タンパク質)と命名されました。
mTORにはmTOR複合体1(mTORC1)とmTOR複合体2(mTORC2)の2種類があります。mTORに幾つかの他のタンパク質が結合して複合体を形成しますが、結合しているタンパク質の違いで2種類の複合体ができ、異なる機能を担っています。
mTORC1は成長因子や、糖やアミノ酸などを含む栄養素のセンサーとして機能し、mTORC2は細胞骨格やシグナル伝達の制御をしています。インスリンやインスリン様成長因子(IGF-1)によって活性化されるのはmTORC1の方です。ラパマイシンで阻害されるのもmTORC1の方です。
ラパマイシンは単独でTOR 活性を阻害するのではなく、細胞内でFKBP12(12kDa FK506 binding protein)と結合し,このFKBP12-ラパマイシン複合体がTOR に結合してTOR 活性を阻害します。

図:哺乳類ラパマイシン標的タンパク質複合体1(mTORC1)は複数のタンパク質から構成されるセリン・スレオニン・リン酸化酵素で、インスリンやインスリン様成長因子-1(IGF-1)や上皮成長因子(EGF)や血小板由来増殖因子(PDGF)などの増殖因子によって活性化される。
mTORC1はタンパク質翻訳の開始因子であるelF4Eを抑制する4E結合タンパク質(4E-BP1)をリン酸化してその機能を抑制する。また、リボソームの生合成を促進するS6K1をリン酸化して活性化する。これらの作用によってmTORC1はタンパク質合成を促進する。その他、多くの標的タンパク質をリン酸化することによって脂質や核酸の合成を亢進し、細胞内小器官の消化・再利用に重要なオートファジーを抑制する。ラパマイシンはFKBP12と結合し、mTORとraptorの相互作用を阻害することによってmTORC1の活性を阻害する。
【mTORC1とAMPKは栄養と増殖シグナルとエネルギー量を感知して増殖を制御する】
細胞の増殖というのは、栄養とエネルギーが利用できる状態にあるときに、新たな細胞構成成分(タンパク質、核酸、脂質など)を合成して、細胞の数を増やす生化学的プロセスのことです。
したがって、増殖するためには、細胞を新たに作る材料(栄養素)とエネルギー(糖質や脂質を酸化して得られるATP)が必要です。増殖因子や成長因子やホルモンなどによって細胞増殖の指令(シグナル)が来たときに、栄養素とエネルギーの供給が十分にある条件で、タンパク質や脂質の合成を促進して細胞増殖を実行するのが哺乳類ラパマイシン標的タンパク質(mTORC1)です。
インスリン、インスリン様成長因子-1(IGF-1)、成長ホルモンなどの増殖刺激が細胞に作用すると、それらの受容体を介してPI3キナーゼ(PI3K)というリン酸化酵素が活性化され、これがAktというセリン・スレオニンリン酸化酵素をリン酸化して活性化します。
活性化したAktは、細胞内のシグナル伝達に関与する様々な蛋白質の活性を調節することによって細胞の増殖や生存(あるいは死)の調節を行います。このAktのターゲットの一つがmTORC1です。
AKTは結節性硬化症(Tuberous Sclerosis:TSC)の原因遺伝子産物であるTSC1/TSC2複合体のTSC2をリン酸化して活性を低下させ、低分子 GTPaseの一種である Rheb (Ras Homolog enriched in Brain)の活性を高めます。活性化したRhebは mTOR のキナーゼ触媒ドメインに直接結合してmTORC1のキナーゼ活性を高めます。
アミノ酸は別の経路でmTORC1の活性を高めます。mTORC1の活性化においてアミノ酸(哺乳類では特にロイシン)が必須であり、これはアミノ酸が十分である場合に限り細胞がタンパク合成を開始できる仕組みと言えます。
このようにして、栄養源と増殖シグナルを感知して細胞の成長や分裂を促進するのがmTORC1です。
一方、細胞内のエネルギー低下を感知するのがAMP依存性プロテインキナーゼ (AMPK)です。グルコース欠乏や低酸素などにより細胞内ATP 量が減少すると、AMP/ATP 比の増加に伴いAMPKが活性化されます。AMPKはmTORC1活性を抑制して、異化作用の亢進や細胞成長の停止をもたらし、エネルギー消費の抑制(同化抑制)とエネルギー産生の亢進(異化促進)へと細胞の代謝をシフトさせます。

図:AMPKは触媒作用を持つαサブユニットと、調節作用を持つβサブユットとγサブユニットから構成されるヘテロ三量体として存在する(①)。運動やカロリー制限や虚血や低酸素などによってATPが減少してAMP/ATP比が上昇すると(②)、γサブユニットに結合していたATPがAMPに置換する(③)。これによってAMPKの構造変化が起こると、LKB1というリン酸化酵素の親和性が高まり、αサブユニットのスレオニン172がリン酸化されると、さらにAMPKの活性が高まる(④)。活性化したAMPKは異化を亢進してエネルギー産生を亢進し、物質合成を抑制するように代謝をシフトする(⑤)。活性化したAMPKはmTORC1(哺乳類ラパマイシン標的タンパク質複合体1)を阻害し、がん細胞の増殖抑制や、抗老化や寿命延長の効果を引き起こす。
AMPKはメトホルミンやビタミンD3で活性化できます(下図)。

図:AMPKの172番目のスレオニン(Thr-172)がリン酸化されるとAMPKは最大に活性化される。Thr-172をリン酸化する酵素にはLKB1とカルモジュリンキナーゼキナーゼβ (CaMKKβ)がある。メトホルミンはミトコンドリアの呼吸鎖を阻害してATP産生を低下させる機序とLKB1を活性化する両方の機序でAMPKを活性化する。ビタミンD3は細胞内のフリーのカルシウムを増加させ、カルモジュリンキナーゼキナーゼβ (CaMKKβ)を活性化させてAMPK活性を亢進する。
AMPKはTSC2のリン酸化(活性化)によるmTORC1の間接的な抑制と、mTORC1構成ユニットのRaptorのリン酸化による直接的な阻害のメカニズムでmTORC1活性を低下させ、細胞の増殖を抑制します。
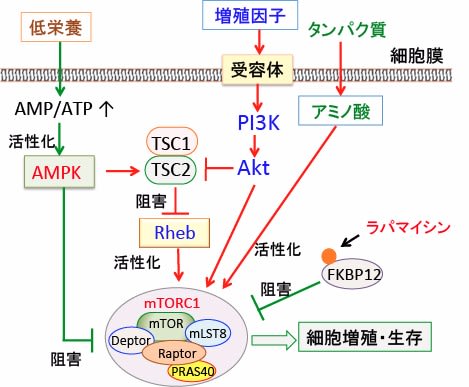
図:インスリンやインスリン様成長因子-1や成長ホルモンなどの増殖刺激が細胞に作用すると、それらの受容体を介してPI3キナーゼ(PI3K)というリン酸化酵素が活性化され、これがAktというセリン・スレオニンリン酸化酵素をリン酸化して活性化する。活性化したAktはTSC1/TSC2を阻害してRheb(Ras homolog enriched in brain)を活性し、mTORC1を活性化する。低栄養の場合は、ATPの産生が低下してAMP/ATP比が上昇し、AMP依存性プロテインキナーゼ(AMPK)が活性化される。AMPKは、TSC1/TSC2の活性化やmTORC1の直接的な作用によってmTORC1活性を抑制する。このようにmTORC1とAMPKは栄養状態と増殖シグナルを感知して細胞の増殖や生存を制御している。ラパマイシンはFKBP12と結合し、mTORC1の活性を阻害する。
【オーラノフィンはPI3K/AKT/mTOR経路を阻害する】
オーラノフィン(Auranofin)は、関節リュウマチにおける炎症反応や免疫異常を抑制して寛解へと導く経口金製剤として1985年以降臨床で使用されています。炎症細胞の機能抑制や、免疫細胞に作用して自己抗体の産生を抑制して、関節における炎症を抑制します。
最近、オーラノフィンの抗腫瘍効果が注目されています。米国ではがん治療へのオーラノフィンの効果を検討する第2相臨床試験の実施がFDA(食品医薬品局)から承認されています。
今まで報告されたオーラノフィンの抗がん作用のメカニズムは多様です。DNAやRNAやタンパク質の合成阻害、ミトコンドリアのチオレドキシン還元酵素やグルタチオン-S-トランスフェラーゼやプロテアソームの機能阻害、抗炎症作用(IL-6/STAT3経路の阻害、NF-κB活性化の阻害など)、ヒストン・アセチル化亢進など多くの作用機序が報告されています(オーラノフィンの抗がん作用の詳細はこちらへ)。
オーラノフィンがPI3K/AKT/mTOR経路を阻害して抗がん作用を発揮するメカニズムも報告されています。以下のような報告があります。
Auranofin-mediated inhibition of PI3K/AKT/mTOR axis and anticancer activity in non-small cell lung cancer cells(非小細胞性肺がんにおけるオーラノフィンによるPI3K/AKT/mTOR経路の阻害と抗腫瘍活性)Oncotarget. 2016 Jan 19; 7(3): 3548–3558.
【要旨】
オーラノフィンは慢性関節リュウマチの治療に使われている金複合体で、安全性が高く、さらに近年、白血病や固形がんに対する治療効果が検討されている。
しかしながら、肺がんに対するオーラノフィン単独の抗腫瘍効果については十分に検討されていない。
肺がんに対してオーラノフィンが単独で抗腫瘍活性を示すかどうかを検討する目的で、10種類の非小細胞性肺がん細胞株を用いてオーラノフィンの抗腫瘍活性を検討した。その結果、オーラノフィンは非小細胞性肺がん細胞に対して、増殖抑制効果を示し、その50%増殖阻止濃度(IC50)は最大で1.0μMであった。
オーラノフィンに感受性の肺がん細胞に対して、オーラノフィンは細胞死(アポトーシス)を誘導した。
さらに、肺がん細胞のオーラノフィンに対する感受性はTXNRD1発現と逆相関を認めた。
TXNRD1を発現するプラスミドを一過性に発現させると、オーラノフィン感受性のCalu3細胞はオーラノフィンに抵抗性を示すように変化した。これはTXNRDの高発現がオーラノフィンに対する抵抗性の因子の一つであることを示している。
さらにメカニズムの検討によって、S6、 4EBP1、 Rictor、 p70S6K、 mTOR、 TSC2、 AKT 、GSK3などを含むPI3K/AKT/mTOR経路の多くのタンパク質の発現とリン酸化を阻害することが明らかになった。このようなオーラノフィンによるPI3K/AKT/mTOR経路の阻害はTXNRD1の一過性の発現によって阻止された。これはPI3K/AKT/mTOR経路の制御にTXNRD1が関与している可能性を示唆している。
肺がんを移植したマウスにオーラノフィンを投与すると明らかな毒性(副作用)を示すことなく、腫瘍の増大が顕著に抑制された。これらの結果は、肺がん治療にオーラノフィンを使用する根拠を提示している。
TXNRD1というのはチオレドキシン還元酵素1(Thioredoxin reductase 1)のことです。
オーラノフィンはチオレドキシン還元酵素を阻害する作用があります。
チオレドキシン還元酵素はPI3K/AKT/mTOR経路の制御(活性化)に関与しており、チオレドキシン還元酵素の阻害剤のオーラノフィンがPI3K/AKT/mTOR経路を阻害するというメカニズムです。
【栄養飢餓になるとmTORC1が不活性化されてオートファジーが亢進する】
オートファジー(Autophagy)という用語はギリシャ語の「自分」(オート;auto)と「食べる」(ファジー:phagy)を組み合わせた用語で、文字通り、「自分を食べる」という意味を持ちます。オートファジーは、私たちの細胞の中で起こっている大規模な分解作用のことで、日本語では「自食作用」と訳されています。栄養が枯渇したときに、自分の細胞を分解して栄養源にしています。
細胞丸ごと食べてしまうようなものではなく、細胞内の一部を少しづつ分解する細胞内のリサイクルのようなものです。例えば、私たちは食事から1日50~100グラム程度のタンパク質を食べています。一方、私たちの体内では、1日に200グラム程度の自分のタンパク質をアミノ酸に分解し、それに相当するタンパク質を合成しています。つまり、口から食べているタンパク質より、ずっと多い量の自分のタンパク質を食べているのです。
インスリンとアミノ酸はオートファジーを抑制します。前述のようにインスリンとアミノ酸はmTORC1を活性化し、mTORC1はオートファジーを抑制するからです。
栄養が過剰にあるとmTORC1が活性化されて、細胞の増殖が促進され、オートファジーは抑制されます。反対に、飢餓になるとmTORC1が不活性化されてオートファジーが誘導されます。TOR阻害剤のラパマイシンは周囲の栄養状態とは無関係にオートファジーを起こします。
オートファジーが抑制されると腫瘍が発生しやすくなります。これは、細胞内に異常タンパク質や不良ミトコンドリアが蓄積することが引き金になると考えられています。また、mTORC1の活性化は酸化ストレスを高めます。つまり、インスリンやアミノ酸の過剰摂取によってmTORC1が活性化されることは、体の成長促進や筋肉増強には効果があるのですが、オートファジーの抑制や酸化ストレスの亢進によって細胞の老化とがん化を促進することになります。
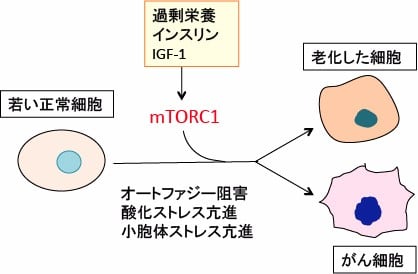
図:栄養素やインスリンによって活性化されるmTORC1はオートファジーの抑制や酸化ストレスの亢進によって細胞の老化とがん化を促進する
一時的飢餓あるいは軽度の飢餓はオートファジー亢進を通じて細胞内をきれいにして、細胞を若返らせる効果があり、さらにがんを予防することもできます。カロリー制限は完全な絶食ではなく、普通の食事の60%程度のカロリーに抑えるのですが、この程度の弱い飢餓でもオートファジーが誘導されます。
線虫の研究では、カロリーを制限しなくても、カロリー摂取で応答するインスリンの信号伝達系に欠陥がある変異体は普通にエサを食べていても長生きすることが明らかになっています。インスリンはオートファジーの抑制因子であり、インスリン信号伝達に異常があるとやはりオートファジーが亢進するのです。このようにがん予防と寿命延長とインスリンシ・グナル伝達系とオートファジーは密接に関連しています。
【カロリー制限とラパマイシンは老化を遅延させて寿命を延ばす】
寿命を延ばす方法として現時点で最も確実なのがカロリー制限です。カロリー制限とは、栄養障害(ビタミンやミネラルやタンパク質の不足)を起こさずに食事からの摂取カロリーを30~40%程度減らす食事を行うことです。カロリー制限には老化を遅延して寿命を延ばし、がんを含めて老化関連疾患の発症を抑制する効果が認められています。
細胞の増殖と老化の制御で重要な役割を担っているのが、mTORC1(哺乳類ラパマイシン標的タンパク質複合体1)という細胞内タンパク質です。
mTORC1はインスリンや成長ホルモンやインスリン様成長因子-1(IGF-1)などの様々な成長因子や過剰な栄養によって活性化され、タンパク質や脂肪の合成を促進し、細胞の増殖や体の成長を促進する作用があります。増殖や成長を促進する作用は老化過程も促進します。老化は成長の延長だからです(図)。
カロリー制限がmTORC1の活性を低下させることによって老化過程を遅延させ、寿命を延ばし、がんを予防することを示す証拠が多く報告されています。mTORC1の阻害剤であるラパマイシンも抗老化と寿命延長とがん予防効果が明らかになっています。
糖尿病治療薬のメトホルミンもAMPK活性化とmTORC1阻害作用のメカニズムで寿命延長効果とがん予防効果を発揮します。
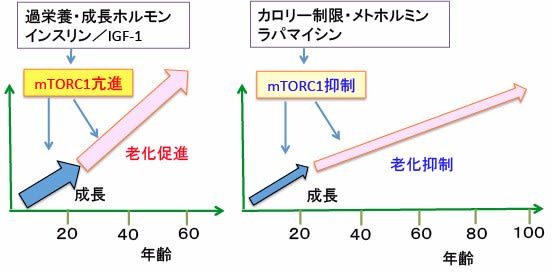
図: mTORC1(哺乳類ラパマイシン標的タンパク質複合体1)は、成長ホルモンやインスリンやインスリン様成長因子-1(IGF-1)などの成長因子や過剰な栄養によって活性化され、細胞の増殖や体の成長を促進する。成長が終了したあともmTORC1の働きが過剰に続くと、細胞や組織の老化が促進される。成長終了後はmTORC1の活性は老化を促進し寿命を短くする(左図)。カロリー制限やメトホルミンやラパマイシンはmTORC1活性を抑制し、老化速度を遅延させ、寿命を延ばす(右図)。
サルにラパマイシンを投与するとがんや糖尿病などの様々な成人病が予防されるという報告があります。ラパマイシンはオートファジーを誘導します。カロリー制限による寿命延長において、オートファジーを誘導することが部分的に貢献していることが明らかになっています。インスリン・シグナルに変異をもつ線虫は長寿命になりますが、同時にオートファジー遺伝子に変異をもつと寿命延長効果は打ち消されるという報告があります。
週1回食事を摂らず水分のみをとる、いわゆるプチ断食という食事療法がありますが、線虫の研究から、断続的なカロリー制限でも寿命延長効果があることが示されています。
近年、このmTORシグナル伝達系の仕組みが次第に明らかになり、細胞の増殖や老化に重要な役割を果たしていることが認められるようになってきました。
いろんな成長因子や栄養素(アミノ酸など)は成長過程においてはmTORC1の働きによって体が成長し成熟していく上で重要な働きを担っていますが、成熟が済むと、成長ホルモンや成長因子やmTORの活性化は細胞や組織の老化を促進する作用になり、さらにがん細胞の発生や増殖や進展を促進することに加担しています。
これは、生殖の終わった個体を早く排除した方が種の繁栄にはメリットがあるので、遺伝子はこの方針が正しいと考えています。
もし遺伝子の思惑に反して寿命を延ばしたければ、成長が終了した後は、むやみにmTORC1シグナル伝達系を活性化しない方が有利になります。後者は不老不死を願う脳の思惑です。
【ビタミンD3はmTORC1の活性を阻害する】
ビタミンDは、血清カルシウム濃度の恒常性や骨代謝における作用が主な働きだと考えられていますが、最近の研究によって、細胞の増殖や分化や細胞死(アポトーシス)や免疫機能など多彩な生理活性の制御に重要な役割を担っていることが明らかになっています。
ビタミンD3がmTORC1(mammalian target of rapamycin complex 1:哺乳類ラパマイシン標的蛋白質複合体1)の活性を抑制する作用も報告されています。
前述のように、ビタミンD3はカルモジュリンキナーゼキナーゼβ (CaMKKβ)を活性化させてAMPK活性を亢進するメカニズムが報告されています。
さらに、活性型ビタミンD3(1,25(OH)2ビタミンD3)がビタミンD受容体を介するメカニズムでDDIT4(DNA-damage-inducible transcript 4)という遺伝子の発現を亢進し、このDDIT4がTuberous Sclerosis Complex 1/2(TSC1/2)を活性化し、これがRheb(Ras homolog enriched in the brain)を阻害してmTORC1の活性を抑制するという作用機序が報告されています。(下図)
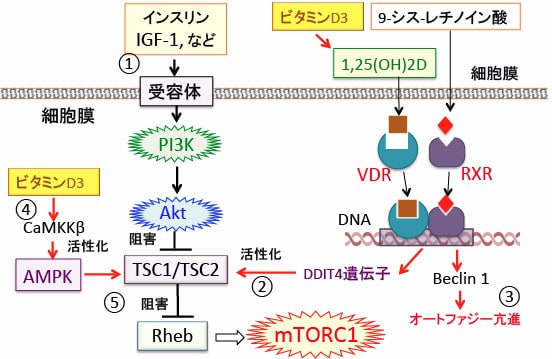
図:インスリンやインスリン様成長因子-1(IGF-1)などの増殖刺激はPI3K/Akt/mTORC1シグナル伝達系を活性化する(①)。ビタミンD3はビタミンD受容体を介する遺伝子転写活性によってDDIT4(DNA-damage-inducible transcript 4)タンパク質の発現を亢進する。このDDIT4はTuberous Sclerosis Complex 1/2(TSC1/2)を活性化し、これがRheb (Ras homolog enriched in the brain)を阻害してmTORC1の活性を抑制する(②)。ビタミンD3はBeclin 1の発現を亢進する。Beclin 1はPI3キナーゼ(PI3K)と相互作用してmTORC1の働きを阻害し、オートファジーを亢進する(③)。ビタミンD3は細胞内のフリーのカルシウム濃度を高めてカルモジュリンキナーゼキナーゼβ (CaMKKβ)を活性化しAMP活性化プロテイン・キナーゼ(AMPK)活性を亢進する(④)。活性化したAMPKはTSC1/TSC2を活性化し、Rhebを阻害してmTORC1の活性を抑制する(⑤)。このようにビタミンD3は複数のメカニズムでmTORC1活性を抑制する。
【ビタミンD3はオートファジーを促進する】
オートファジーは変性したタンパク質や障害をうけた細胞内小器官を除去して細胞における恒常性を維持する役割を担っていいます。
細胞内大規模分解システムであるオートファジーは、細胞成分のリサイクルや飢餓時の栄養源確保に加え、炎症反応、心不全、糖尿病、アルツハイマー病の防止や寿命延長、病原菌の排除、免疫システムの維持など多岐に亘る役割を持つことが最近明らかになってきています。
カロリー制限するとオートファジーが亢進します。mTORC1はオートファジーを抑制するので、mTORC1の阻害剤のラパマイシンはオートファジーを亢進します。
オートファジーの亢進は抗老化作用や寿命延長や抗がん作用の重要なメカニズムと考えられています。
前述のように、ビタミンD3は間接的にmTORC1の活性を抑制します。
さらに、ビタミンD3はbeclin 1というたんぱく質の発現を亢進します。Beclin 1はPI3キナーゼ(PI3K)と相互作用してmTORの働きを阻害し、オートファジーを亢進します。
Beclin 1 は元来 bcl-2 結合タンパク質として同定された因子で,PI3K 複合体を形成してオートファジーに関与しています。また,抗がん作用や抗ウイルス作用を有することも報告されています。
オートファジーは多くのたんぱく質が関与する複雑なプロセスです。オートファジーの様々な段階で、ビタミンD3のシグナル伝達系が関与していることが明らかになっています。炎症や感染症やがん細胞の増殖などに対するビタミンD3の効果にオートファジーの制御が重要な関与をしているようです。
オートファジーの制御におけるビタミンD3の作用として以下のようなメカニズムが報告されています。
1) mTORたんぱく質の発現を抑制してオートファジーを誘導する
2) 細胞内のフリーのカルシウム濃度を高めてmTOR活性を阻害してオートファジーを誘導する
3) Beclin 1に対するBcl-2の阻害作用を抑制することによってオートファジーを誘導する。小胞体のBcl-2を減少させ、カルシウム濃度を高めてオートファジーを誘導する
4) Beclin 1の発現を亢進してオートファジーを誘導する
5) PI3KC3の発現を亢進してオートファジーを誘導する
6) Cathelicidin を増やしてBeclin 1の発現量を増やし、オートファゴゾームとリソソームの融合を促進して、オートファジーを亢進する
7) サイクリン依存性キナーゼ阻害剤のp19INK4Dの発現を抑制してオートファジーを誘導する
(参考:Vitamin D, Vitamin D Receptor, and Macroautophagy in Inflammation and Infection. Discov Med. 2011 Apr; 11(59): 325–335.)
オートファジーのメカニズム自体が複雑でまだ不明な点も多いので、オートファジーに対するビタミンD3の作用もまだ不明な点が多く残っています。しかし、オートファジーを亢進して抗老化や寿命延長を期待する目的ではビタミンD3のサプリメントは有用かもしれません。
ビタミンD3が寿命を延ばすことも大規模疫学研究で明らかになっています。
ビタミンD3は全死因死亡率を低下させることが報告されています。
「ビタミンDの血清濃度が高い人は循環器疾患やがんの死亡率が低く、全死因死亡率も減少する」ことを示すメタ解析の結果が複数の研究グループから報告されています。(394話参照)
ビタミンDに関する多くの研究で、ほぼコンセンサスが得られている点は以下のようにまとめることができます。
1)ビタミンD3には全死因死亡率、心血管系疾患の死亡率、がんの既往のある人のがん死亡率を減らす。(呼吸器疾患による死亡率も減らすことが報告されています。)
2)植物由来のビタミンD2(ergocalciferol)と活性型ビタミンD3のアルファカルシドール(1-ヒドロキシビタミンD3)とカルシトリオール(1,25-ジヒドロキシビタミンD3)には死亡率を低下させる効果は認めない。
3)ビタミンD3にはがんの発生を予防する効果はない(予防効果があるという結果も多く発表されている)。しかし、がんの既往のある人のがん死亡率は低下させる。
がんサバイバー(がんと診断されてから死亡するまでの全てのがん患者)においては、ビタミンDが低いほど死亡率が高くなることが多くの研究で明らかになっています。つまり、がんサバイバーにとってはビタミンD3のサプリメントは有益である可能性が高いと言えます。
ビタミンD3ががんを予防する効果を示す報告もありますが、最近のメタ解析ではがん予防効果はあっても弱いようです。
「全死因死亡率を低下させる」ということは寿命を延ばすことになります。
人間の死亡率は100%です(他の生き物も同じです)。いずれ何らかの原因(病気や老衰や事故など)で必ず死にます。「ビタミンD3が死亡率(mortality)を減らす」というのは、「ある一定期間の死亡確率が低下する」ということです。
血清中のビタミンD濃度が低い下位5分の1のグループの人は、ビタミンD濃度が高い上位5分の1に比べて、死亡確率が1.5倍くらいになるというコホート試験の結果が得られています。
これは、50歳の人が、ビタミンDが不足している場合は余命が20年に対して、ビタミンDの濃度が高ければ余命が30年になるというレベルの差になります
寿命を延ばす最も確実な方法はカロリー制限ですが、このカロリー制限と同じ効果(抗老化や寿命延長効果)を示す薬をCalorie restriction mimetics (CRM:カロリー制限模倣化合物)と言います。
CRMには2-デオキシ-D-グルコース(381話)、D-グルコサミン(387話)、糖尿病治療薬のメトホルミン(384話)、mTORC1阻害剤のラパマイシン(383話)、赤ワインに含まれるレスベラトロール、ポリアミンの一種のスペルミジン、生薬成分のベルベリンなどが知られています。
そして、最近はビタミンD3も寿命を延ばす物質のリストに入っています。
したがって、これらを組み合せれば、相乗的な抗老化作用と寿命延長作用が期待できるかもしれません。また、これらの組合せががん治療において相乗的な抗腫瘍効果を発揮する可能性が報告されています。
老化を促進するメカニズムはがんの発生や進展を促進します。したがって、抗老化(老化抑制)作用と抗がん作用には共通のメカニズムが存在します。この共通のメカニズムを理解すると、抗老化とがん予防を実践できます。
ラパマイシンとメトホルミンとビタミンD3は寿命延長効果があります。オーラノフィンもFOXO3を活性化するので、寿命延長効果が期待できます。つまり、これらは、老化を抑制し寿命を延ばす効果があるがん治療薬と言えます。
通常の毒性の強い抗がん剤は、正常細胞へのダメージによって老化速度を速め、寿命を短くし、2次がんの発生を増やします。腫瘍の縮小だけを目標にして、老化促進と寿命短縮と2次がん発生亢進というデメリットのある治療が最善だとは思えません。
老化とがん発生を抑制し、寿命を延ばすがん治療をもっと検討すべきだと思います。
メトホルミンとオーラノフィンとビタミンD3は非常に安価で安全性が高く、それぞれが多彩なメカニズムで抗がん作用を示します。
メトホルミンやビタミンD3やオーラノフィンは「医薬品の再開発(Drug Repositioning)」として、がん治療に利用すべきエビデンスは十分に存在すると思います。

ビタミンD3のサプリメント:
1カプセル1000 IU/250錠(6300円)
米国:DaVinci Laboratories of Vermont
購入ご希望の方は銀座東京クリニックにお問い合わせください。
画像をクリックするとサイトに移行します。
| « 559)がん細胞... | 561)トリプル... » |





