がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
454)抗腫瘍免疫の増強法(その10):メラトニン
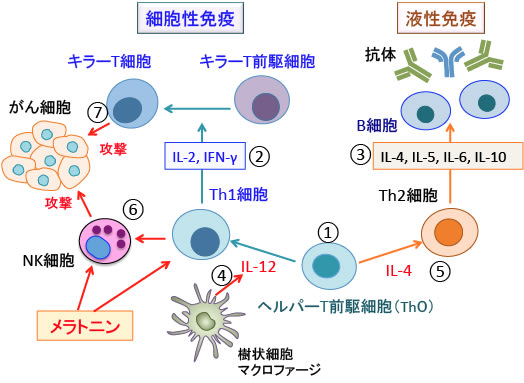
図:①ヘルパーT前駆細胞(Th0)は1型ヘルパーT細胞(Th1)と2型ヘルパーT細胞(Th2)に分化誘導される。 ②Th1細胞はインターフェロン・ガンマ(IFN-γ)や インターロイキン-2(IL-2)を分泌して細胞性免疫に関与し、③Th2細胞はIL-4, IL-5, IL-6, IL-10などを分泌して液性免疫に関与する。④ヘルパーT前駆細胞(Th0)がTh1細胞になるためにはマクロファージや樹状細胞から分泌されるIL-12が必要であり、⑤一方、Th2細胞となるためにはT細胞から分泌されるIL-4が必要とされている。⑥Th1細胞はナチュラルキラー(NK)細胞やキラーT細胞(⑦)を活性化してがん細胞を攻撃する。メラトニンはTh1細胞を活性化してキラーT細胞の働きを高め、さらにナチュラルキラー(NK)細胞を活性化する。
454)抗腫瘍免疫の増強法(その10):メラトニン
【メラトニンは体内時計を制御する】
生体の生理機能は昼夜常に同じ状態を保っているわけではなく、ほぼ1日を周期として変動する概日リズム(サーカディアンリズム)が存在します。
私達の体の中(脳)にはいわゆる『体内時計』があり、昼夜サイクルの時間を刻みながら、体の多くの機能に活動と休息のリズムを与えています。これをサーカディアンリズム(circadian rhythm)と言います。ラテン語で「サーカ」は「約」、「ディアン」は「1日」という意味で、日本語では「概日リズム」と言います。
メラトニンは睡眠を促すホルモンで、脳のほぼ真ん中にある『松果体』と呼ばれる、松かさに似たトウモロコシ1粒くらいの大きさの器官から放出されるホルモンです。
夜暗くなると、メラトニンが松果体から分泌され始め、メラトニンが増えると睡魔が襲ってきます。そして、生体リズムは睡眠や体息に適したものに調整されます。
朝、太陽光線が目に入ると、松果体にその刺激が伝わりメラトニンの分泌が抑制されます。
これによって覚醒スイッチがONとなり、諸々の生体機能は昼間の活動に適応した状態になります。
ところが夜の時間帯に強い光を浴びると、メラトニンの産生が減って寝つきが悪くなります。昼夜サイクルを無視した生活をすると体内時計の調子が狂い、体調を損ねる原因となります。
夜間に光を浴び続けると、メラトニンの分泌が低下し、免疫力が低下し、がんの発生が増えることが報告されています。
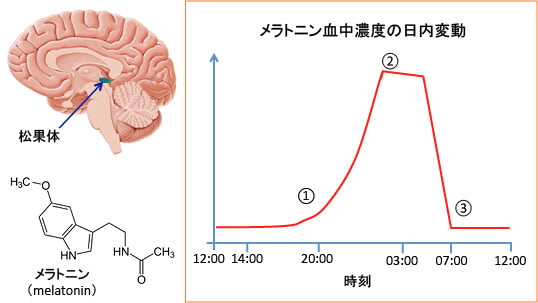
図:メラトニンは脳の松果体から分泌される。①夕方になって暗くなると松果体からメラトニンの産生が始まる。②夜間にメラトニンの血中濃度が上昇し、真夜中(午前2時から4時ころ)にピークに達する。夜間のメラトニンの濃度は日中の5~10倍に達する。③メラトニンは分泌開始から10~12時間で分泌を中止し、急激に血中濃度が低下し、午前7時ころに最低になって覚醒する。
メラトニンの原料は必須アミノ酸のトリプトファンです。トリプトファンに2種類の酵素が働いてセロトニンに変わります(トリプトファン → 5-ヒドロキシトリプトファン → セロトニン)。
セロトニンは神経細胞と神経細胞のつなぎ目(シナプス)で情報伝達の役目をする神経伝達物質の一つです。このセロトニンに2種類の酵素が働いてメラトニンが合成されます(セロトニン → N-アセチルセロトニン → メラトニン)。
メラトニンの化学名はN-アセチル-5-メトキシトリプタミン(N-acetyl-5-methoxytrypamine)です。
セロトニン → メラトニンという段階は、体内時計(視交叉上核)からの指令が来ないとスタートしない仕組みになっています。すなわち、目から入った光の情報は視神経と通って脳にある視交叉上核に伝えられ、さらに神経によって松果体に連絡が入ってメラトニンの合成が制御されます。
メラトニンは松果体から分泌された後、血液に乗って全身に運ばれ、最終的には肝臓で代謝されます。唾液や脳脊髄液、卵巣の卵包液、胆汁中にも移行します。血液脳関門や胎盤も通過します。メラトニンは松果体の他にも、網膜や消化管や皮膚や骨髄からも産生されることが明らかになっています。
【メラトニンは様々な生体機能を調節する】
メラトニンはヒトの体内時計を調節するホルモンとして、快適な睡眠をもたらし、時差ぼけを解消するサプリメントとして評判になりましたが、最近の研究で若返り作用や抗がん作用や免疫増強作用なども報告されています。
メラトニンの分泌異常が不眠や時差ぼけや抑うつ、ストレス、生殖能力、免疫異常やある種のがんの発生と関連している可能性が報告されています。
がんとの関連においては、特に、乳がんとの関連が研究されています。例えば、夜間の電灯が、メラトニンの分泌の低下を引き起こし、乳がんの発症に関与している可能性を指摘する「乳がん発生のメラトニン仮説」も提唱されています。
盲目の人には乳がんが少ないという報告や、夜間勤務の人には乳がんが多いという報告があり、これらはメラトニンが多く分泌される状況にあると乳がんの発生が抑えられ、夜間勤務のようにメラトニンの分泌が抑えられると乳がんが発生しやすい可能性を示唆しています。
実際に、メラトニンの主要代謝産物の6-sulfatoxymelatoninの尿中排泄量が多い人(体内でのメラトニンの産生量が多い)ほど乳がんの発生率が低いことが報告されています。
メラトニンのレベルががんの発生や進展に関与するという報告は乳がん以外にも、前立腺がん、大腸がん、脳腫瘍、子宮体がん、肝臓がんなどで報告されています。
夜勤の多い看護師や、国際線の乗務員のように概日リズムが慢性的に乱れやすい職業の人では、他の職業の人に比べて、乳がんや前立腺がんの発生率が高いことが報告されています。
例えば、乳がんの発生率を検討した疫学研究のメタ解析では、国際線の乗務員では70%、交代制勤務の職種では40%の乳がん発生率の上昇が認められています。前立腺がんに関しては、国際線の乗務員では40%の発生率の上昇が認められています。(Naturwissenschaften 95: 367-382, 2008)
世界保健機関(WHO)の附属組織で人間への発がんリスクの評価を専門に行っている国際がん研究機関(IARC)は、2007年に概日リズムを乱す交代制の仕事(shift-work)を、発がん作用の可能性がある(group 2A)と分類して発表しています。
メラトニンには抗酸化作用や免疫増強作用やその他多くのメカニズムによって抗腫瘍効果を発揮します。
メラトニンの抗腫瘍効果は、多くの臨床試験で確かめられています。
メラトニンは神経ホルモン(neurohormone)や神経免疫調節物質(neuroimmunomodulator)という表現が使われています。つまり、神経伝達物質やホルモンやサイトカインなど様々な生理活性物質の働きに作用して神経系や免疫系を制御する生体応答修飾物質(biological response modifier)としての作用を示し、中枢神経、免疫、内分泌、消化管、心血管、腎臓、骨など多くの生体機能を調節しています。そして、その効果は一般的に抗老化やがん予防の方向で作用します。
メラトニンの産生は加齢とともに分泌量が減少します。60歳以上になると夜間のメラトニンの増加もほとんど認めなくなります。これが、高齢者が感染症やがんの発症を起こしやすくなる理由の一つという意見もあります。
したがって、メラトニンをサプリメントとして補うことは、加齢とともに低下する抗酸化力や免疫監視機構の働きを若いレベルに維持する効果が期待できます。マウスやラットを使った実験では、メラトニンの補充で寿命を延ばせることが報告されています。

図:年齢によるメラトニン分泌量の違いを示している。①新生児はメラトニンの分泌はほとんどないが、②徐々に増加して小児期にピークになる。③思春期を超えるとメラトニン分泌は減少し始める。④中年期には加齢とともにメラトニン分泌量が減少し続ける。⑤60歳を超えるとメラトニンの分泌はごくわずかになる。⑥メラトニンの血中濃度は午前2時から4時くらいをピークに夜間に上昇するが、加齢とともに減少し、60歳以上になると、分泌量は極めて低下する。
【メラトニン受容体はGタンパク質共役型受容体】
メラトニンの多くの作用は、細胞膜に存在するメラトニン受容体を介して起こります。
メラトニン受容体にはMT1とMT2の2種類が知られています。MT1は抗けいれん作用や血管収縮作用などに関与しています。一方、MT2は血管拡張作用に関与しています。その他、受容体を介して、メラトニンは免疫調節作用、心筋保護作用、体重増加を抑制する作用、エストロゲンの作用を阻害する作用など様々な作用を発揮します。
メラトニン受容体はGタンパク質共役型受容体(G protein coupled receptor : 略してGPCR)です。
細胞膜受容体には多くの種類が知られていますが、そのうちもっとも大きなグループを構成しているのがGタンパク質共役型受容体で、α-ヘリックスというらせん構造で親油性の部分が、細胞膜(脂質二重層)を内外に行ったり来たりを7回繰り返しているので「7回膜貫通型受容体」という名称で呼ばれることもあります。
GPCRが活性化されると、細胞内のGタンパク質と呼ばれるタンパク質を介してシグナルを細胞内に伝達するために、「Gタンパク質共役型受容体」という名前がつけられています。
GPCRは多数の種類があって多様な生理機能に関与しているので、既存の医薬品の半数くらいが、何らかの形でGPCRの機能に影響を及ぼすことによって薬理作用を示すと考えられています(434話参照)。
つまり、メラトニン受容体がGタンパク質共役型受容体の一種であるということは、メラトニンが生体機能の調節において重要な役割を担っていることを意味しています。

図:Gタンパク質共役型受容体(GPCR)は細胞膜を7回貫通する特徴的な構造から7回膜貫通型受容体とも呼ばれている。細胞膜を貫通する部分をつなぐ細胞外のループ状の部分にシグナル分子(リガンド)が特異的に結合する鍵穴様の領域が存在する。Gタンパク質は細胞膜の細胞内側に存在し、α、β、γの3つのサブユニットから構成される三量体を形成している。αサブユニットはGTP(グアノシン三リン酸)あるいはGDP(グアノシン二リン酸)のどちらかを結合できる。三量体のGタンパク質はGDPが結合した不活性な状態で細胞膜に存在している。GPCRにリガンドが結合するとGPCRの構造が変化して三量体Gタンパク質のαサブユニットのGDPが外れてGTPが結合する。GTPが結合して活性化状態になったGタンパク質αサブユニットは、受容体(GPCR)やβサブユニットやγサブユニットと解離して、酵素やイオンチャネルなどに作用して、その下流のシグナル伝達経路を活性化する。このようなメカニズムでGPCRは光・匂い・味などの外来の刺激や、神経伝達物質・ホルモン・イオンなどの内因性の刺激を感知し、細胞内に伝達する働きを担っている。
【メラトニンはTh1サイトカインの産生を高める】
松果体と免疫系との関係が最初に指摘されたのは90年前(1926年)です。猫に松果体抽出エキスを投与すると免疫システムが活性化することが報告されています。
1970年代には、マウスの動物実験でメラトニンを産生する松果体を切除すると、胸腺の重量が減少し(130mgから70mgに減少)、胸腺のリンパ球の増殖が停止するなど免疫系の働きが顕著に低下することが報告されています。松果体はメラトニンを産生する器官です。
1980年代後半から、メラトニンが免疫細胞に直接作用することが報告されています。その作用メカニズムは、免疫細胞におけるメラトニン受容体の分布の解析から解明されています。
リンパ球にメラトニン受容体が存在することは1992年に報告されています。胸腺や脾臓やリンパ節など免疫組織においてメラトニン受容体(MT1とMT2)が発現していることが確認されています。
Tリンパ球や単球の表面にメラトニン受容体があり、メラトニンはこの受容体を介してリンパ球や単球を刺激して、インターフェロンγ(IFN-γ)やインターロイキン(IL)1,2,6,12などの免疫反応を増強するサイトカイの分泌を促進する作用があります。これらのサイトカインは1型ヘルパーT細胞(Th1)を増やし、キラーT細胞(細胞傷害性T細胞)による細胞免疫を増強します。
1型ヘルパーT細胞(Th1)とは細胞性免疫を亢進するヘルパーT細胞です。
リンパ球にはB細胞・T細胞・ナチュラルキラー細胞などがあります。
B細胞は抗体を使って細菌やウイルスを攻撃するもので、これを「液性免疫」といいます。IgEという抗体の一種が関与するアレルギー性疾患はこの液性免疫が過剰に反応する結果発生します。
一方、ウイルス感染細胞やがん細胞など自分の細胞に隠れている異常を発見して、Tリンパ球などが直接攻撃する免疫の仕組みを「細胞性免疫」といいます。
この液性免疫と細胞性免疫の制御は2種類のヘルパーT細胞 (Th) のバランスによって決まります。ヘルパーT細胞は、B細胞やT細胞の増殖や働きを調節するタンパク質(サイトカイン)を分泌して、液性免疫と細胞性免疫のバランスを調節しており、そのサイトカインの産生パターンから、Th1(1型ヘルパーT) 細胞とTh2(2型ヘルパーT) 細胞に分類されます。
Th1細胞はインターフェロン・ガンマ(IFN-γ)や インターロイキン-2(IL-2)を分泌して細胞性免疫に関与し、Th2細胞はIL-4, IL-5, IL-6, IL-10などを分泌して液性免疫に関与します。ヘルパーT前駆細胞(Th0)がTh1細胞になるためにはマクロファージや樹状細胞から分泌されるIL-12が必要であり、一方、Th2細胞となるためにはT細胞から分泌されるIL-4が必要とされています。
メラトニンはTh1細胞を活性化して細胞性免疫を増強することが知られています。

がんの発生や再発の予防、治療による副作用軽減においてメラトニンが有効である理由として、免疫増強作用と同時に抗酸化作用の関与が大きいと考えられています。
さらに、抗腫瘍免疫の活性を高める方法を組み合せれば、有効ながん治療法になります。(下図)

| « 453)抗腫瘍免... | 455)内因性カ... » |



