がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
675)カンナビジオールはグリオブラストーマ(膠芽腫)の治療効果を高める
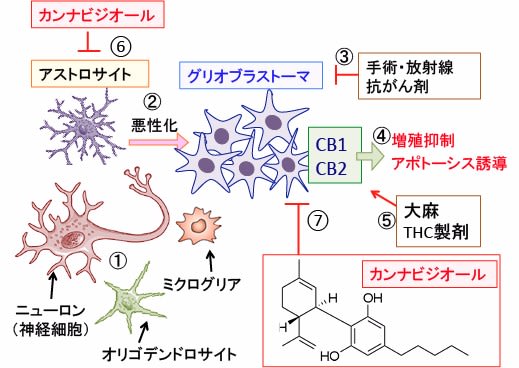
図:神経組織はニューロン(神経細胞)とそれを支えるグリア細胞(アストロサイト、オリゴデンドロサイト、ミクログリア)から構成される(①)。脳腫瘍のグリオブラストーマ(膠芽腫)はアストロサイトが悪性化した腫瘍で(②)、標準治療として手術や放射線治療や抗がん剤治療が行われる(③)。グリオブラストーマにはカンナビノイド受容体のCB1とCB2が発現しており、これらの受容体がリガンドで活性化されると、細胞増殖の抑制とアポトーシス誘導などによって抗腫瘍効果が得られる(④)。大麻草に含まれるΔ9テトラヒドロカンナビノール(THC)はCB1受容体とCB2受容体を介して抗腫瘍活性を示す(⑤)。カンナビジオール(CBD)はカンナビノイド受容体(CB1とCB2)を介さない多彩なメカニズムでアストロサイトの活性を抑制する作用がある(⑥)。同様に、CBDはアストロサイト由来のグリオブラストーマに対して抗腫瘍作用を示す(⑦)。膠芽腫の抗がん剤治療にTHCとCBDを含む大麻抽出エキスを併用すると生存期間を延長できることが報告されている。CBD単独でも有効性が報告されている。
675)カンナビジオールはグリオブラストーマ(膠芽腫)の治療効果を高める
【グリオブラストーマ(膠芽腫)は神経膠細胞から発生する】
脳や脊髄など神経組織には大きくわけて2種類の細胞が含まれています。神経細胞(ニューロン)とそれを支える神経膠細胞(グリア細胞)です。その他に血管を構成する細胞もあります。
ニューロンは感覚や運動などの情報を処理する主体で、そのニューロンに栄養を与え、神経組織を健全に維持するのがグリア細胞の役目です。
「グリア細胞」の日本語訳は「膠細胞」です。
「膠」は事典によると、「獣や魚の皮・骨などを水で煮沸し、その溶液からコラーゲンやゼラチンなどを抽出し、濃縮・冷却し凝固させたもの」とあります。つまり、動物の腱などから作られた接着剤のようなもので、「膠細胞」は神経細胞の間の組織を埋めるような支持組織で不活性が細胞と考えられていました。
しかし、最近の研究でグリア細胞は脳機能やニューロンの制御に重要な役割を持っていることが明らかになっています。
ヒトの場合はグリア細胞の数はニューロンの10倍程度存在します。
グリア細胞は主に3種類あり、アストロサイト、オリゴデンドロサイト、ミクログリアと呼ばれています。
アストロサイト(星状膠細胞)は多数の突起があり、星のように見えることからこの名があります。神経組織の形態維持、血液脳関門、栄養補給、神経伝達物質の輸送などの役割を担っています。
オリゴデンドロサイト(乏突起膠細胞)は神経細胞の軸策に巻き付いて髄鞘の形成や栄養補給の機能を持っています。
ミクログリア(小膠細胞)は骨髄系のマクロファージに由来し、病原菌の排除や死細胞の除去や傷害を受けた神経組織を修復する働きを担っています。アルツハイマー病など神経変性疾患ではミクログリアが炎症の増悪や神経細胞死に関わってきます。
グリオブラストーマ(膠芽腫)はアストロサイト(星状膠細胞)から発生する悪性腫瘍です。(下図)

図:脳組織はニューロン(神経細胞)とグリア細胞(アストロサイト、オリゴデンドロサイト、ミクログリア)と血管組織などから構成される。グリオブラストーマ(膠芽腫)はアストロサイトが悪性化した腫瘍。
【膠芽腫は増殖が早く再発しやすい】
神経膠細胞から発生する腫瘍を神経膠腫(グリオーマ)と言い、神経膠腫の中で最も悪性度の高い腫瘍が膠芽腫(グリオブラストーマ)です。
膠芽腫は増殖活性が高く、進行が早く、ヒトの悪性腫瘍の中で最も予後不良の腫瘍と言われています。
手術や放射線治療や抗がん剤治療などが行われますが、このような集学的治療をおこなっても平均生存期間は12~14カ月程度であり,治療成績はここ30年以上、ほとんど改善がないと言われています。
膠芽腫は周囲の脳組織にしみ込むように広がっていくのが特徴で、腫瘍と正常脳との境界が不鮮明となり、そのため手術によって腫瘍を完全に摘出することは極めて困難です。したがって、手術でできるだけ摘出した後に放射線療法と抗がん剤治療が行われます。
しかし、放射線治療や抗がん剤治療によって生き残るがん細胞がいるため、再発しやすいということです。
このような「放射線治療や抗がん剤治療によって生き残るがん細胞」として「がん幹細胞」の存在が重要と考えられています。
【膠芽腫の標準治療に大麻製剤を併用すると生存期間が延長する】
SativexやEpidiolexなど大麻製剤の研究開発を行っている英国の製薬会社のGW Pharmaceuticalsは多発性硬化症や癲癇(てんかん)や癌(がん)の治療における大麻製剤の臨床試験を行っています。
多発性硬化症に対するSativex(THCとCBDをほぼ1:1で含む大麻抽出エキス)の有効性や、薬剤抵抗性てんかん(Dravet症候群やLennox-Gastaut症候群)に対するEpidiolex(CBD主体の大麻抽出エキス)の有効性はすでに多くの臨床試験で確認され、複数の国で承認されています。
がん患者に対しては、大麻は症状の改善作用や緩和作用が証明されています。すなわち、食欲増進、体重増加、睡眠の改善、抗がん剤治療による吐き気や嘔吐の軽減などの症状の緩和や改善の効果は多くの臨床試験で有効性が示されています。
がん細胞の増殖抑制やアポトーシス誘導などの抗がん作用が培養細胞や動物モデルを用いた研究で示されています。
そこで、大麻製剤(医療大麻や大麻抽出エキス製剤など)の抗がん作用を検討する臨床試験が始まっています。
2017年にはGW社はTHCとCBDを含む大麻製剤が、脳腫瘍(膠芽腫)に対する臨床試験で有効性を認めたと発表しています。
すなわち、再発した多形性膠芽腫(Glioblastoma Multiforme)の患者21人を対象にした探索的第2相プラセボ対照臨床試験によって、テトラヒドロカンナビノール(THC)とカンナビジオール(CBD)を含む大麻抽出エキスの有効性を検討し、有効性を示す結果を得たと発表しています。
再発性神経膠芽腫患者の1年生存率は、対照群が53%、THC:CBD製剤で治療を受けた群が83%で、統計的に有意な差を認めました(p=0.042)。生存期間の中央値は対照群が369日で、THC:CBD群は550日でした。
この臨床試験の結果は、テモゾロマイド治療を受けている膠芽腫の患者にTHCとCBDを含む大麻抽出製剤を併用することによって治療効果を改善できることを示唆しています。(下表)

表:再発した多形性膠芽腫(Glioblastoma Multiforme)の患者21人を対象にした探索的第2相プラセボ対照臨床試験の結果。標準治療にTHC/CBD製剤を併用すると生存率と生存期間の改善が認められた。 (GW Pharmaceuticals, 2017年2月7日発表のプレスリリースより)
【カンナビジオールは膠芽腫患者を延命する】
前述のように膠芽腫の標準治療に大麻製剤を併用すると生存期間が延長するのですが、日本ではまだ医療大麻は使えません。成熟した茎から抽出したCBDオイルであれば、食品扱いで販売されています。
CBD単独でも膠芽腫に対してある程度の効果が期待できるようです。例えば、以下のような報告があります。
Case Report: Clinical Outcome and Image Response of Two Patients With Secondary High-Grade Glioma Treated With Chemoradiation, PCV, and Cannabidiol.(症例報告:化学放射線療法とPCVとカンナビジオールで治療した二次性高悪性度グリオーマ患者2人の臨床転帰および画像所見)Front Oncol. 2019 Jan 18;8:643. doi: 10.3389/fonc.2018.00643. eCollection 2018.
【要旨の抜粋】
今回報告する2人の患者は、O6-メチルグアニン-DNAメチルトランスフェラーゼ(MGMT)メチル化およびイソクエン酸デヒドロゲナーゼ(IDH-1)変異を示す高悪性度神経膠腫(グレードIII / IV)の確定診断を受け、腫瘍の切除の後、化学放射線療法を受け、さらに多剤併用のPCV療法(プロカルバジン、ロムスチン、ビンクリスチン)とカンナビジオールの併用を行なった。
2人の患者は、臨床経過および画像検査による定期的な評価で満足のいく結果を示した。
患者の一人は、化学放射線療法の直後に、一時的な悪化が磁気共鳴画像法(MRI)によって評価されたが、これは短期間で解消された。
もう一人の患者は、MRIで評価した術後スキャンと比較して、腫瘍部位の顕著な改善を示した。
このような結果は、従来の治療法のみで治療された患者では一般的に観察されない。
この観察結果は、神経膠芽腫の化学放射線療法に対する感受性を高めるCBDの潜在的な効果を示唆している。より多くの患者を対象にした臨床試験と、作用機序の研究を進める必要がある。
ブラジルのサンパウロのシリオ・リバネス病院(Sirio Libanes Hospital) の神経腫瘍部門からの報告です。シリオ・リバネス病院はブラジルで最もレベルの高い医療機関の一つです。
二次性高悪性度グリオーマというのは、初めは低悪性度のグリオーマとして診断され、テモゾロミドなどで治療を受けたあとに、二次性に悪性度が高くなって高悪性度のグリオーマになった症例です。
高悪性度のグリオーマは極めて治療に抵抗性で、治癒することは極めて稀です。
そのような治療抵抗性の二次性高悪性度グリオーマに対して、カンナビジオールが顕著な改善を示したという2例の症例報告です。
2名の患者は腫瘍の可能な範囲での切除を受け、そのあとに化学放射線療法を受け、さらに6サイクルの多剤併用のPCV療法(プロカルバジン、ロムスチン、ビンクリスチン)を受け、カンナビジオールの併用を行なっています。
カンナビジオール(CBD)は通常は舌下投与が良いと言われていますが、この研究では50mgのCBDを含有するカプセルを内服しています。
1日量は300mgから450mgです。
服用量は副作用(主に眠気)の出方を基準に決めています。
CBDは多く服用するほど抗腫瘍効果が強まるのですが、服用量が多いと精神機能を抑制的に作用して眠気(drowsiness)が強くなります。つまり、眠気の程度が耐えられるレベルで服用量を決めています。
2例とも2年以上生存しています。1名は2年半後に再発を認めています。
CBDは長期間服用しても血液検査の異常や肝臓や心臓への悪影響は認めなかったと報告しています。
さらに、CBDは抗がん剤の副作用を軽減する効果も多く報告されています。
膠芽腫の標準治療にカンビジオールを併用する根拠は高いと言えます。服用量は1日に300mgから400mg程度ですが、副作用(主に眠気)を目安に服用量を加減すれば、ほとんど問題はないようです。
さらに先月(2019年10月)の論文で、CBDを併用した膠芽腫の9人の患者の症例が報告されています。
Concomitant Treatment of Malignant Brain Tumours With CBD - A Case Series and Review of the Literature.(CBDによる悪性脳腫瘍の併用治療-症例シリーズと文献レビュー)Anticancer Res. 2019 Oct;39(10):5797-5801.
【要旨】
グレードIVの多形膠芽腫は致命的な疾患であり、生存期間の中央値は約14〜16ヶ月である。腫瘍の最大限の切除とそれに続く補助放射線化学療法が長年の治療の主流であったが、生存期間は数ヶ月しか延長されていない。
近年、カンナビノイド、特に精神作用のないカンナビジオールを用いたin vitroおよびin vivoの研究報告が増えており、腫瘍抑制剤としてのカンナビジオールの潜在的な役割を示唆している。
この報告では、連続した合計9人の脳腫瘍患者をケースシリーズとして提示する。
すべての患者は、腫瘍の可能な限りの切除とそれに続く放射線化学療法の標準的な治療に加えて、1日量400 mgのカンナビジオールの投与を受けた。この論文の提出時までに、1人の患者を除いてすべてが生存しており、平均生存期間は22.3か月(範囲= 7〜47か月)である。これは予測される生存期間よりも長い。
オーストリアのクラーゲンフルト病院(Klinikum Klagenfurt am Wörthersee)の麻酔・集中治療科(Department of Anaesthesiology and Intensive Care)と神経科とCIS Clinical Investigation Support GmbHの研究グループからの報告です。
ランダム化試験ではないのですが、最大切除とそれに続く放射線化学療法の標準的な治療にCBD投与を併用すると、顕著な延命効果が認められたという報告です。
グレードIVの多形膠芽腫は致命的な疾患であり、生存期間の中央値は約14〜16ヶ月と報告されていますが、CBDを併用すると、論文の提出時点までに、1人の患者を除くすべての患者がまだ生存しており、平均生存期間は22.3か月(範囲= 7〜47か月)でした。著者らは、これは「予想されるよりも長い」という評価で、CBDの効果を推測しています。
膠芽腫はグリア細胞の1種のアストロサイトが悪性化した腫瘍です。カンナビジオールはアストロサイトの病的な活性化を抑制することによって様々な神経変性疾患やてんかんに対して治療効果を発揮します。
つまり、カンナビジオールによる膠芽腫や神経変性疾患やてんかんに対する作用機序は共通の部分があるようです。
このような研究に対して、ランダム化試験でないから結論が出せないという意見はあります。しかし、このような難治性のがん患者にランダム化試験を行う倫理的問題や、特許が取れない治療薬の経済的サポートがない現状から、ランダム化試験でない臨床試験でも最近は許容される傾向にあるようです。
【カンナビジオールは副作用を引き起さずに抗腫瘍効果を発揮する】
通常の抗がん剤治療は耐え難い副作用を伴うのが欠点であり、問題点です。
カンナビジオールはほとんど副作用を起こさずに抗腫瘍効果を発揮することが報告されています。以下のような報告があります。
Report of Objective Clinical Responses of Cancer Patients to Pharmaceutical-grade Synthetic Cannabidiol.(医薬品グレードの合成カンナビジオールに対するがん患者の客観的な臨床的反応の報告)Anticancer Res. 2018 Oct;38(10):5831-5835. doi: 10.21873/anticanres.12924.
【要旨】
研究の背景と目的:カンナビノイドは、がん患者の疼痛、悪心および悪液質の管理に広く使用されている。 しかしながら、まだ何らかの抗がん活性の客観的臨床的証拠は存在していない。 この研究の目的は、様々ながん患者に対する医薬品グレードの合成カンナビジオールの効果を評価することである。
患者と方法:4年間以上における通常の診療で得た119人のがん患者のデータを解析した。
結果:臨床応答は、固形がん患者の119例のうち92%で見られた。その臨床的反応は、循環腫瘍細胞の減少や、CTスキャンで確認された腫瘍サイズの減少であった。 薬学的グレードの合成カンナビジオールを使用する場合、いかなる種類の副作用も観察されなかった。
結論:医薬品グレードの合成カンナビジオールは、乳がんおよび神経膠腫患者の治療の候補である。
100種類以上存在する大麻のカンナビノイドのうち、精神作用を示すのはテトラヒドロカンナビノール(THC)のみと考えられています。THCに次いで多いカンナビノイドがカンナビジオール(CBD)です。
CBDはがん細胞に対して増殖抑制や細胞死誘導の作用が報告されています。がん細胞の増殖を促進するPI3K/AKT/mTOR や ERKシグナル伝達系を阻害する作用が報告されています。
抗がん剤治療と併用して、抗がん剤の効き目を高める効果も報告されています。
この報告では医薬品グレードのCBDのオイルを、1回10mgを1日2回服用を基本にしています。(1日20mgです)
腫瘍が大きい場合には増量し、1回30mgを1日2回まで増やしています。
一方、腫瘍の増大が抑えられているとき(病状安定)は1回5mgを1日2回に減らしています。
3日間服用して3日間休薬する方法で投与しています。この方が連日の服用より効果が高いと言っています。
副作用は全く認められなかったので、最大耐用量は決定できなかったと考察しています。
他に治療法が無くなったがん患者の治療法として、カンナビジオールはがん細胞の増殖抑制やがんの縮小など、客観的な臨床応答が得られたという報告です。
この論文では、顕著な有効性が認められた症例を紹介しています。
患者は5歳の男児で、退形成性上衣腫(anaplastic ependymoma)という悪性度の高い脳腫瘍でした。2回の手術と抗がん剤治療と放射線治療を受けて、もう治療法が無くなったという段階でCBDのみによる治療が2016年2月に開始されました。2016年12月のCTスキャンでは、腫瘍は60%程度に縮小していました。その後もCBDだけで腫瘍の増大が抑制されたと報告しています。
他の症例は、50歳の進行性のグレード2の上衣腫(tanycytic ependymoma)で2013年6月に診断され、放射線治療が行われて2015年6月に終了しています。抗がん剤治療を拒否し、CBD治療を2016年7月から開始しています。
1回10mgを1日2回のCBD摂取を3日間続けて3日間休むという投与スケジュールです。
この患者はロンドンのクリニックから代替療法としてメトホルミン、メベンダゾール、ドキシサイクリン、アトルバスタチンの投与を受けています。これらとカンビジオールを併用して、腫瘍の縮小が認められています。カンナビジオールの摂取を止めるとがんが増殖しました。
その他に、前立腺がん、乳がん、食道がん、悪性リンパ腫などの腫瘍で、医薬品レベルの合成カンナビジオールの抗腫瘍効果が認められました。
グリオブラストーマなどの脳腫瘍の代替療法として、メトホルミン、メベンダゾール、ドキシサイクリン、スタチン類などに加えて、カンナビジオールの併用は有効だと言えます。
さらに、ニトロキソリン(660話)とイベルメクチン(673話、674話)を併用すると、さらに効果が期待できるように思います。
【CBDの服用法について】
前述の合成カンナビジオールの臨床試験では、1回に10から30mgのCBDを1日2回という投与量です。
天然のCBDを用いた臨床試験では1日300mgから450mgが投与されています。
かなりのギャップがあります。
難治性てんかんの治療では最大で1日に体重1kg当たり20mgまで投与しています。通常は数mg/kgです。
構造が同じであれば普通は有効量は同じはずですが、合成カンナビジオールと天然カンナビジオールでは何かが違うのかもしれません。
がん治療の場合は、服用量が多いほど抗腫瘍効果が高くなりますが、服用量が多いと眠気などの副作用もでてきます。
したがって、眠気が出る量を上限に設定して服用量を決めるのが良いと思います。
通常は1日に体重1kg当り1〜5mg程度が目安になります。副作用がでなければ10mg/kg程度まで増量は可能です。ただし、多く摂取すると経済的に負担になります。少ない量で効き目を高める工夫も大切です。
つまり、体内摂取量を増やす工夫です。
1日に数回に分けて服用します。1回に数十mg分のCBDオイルの服用を1日に2〜4回程度繰り返します。
服用法はCBDオイルを舌下に滴下して、60〜90秒程度飲み込まないでそのまま保持します(下図)。60〜90秒程度口腔内で保持したあとに飲み込みます。これは舌下や口腔粘膜からの方が体内吸収が良いためと、肝臓を通さずに全身循環に行き渡らせるためです。内服して肝臓を最初に通ると、肝臓で多くのCBDが分解されます。
図:CBDオイルの舌下からの服用法:顔を上に向けて、舌の裏にCBDオイルを滴下し、1分間ほど保持したあとに飲み込む。
舌下での服用が困難な場合は、カプセルに入れたり、そのまま服用します。
舌下で服用した場合も、口に残ったものは飲みこみます。
この場合、油の多い食事の後がCBDの吸収が良いことが知られています。以下のような報告があります。
Dietary fats and pharmaceutical lipid excipients increase systemic exposure to orally administered cannabis and cannabis-based medicines(食事からの脂肪および医薬品用脂質賦形剤は経口投与された大麻および大麻由来の医薬品の体内吸収を増加させる)Am J Transl Res. 2016; 8(8): 3448–3459.
【要旨】
近年、大麻(Cannabis sativa)の医療目的での使用への関心が高まっている。大麻は、脂肪を含む食品と一緒に経口投与されるか、脂質ベースの製剤で投与されることが多い。しかしながら、大麻成分への患者の体内吸収に対する脂質の影響は十分に検討されていない。この研究は、2つの主要な活性カンナビノイド、Δ9 - テトラヒドロカンナビノール(THC)とカンナビジオール(CBD)の体内吸収に対する脂質の経口同時投与の効果を解明することを目的とした。
この研究では、脂質の経口同時投与は、脂質を含まない製剤と比較して、ラットのTHCおよびCBDの体内吸収をそれぞれ2.5倍および3倍増強した。
カンナビノイドの腸内での可溶化に対する脂質の影響を調べるために、インビトロでの脂肪分解実験を行った。 脂肪分解後にTHCおよびCBDの30%以上が脂肪のミセル画分に分配された。これは経口投与された量の少なくとも3分の1が、脂質と同時投与することによって消化管からの吸収に利用可能であることを示唆している。
両方のカンナビノイドは、人工のカイロミクロン様粒子、ならびにラットおよびヒトのカイロミクロンに対して非常に高い親和性を示し、腸管のリンパ輸送の高い可能性を示唆している。さらに、ラットおよびヒトのカイロミクロンに対するカンナビノイドの同程度の親和性は、脂質によるカンナビノイドの体内吸収の増加がヒトにおいて起こり得ることを示唆する。
結論として、食事性脂質または医薬用脂質賦形剤の同時投与は、経口投与された大麻および大麻由来医薬品への体内吸収を実質的に増加させる可能性がある。
カンナビノイドへの患者の体内吸収量の増加は、経口投与された大麻または大麻由来医薬品の治療効果に影響を与える可能性があるが、毒性にも影響を与える可能性があるため、臨床的に非常に重要である。
カンナビジオールを服用するとき、油の多い食事の後だと、脂肪がミセルを形成して腸管のリンパ管から吸収されるので、肝臓を通らずに全身に吸収されるということです。
このとき、中鎖脂肪酸(MCTオイル)だとミセルを作らないので、オリーブオイルや亜麻仁油や魚油(脂の乗った魚)や通常の食用油や動物性脂肪と一緒に摂取するのが良いと言うことです。これには長鎖脂肪酸と中鎖脂肪酸の吸収の違いを理解しておく必要があります。(下図)

図:長鎖脂肪酸トリグリセリドと中鎖脂肪酸トリグリセリドの吸収の違い。脂肪はグリセロール(グリセリンともいう)1分子に3分子の脂肪酸が結合した構造をしており、これを中性脂肪(トリグリセリド)と言う。食事から摂取した脂肪は十二指腸や小腸内で膵液中のリパーゼによって加水分解され、トリグリセリド(中性脂肪)から脂肪酸とグリセロールが分離される。グリセロールは水溶性なのでそのまま小腸から毛細血管に吸収される。
脂肪酸は水に不溶性で、胆嚢から十二指腸に分泌される胆汁中に含まれる胆汁酸やホスファチジルコリンやコレステロールによって乳化されたミセルを形成する(①)。ミセルというのは、水になじむ部分(親水基)と油になじむ部分(親油基)をもつ物質が、水の中で親水基を外に親油基を内に向けて球状に会合した粒子(②)。ミセルは水溶性で受動拡散によって消化管粘膜の吸収上皮細胞内に吸収される(③)。
脂肪酸が腸管から吸収されるとき、脂肪酸の大きさ(炭素鎖の長さ)の違いによって代謝のされかたが異なる。炭素数が13以上の長鎖脂肪酸の場合は、腸壁を通り抜けると、腸管粘膜上皮細胞内で再びグリセロールと結合して中性脂肪(トリグリセリド)になり蛋白質などと一緒になってカイロミクロンというリポ蛋白質粒子になる(④)。カイロミクロンはリンパ管から胸管に入り(⑤)、鎖骨下静脈から大循環系に入って全身に運ばれる(⑥)。
炭素数が8~12の中鎖脂肪酸(⑦)は胆汁酸によるミセル化は不要で、小腸吸収細胞に容易に吸収され、分子が小さいことから腸管で毛細血管に吸収され、カイロミクロンを作らずに遊離脂肪酸のまま門脈に入って肝臓へ運ばれ、速やかにエネルギー源となって代謝される(⑧)。
カンナビジオールの薬物動態に関して以下のような総説があります。
A Systematic Review on the Pharmacokinetics of Cannabidiol in Humans.(ヒトにおけるカンナビジオールの薬理学的動態に関する系統的レビュー)Front Pharmacol. 2018 Nov 26;9:1365. doi: 10.3389/fphar.2018.01365. eCollection 2018.
【要旨】
背景:カンナビジオールは経口投与による複数の症状の治療法として利用されている。動物実験では経口摂取によるバイオアベイラビリティー(生体利用性)が低いことが示唆されているが、ヒトでの検討は不十分である。このレビューの目的は、この研究領域で公開されているデータを検討することである。
方法:PubMedおよびEMBASE(MEDLINEを含む)の系統的検索を行い、ヒトにおけるCBDの薬物動態データを報告しているすべての論文を検索した。
結果:検討した792件の論文のうち、24件にはヒトにおけるCBDの薬物動態学的パラメータが含まれていた。カンナビジオールの半減期は、口腔粘膜スプレーによる投与では1.4〜10.9時間、慢性経口投与では2〜5日、静脈内投与では24時間、および喫煙の場合は31時間と報告された。
喫煙による摂取の場合の生体利用率(バイオアベイラビリティー)は31%であったが、静脈内製剤が利用可能であるにもかかわらず、ヒトにおける他の経路による投与法でのCBDのバイオアベイラビリティーの報告は無かった。
血中濃度-時間曲線下面積(AUC)および最高血中濃度(Cmax)は用量依存的に増加し、経口/口腔粘膜経路と比較して喫煙/吸入後より早く到達する。最高血中濃度(Cmax)は食事摂取後および脂質製剤中で増加する。最高血中濃度 到達時間(Tmax)は0から4時間であった。
結論:このレビューは、ヒトにおけるその広範な使用にもかかわらず、カンナビジオールの薬物動態学におけるデータの少なさと、いくつかの食い違いを明らかにした。バイオアベイラビリティおよび半減期などの特性の分析および理解は、将来の治療上の利用において極めて重要であり、さまざまな製剤からの多くのデータが必要とされる。
CBDを高脂肪の食事と一緒に摂取した場合、その生物学的利用能は約4から5倍に増加します。つまり、脂肪の多い食物と一緒にCBDを投与すると、生物学的利用能が最大化され、薬物への全身曝露の日内変動が減少する可能性があります。
つまり、脂肪を多く摂取するケトン食とカンナビジオールは、グリオブラストーマに対して相互に抗腫瘍効果を高めることができます。
舌下投与より、オリーブオイルなどに混ぜて内服する方が勝っている可能性があります。
また、CB2のアゴニストのβカリオフィレンも油に溶けるので、CBDとβカリオフィレンを一緒にオリーブオイルに溶かして服用すると抗腫瘍効果と鎮痛効果を高めることができます。(βカリオフィレンについては663話参照)
また、最大耐用量に関しては、「1日1500mgを4週間投与でも耐えられる」「50mg/kg/dayを3ヶ月間投与も可能」などという報告もあります。臨床試験では1日1000mgや3000mgの投与も、強い副作用は起きないようです。
大量に投与したときの副作用は下痢、吐き気、頭痛、眠気などです。このような副作用が出ない範囲で服用量を決めるのが良いと思います。
【日本におけるカンナビジオール使用と大麻取締法第四条の関連】
大麻取締法は第四条で、大麻の医療使用を禁止しています。該当部分は以下のようになっています。
第四条 何人も次に掲げる行為をしてはならない。
一 大麻を輸入し、又は輸出すること(大麻研究者が、厚生労働大臣の許可を受けて、大麻を輸入し、又は輸出する場合を除く。)。
二 大麻から製造された医薬品を施用し、又は施用のため交付すること。
三 大麻から製造された医薬品の施用を受けること。
そして、『この規定に違反して、大麻から製造された医薬品を施用し、もしくは交付し、又はその施用を受けた者』は五年以下の懲役に処する(第二十四条の三)となっています。
「何人も」と定められているため、患者、医者、研究者であっても、例外なしに大麻を医療目的で使用することはできません。海外で有効性が証明されている疾患でも日本では大麻は使用できません。病気の治療目的であっても大麻を使用すれば、医者も患者も処罰されます。
さて、日本の大麻取締法は大麻草の葉と花穂(花冠)とその製品を禁止していますが、成長した大麻草の茎や種子の使用やそれ由来の製品は除外されています。
すなわち、日本の大麻取締法では「成熟した茎と種子及びその製品が除外される」とあり、成分として規制対象は精神作用のあるテトラヒドロカンナビノール(THC)のみで、カンナビジオールは対象外になっています。THCも化学合成されたものは麻薬取締法で規制されていますが、天然で微量に混入していても規制されていません。
したがって、繊維を取る目的の産業用大麻(Industrial hemp)から抽出した製品は日本でも合法的に使用できることになります。
日本で流通している製品は建前上は「成熟した茎と種子」から抽出したということになっています。そうでなければ通関も流通もできません。
ただし、流通しているCBDオイルの原料が本当に茎からだけかは、かなり疑問だという意見もあります。
実際に、種子にはCBDは検出できず、茎のCBD含有量は極めて微量なので、茎のみからのCBDオイルの製造は経済的に成り立たないというのが、海外のメーカーの常識のようです。
特に米国の製品は、CBD/Hempの原料は「茎と種だけ」からではなく「葉や花を含む」ものがほとんどのようです。そうしないと、価格的に競争できないということです。
もし、CBDオイルの原料に葉や花が少しでも含まれていたら、日本では違法であり、通関できないか、あるいは大麻取締法違反で逮捕されるかもしれません。このような現状で、もしCBDの流通が規制されると、てんかんや神経難病やがんなど多くの患者さんに影響が及びます。その解決法は以下のようなものになります。
1)純粋に茎からだけ抽出した製品を使う。(価格が高くなるデメリットがある)
2)合成のCBDや酵母で産生させたCBDを製品化して使う。(もっとも現実的解決法かもしれない)
3)大麻取締法の第四条を削除するように法律を改正して、医療大麻の使用を許可する。(日本の現状では実現はまだ先か?)
(大麻取締法第四条と人権については478話で考察しています)
新刊紹介:膠芽腫(グリオブラストーマ)の根治を目指す補完・代替医療
本書はプリント・オン・デマンド(Print on Demand)という出版形式で書店では販売していません。アマゾンからの購入になります。
アマゾンからの購入はこちらへ:
| « 674) イベルメ... | 676) Hippo経... » |





