がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
794)ノスカピン(Noscapine)+ドセタキセル+重曹の相乗効果
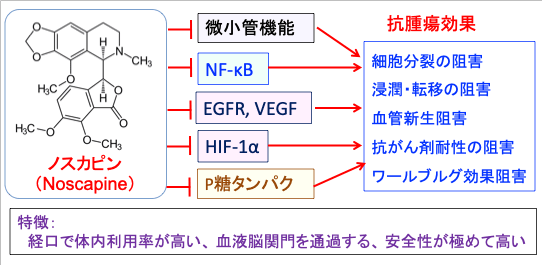
図:ノスカピンは微小管機能、転写因子のNF-κB、上皮成長因子受容体(EGFR)、血管内皮増殖因子(VEGF)、低酸素誘導因子-1α(HIF-1α)、多剤耐性に関与するP糖タンパクなどを阻害する作用がある。その結果、がん細胞の細胞分裂や浸潤・転移、血管新生、抗がん剤耐性、ワールブルグ効果などを阻害するメカニズムで、多彩な抗腫瘍効果を発揮する。さらに、ノスカピンは経口投与で消化管からの吸収が良く体内利用率が高く、血液脳関門を容易に通過し、安全性が極めて高いという特徴を有する。
794)ノスカピン(Noscapine)+ドセタキセル+重曹の相乗効果
【ノスカピンはアヘンに含まれるアルカロイド】
ノスカピン(Noscapine)はモルヒネと同じくけしの液汁(アヘン)に含まれる植物アルカロイド性の成分です。ケシの未熟果実に傷をつけて滲出する乳液を乾燥したものをアヘンと言い、その主成分は麻薬のモルヒネです。アヘンにはモルヒネ以外にも多くのアルカロイドが含まれています。
アヘンから単離された成分としてもっとも古いのがノスカピンです。1803年に単離されています。当時は、アヘンの麻酔・鎮痛作用の成分と考えられて、麻酔睡眠薬を意味するnarcoticからナルコチン(Narcotine)と命名されました。しかし、この成分には麻酔作用や鎮痛作用は無いことが明らかになり、ナルコチンの名称は不適当として、ノスカピンと改称されました。
アヘンに含まれるアルカロイドでは、ノスカピンはモルヒネについで2番目に多く含まれています。

図:ケシの未熟果実に傷をつけて滲出する乳液を乾燥したものをアヘンと言い、アヘンから麻薬のモルヒネや鎮咳薬のノスカピンが見つかった。
モルヒネは強い麻酔・鎮痛作用があり身体的・精神的依存性があるので麻薬に指定されています。
一方、ノスカピンには麻酔・鎮痛作用や依存性は無く、強い鎮咳作用があります。
ノスカピンは脳の咳中枢を抑制することによって鎮咳作用を示しますが、麻薬系の咳止め薬と異なり、呼吸を抑制することなく、また習慣性も無いので、『非麻薬性中枢性鎮咳剤』に分類されている医薬品です。咳止め(鎮咳薬)としては1950年代から多くの国で使用されています。
咳中枢とは脳幹の延髄にある咳のコントロール部で、のどや気管支の刺激を受けて咳を起こさせます。ノスカピンは、この咳中枢を抑えることで速効性の鎮咳作用を発揮します。さらに、気管支のけいれん収縮をおさえて、咳をやわらげ呼吸を楽にします。そのような作用から、かぜを含め上気道炎や気管支炎などによる咳の治療に使用されます。
咳止めの龍角散や、総合感冒薬(パブロンゴールド、新ルルAゴールド、エスタック顆粒など)のような大衆薬にも含まれている極めて安全性の高い薬です。
麻薬作用が無いため、ノスカピンは咳を治療するためのコデインおよびデキストロメトルファン(メジコン)の安全な代替品になります。オランダでは、ノスカピンは小児の咳を治療するための第一選択薬と見なされています。つまり、極めて安全性の高い薬と言えます。
咳止めとして使用される量より多い量のノスカピンを服用すると、がん細胞のアポトーシス誘導や増殖抑制などの抗がん作用があることが報告されています。がんの代替医療において、乳がん、肺がん、前立腺がん、卵巣がん、脳腫瘍、悪性リンパ腫、白血病など多くのがん種に使用されています。
【ノスカピンの抗がん作用】
1958年、米国の国立がん研究所( National Cancer Institute)における培養がん細胞を使った研究で、ノスカピンにがん細胞を殺す作用があることが発見されました。しかし、薬として特許出願するには新しい物質でなければならず、200年以上前から知られているノスカピンでは特許権が取れないため、製薬会社にとっては大きな利益をあげることができないため、がん治療薬としての開発は行われませんでした。
1997年、米国アトランタのエモリー大学の研究者が、ノスカピンには細胞の分裂に重要な役割を果たす微小管の働きを阻害する効果があることを発見し、がん治療薬として再び注目を集めました。
細胞が分裂するときに微小管は重要な役割を担っているため、微小管の働きを阻害する薬が抗がん剤として極めて有効であることが知られていたからです。
細胞の微小管に作用する抗がん剤として、パクリタキセル(商品名タキソール)やドセタキセル(商品名タキソテール)などのタキサン製剤,ビノレルビン(商品名ナベルビン)などのビンカアルカロイド製剤があります。これらの抗がん剤は注射薬ですが、ノスカピンは内服で効果が出るというメリットがあります。
エモリー大学の研究では、ヒトのがん細胞を移植した動物にノスカピンを投与すると、副作用がほとんど出ない量で、3週間で80%も腫瘍が縮小しました。
エモリー大学の研究結果は1998年に発表されましたが、さらにその後の研究では悪性リンパ腫や乳がん、大腸がん、白血病、グリオーマなどの他のがんでも有効性が確認されました。
この研究グループの報告によると、ノスカピンは腎臓や肝臓、心臓、骨髄などの臓器にダメージを与えない量で抗腫瘍作用を示すということです。さらに、免疫抑制作用も認められないと報告されています。血液脳関門を通過するので脳腫瘍にも効果があります。
人間における臨床試験でも、前立腺がんや肺がんなど多くのがんで有効性が示され、毒性が少ないことが報告されています。抗腫瘍効果はシスプラチンよりも高いという報告もあります。また、シスプラチンやドキソルビシンなど他の抗がん剤との併用で、抗がん作用を相乗的に高めるという報告もあります。
図:微小管はαチューブリンとβチューブリンが結合したヘテロ二量体(ヘテロダイマー)を基本単位として構成され(①)、チューブリンのヘテロ二量体が繊維状につながったものをプロトフィラメントと呼び(②)、これが13本集まって管状の構造(直径25nm)を取ったものが微小管となる(③)。細胞分裂が行われる際、細胞の中ではDNAが複製され(④)、複製されたDNAは微小管によって引き寄せられ、分裂後のそれぞれの細胞に分けられる(⑤)。ノスカピンは微小管の働きを阻害し、細胞分裂のM期を停止させてアポトーシスを起こす(⑥)。
【ノスカピンは微小管の働きを阻害するのに副作用が極めて軽い】
微小管は、α-チューブリンとβ-チューブリンのヘテロダイマー(ヘテロ二量体)で構成される非常に動的な構造であり、細胞の移動と細胞内輸送に関与しており、細胞分裂に不可欠です。G2 / M期の細胞分裂において重要な役割を果たすので、微小管は抗がん剤開発の重要なターゲットになっています。
ビンカアルカロイド、パクリタキセル、コンブレタスタチン、コルヒチンなど、さまざまな天然分子が微小管の働きを阻害することが知られています。
これらの微小管標的薬は、チューブリンの重合を阻害するものと、チューブリンの脱重合を阻害する物があり、基本的にチューブリンに結合して、チューブリンの重合反応や脱重合反応を阻害します。微小管阻害剤のチューブリンにおける結合部位が報告されています。

図:チューブリン上の微小管標的化剤の既知の結合部位。(出典:Trends Cell Biol. 2018;28:776–792.)
タキソール誘導体やビンカアルカロイドなどの微小管に作用する薬剤は、様々がんに使用される強力な抗がん剤です。しかしながら、これらの薬物は、末梢神経障害、胃腸毒性、骨髄抑制、免疫抑制などの毒性があります。それにもかかわらず、米国の食品医薬品局(FDA)は1996年に乳がんと卵巣がんのタキソールを承認しました。
ノスカピンは微小管の働きを阻害しますが、他の微小管阻害剤(パクリタキセル、ドセタキセル、ビンカアルカロイドなど)のような末梢神経障害や消化管障害や骨髄抑制などの副作用はほとんど出ません。
細胞分裂するときに必要な微小管の働きを阻害するのであれば、他の抗がん剤と同じような副作用が出ないのは不思議です。その理由として、微小管阻害のターゲット部位がパクリタキセルやドセタキセルやビノレルビンとは異なる点が指摘されています。ノスカピンはチューブリンポリマーの総量には影響せずに、微小管の働きを阻害することが報告されています。
ノスカピンはチューブリンに結合し、微小管が蓄積する能力を破壊することによって細胞周期を破壊します。しかし、ほとんどの抗チューブリン剤とは異なり、ノスカピンは微小管のポリマー量を大幅に変化させることはなく、微小管に深刻な損傷を与えることはありません。代わりに、ノスカピンは微小管の蓄積とダイナミクスに小さな変化を加えることによって作用します。この作用は、微小管のダイナミクスを調節し、がん細胞の有糸分裂を防ぎます。したがって、ノスカピンは、タキソールやビンカアルカロイドなどの抗がん剤とは異なる働きをします。ノスカピンは微小管の配置を変えませんが、微小管のダイナミクスを低下させて有糸分裂を阻害します。
ノスカピンは経口投与で、高い生体利用率を示します。ノスカピンは、体内で急速に経口吸収され、チューブリンに作用する現時点では唯一の薬と言っても過言ではありません。
さらに、ノスカピンには微小管の働きを阻害する以外の抗がん作用もあります。
最近の研究では、ノスカピンには血管新生阻害作用があることが報告されています。
がん細胞が低酸素になると低酸素誘導因子-1α(HIF-1α)という転写因子が活性化され、この転写因子は血管内皮細胞増殖因子(VEGF)の産生を高めます。VEGFは血管を作る増殖因子です。ノスカピンはHIF-1αの活性化を阻害してVEGFの産生を阻害し、血管新生を抑える作用があると報告されています。
また、ノスカピンはブラジキニンという炎症性伝達物質の産生を抑制する作用が報告されています。ブラジキニンは多くのがん細胞の増殖を促進する作用があるので、ブラジキニンの産生阻害作用も抗がん作用のメカニズムと関連していることが示唆されています。
さらに、転写因子のNF-κB活性を阻害する作用があることも報告されています。
このように、ノスカピンの抗がん作用には幾つかの作用メカニズムが働いているようです。その結果、副作用が極めて少ないのに、強い抗がん作用を示すのです。
ノスカピンは、その高い親油性のために、血液脳関門を非常に迅速に通過することができます。そのため膠芽腫などの脳腫瘍にも有効です。
【ノスカピンはドセタキセル耐性を阻止する】
以下のような報告があります。ノスカピンがトリプル・ネガティブ乳がん細胞のドセタキセルの効果を高めるという報告です。
Reversal of drug-resistance by noscapine chemo-sensitization in docetaxel resistant triple negative breast cancer. (ドセタキセル耐性のトリプル・ネガティブ乳がん細胞におけるノスカピンによる抗がん剤感受性増強による薬剤耐性の正常化。)Sci Rep. 2017; 7: 15824.
【要旨の抜粋】
多剤耐性はがん治療の大きな障害である。この研究では、トリプルネガティブ乳がんの薬物耐性を克服するために、ドセタキセルと組み合わせた低濃度のノスカピンの化学増感効果を調べた。
培養細胞を使ったin vitroの実験では、ノスカピンは通常のトリプルネガティブ乳がん細胞(p <0.01)および薬剤耐性のトリプルネガティブ乳がん細胞(p <0.05)の増殖を有意に阻害した。
移植腫瘍によるin vivoの実験で、ノスカピン(100mg/kg)の経口投与に続いて、ドセタキセルの静脈内投与によって、通常のトリプルネガティブ乳がん細胞(p <0.001)および薬剤耐性のトリプルネガティブ乳がん細胞(p <0.05)の移植腫瘍は有意に縮小した。
通常のトリプルネガティブ乳がん細胞の移植腫瘍において、ノスカピンとドセタキセルの併用群では、ノスカピンおよびドセタキセルのそれぞれの単独投与と比較して、腫瘍体積の減少の度合いはそれぞれ5.49倍および3.25倍であった。
薬剤耐性のトリプルネガティブ乳がん細胞の移植腫瘍では、ノスカピンおよびドセタキセルの単独投与と比較してノスカピン+ ドセタキセルの併用で処置した移植腫瘍では腫瘍体積の減少は2.33倍および1.41倍になり、抗アポトーシス因子および多剤耐性タンパク質の発現が減少した。
以上の結果から、ノスカピンの化学増感効果に続くドセタキセルを投与するレジメは、有望な化学療法戦略を提供し、薬物耐性のトリプルネガティブ乳がん細胞の治療に重要な役割を果たすことが期待される。
トリプルネガティブ乳がんは、乳がん細胞にエストロゲン、プロゲステロン、およびヒト上皮成長因子受容体(EGFR)が存在しないことを伴う、悪性度の高い乳がんの形態です。乳がん全体の10〜15%を占めます。
ドセタキセル3週1回投与療法は乳がんにおける代表的な治療法の一つです。微小管阻害剤の一つです。
このマウスの実験でノスカピンの投与量は経口投与で100mg/kgです。一般にマウスの体重当たりのエネルギー消費量や薬物の代謝速度は人間の約7倍と言われています。したがって、マウスの100mg/kgは人間の場合は7分の1の用量(14mg/kg)に相当します。体重60kgで800mg程度です。
【ノスカピンの服用量と副作用】
咳止めとして使用する場合は、1日量が45~200mgです。
がんの治療の場合には、さらに多くの量を服用しなければなりませんが、その量はまだ決定されていません。
米国で行われている臨床試験では、1日に1000~2250mgを3回に分けて服用する投与法が使用されています。
注射や座薬での投与も研究されていますが、ノスカピンは内服で体内への吸収が非常に良いので、経口投与で十分だと考えられてます。注射よりも内服の方が使用しやすく安全性も高いと言えます。
ノスカピンの体内での半減期は4.5時間です。
動物における安全性試験では、ノスカピンは極めて毒性が低いことが報告されています。大量に服用した場合の副作用としては、吐き気、腹部不快感が数%程度の頻度で発生しています。
1961年に余命数日と診断された末期がん患者にノスカピンを投与した臨床試験がジョンズ・ホプキンス大学で行われていますが、1日3000mgの投与で80%の患者はなんら副作用が認められませんでした。
残りの20%の患者では、軽度の鎮静化と腹部不快感が認められましたが、この研究ではノスカピンを投与しないコントロール群との比較が行われていないため、このような症状がノスカピンの副作用なのか末期がんの症状によるものなのかは不明です。
催奇形性の可能性が否定できないので妊娠中の服用はできません。
チューブリン阻害剤は効果的な抗がん剤ですが、多剤耐性、重度の副作用、一般的にバイオアベイラビリティの低さなど、クリニックで利用可能なチューブリン阻害剤の使用には多くの制限があります。したがって、これらの制限を克服することができる新規チューブリン阻害剤を探す必要が常にあります。
ノスカピンは経口で使用でき、副作用が少なく、確実な抗がん作用を発揮します。1日1000mg程度を目安服用すると効果が期待できます。
【植物アルカロイドは様々な薬効を発揮する】
西洋医学の化学薬品は強い選択的な薬理作用を発揮します。このような合成医薬品の薬効を知っている医師の多くは、漢方薬の薬効を信じていません。「漢方薬なんて効かない」と断言する医師も多くいます。
しかし、漢方薬に使われる生薬(薬草)には、確実な薬理作用を示す成分が多く含まれ、その中には西洋医学で使用されているものも多くあります。
例えば、植物由来の薬効成分に「アルカロイド(alkaloid)」というグループの化合物があります。
アルカロイド(alkaloid)という言葉は「アルカリ様」という意味ですが、窒素原子を含み強い塩基性(アルカリ性)を示す有機化合物の総称です。
植物内でアミノ酸を原料に作られ、植物毒として存在しますが、強い生物活性を持つものが多く、医薬品の原料としても利用されている成分です。
モルヒネ、キニーネ、エフェドリン、アトロピンなど、医薬品として現在も利用されている植物アルカロイドは多数あります。
漢方薬の薬効にもアルカロイドは重要な働きを担っています。
抗がん剤として使用されている植物アルカロイドとして、キョウチクトウ科ニチニチソウに含まれるビンクリスチンやビンブラスチンなどのビンカアルカロイド系、イチイ科植物由来のパクリタキセルやドセタキセルのタキサン系、メギ科ポドフィルム由来のエトポシドやテニポシドなどのポドフィロトキシン系などがあります。
イリノテカンは中国の喜樹という植物から見つかったカンプトテシンという植物アルカロイドをもとに改良された誘導体から開発されました。
ビンカアルカロイドは細胞分裂に重要な微小管の重合を阻害し、細胞分裂を停止させます。タキサン系は微小管の脱重合を阻害して細胞分裂を阻害します。エトポシドやイリノテカンはトポイソメラーゼの働きを阻害して細胞分裂を阻害します。(下図)
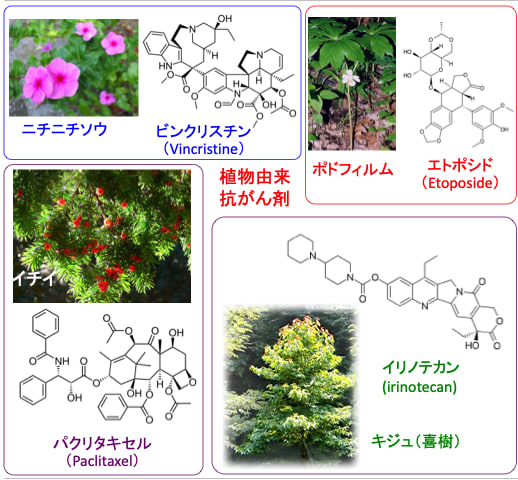
図:抗がん剤として使用されている植物アルカロイドとして、キョウチクトウ科ニチニチソウに含まれるビンクリスチンやビンブラスチンなどのビンカアルカロイド系、イチイ科植物由来のパクリタキセルやドセタキセルのタキサン系、メギ科ポドフィルム由来のエトポシドやテニポシドなどのポドフィロトキシン系などがある。イリノテカンは中国の喜樹という植物から見つかったカンプトテシンという植物アルカロイドをもとに改良された誘導体から開発された。
アルカロイドは多くのグループに分けられますが、その一つにイソキノリン・アルカロイド(Isoquinoline alkaloids)というグループがあります。
イソキノリン (isoquinoline) は、ベンゼン環とピリジン環が縮合した構造を持つ複素環式芳香族化合物の一種です。キノリンの構造異性体にあたります。イソキノリン環はチロシンから誘導されている。

図:キノリンはベンゼンとピリジンが縮合してできる。イソキノリンはキノリンの異性体。キノリンアルカロイドやイソキノリンアルカロイドには抗がん作用や抗菌作用など様々な薬効を示す物質見つかって、医薬品として利用されている。
【弱塩基性抗がん剤は酸性化したがん細胞外にトラップされる】
固形腫瘍の酸性細胞外空間は、弱塩基の細胞取り込みに対する生理学的障壁を作り出します。これをイオントラッピング(ion trapping)現象と言います。
イオン化した物質は細胞膜の脂質二重層を通過できません。イオントラップは、薬物のイオン化したもの(非透過性)とイオン化していないもの(透過性)の間に大きな透過性の違いがある場合に発生します。(図)

図:弱酸性医薬品(HA)は水素イオン(H+)を放出してイオン化した物質(A-)になる(①)。弱塩基性医薬品(B)は水素イオン(H+)を受け取ってイオン化した物質(BH+)になる(②)。細胞膜の脂質二重層(③)はイオン化していない物質(HAとB)しか通過できない(④)。がん細胞の外側は水素イオンが増えて酸性化している(⑤)。その結果、それぞれの反応式は左側に移行し、弱酸性医薬品は非イオン化型(HA)が増え(⑥)、弱塩基性医薬品はイオン化型(BH+)が増える(⑦)。イオン化していない物質しか脂質二重層を通過できないので、弱塩基性医薬品はイオン化型(BH+)が増えて、がん細胞の外側にトラップ(捕捉)される。抗がん剤の多くは弱塩基性であるため、酸性化したがん組織では、抗がん剤ががん細胞内に入り込めないので、抗腫瘍効果を発揮できない。
ビンクリスチン、ミトキサントロン、ドキソルビシン、ビンブラスチンなど多くの抗がん剤は解離定数が7.5〜9.5の弱塩基性です。例えば、ドキソルビシンは、8.3の塩基性解離定数(pKa)を持つイオン化可能な一級アミンからなるアントラサイクリンです。 pKaが8.3の場合、細胞膜を通過できる非イオン化型の割合は、pH 7.3では約10%、pHが6.3では約1%になります。非イオン化形態の薬物は膜の両側に等分布するため、細胞外環境のより低いpHでより多くの薬物が隔離され、治療効果が低下します。
このように塩基性抗がん剤は、酸性条件下でイオントラッピングを受け、がん細胞内への取込みが大幅に減少することが、培養細胞や動物実験で証明されています。
したがって、弱塩基性の抗がん剤を使用するときは、がん組織の酸性化を改善する重曹(重炭酸ナトリウム)やプロトンポンプ阻害剤やジクロロ酢酸ナトリウム使ったアルカリ療法を併用すると、抗がん剤の治療効果を高めることができます。
つまり、ノスカピンはアルカロイドで弱塩基性の薬ですので、がん組織が酸性化しているとがん細胞内に十分に取り込まれません。重曹服用などアルカリ療法を併用するとノスカピンの抗腫瘍効果を高めることができます。(アルカリ療法は792話で解説しています)
◉ ノスカピン治療についてはこちらへ:
| « 793) がん治療... | 795)再利用医... » |



