がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
249)エピジェネティクスと発がん
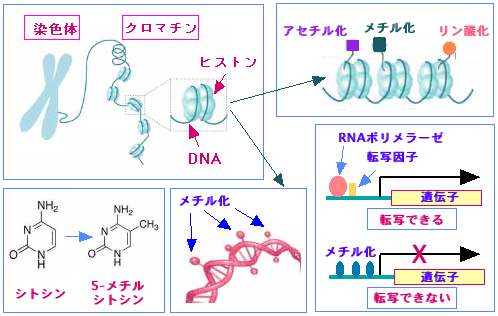
図。DNAのメチル化やヒストンの修飾(アセチル化など)によって遺伝子の発現が変化することをエピジェネティクスと言う。食品や漢方薬の抗がん作用の機序として、エピジェネティクスの関与が注目されている。
249)エピジェネティクスと発がん
【エピジェネティクスとは】
細胞の遺伝情報は細胞核の中の遺伝子(=DNA)に入っています。人間の1個の細胞の核には、約30億対のヌクレオチドからなるDNA(デオキシリボ核酸)が格納されており、このDNAが遺伝子の本体です。ヒト遺伝子は約3万種類のタンパク質を作る設計図(遺伝情報)をもっていますが、このゲノムの持つ遺伝情報の発現は、DNAの塩基配列と転写装置だけで制御されているわけではなく、DNAのメチル化やヒストン(DNAに結合するタンパク質)の修飾などによって複雑に制御されています。
「ゲノム(遺伝子)の塩基配列以外のメカニズムで遺伝子発現を制御し、細胞や生体に変化を生じさせる現象」のことを、エピジェネティクス(epigenetics)と言います。
エピジェネティクスの「エピ」はギリシャ語の接頭語で「上にある、別の、後から」という意味で、本来の遺伝情報(DNAの塩基配列)の土台の「上にかぶさる別の遺伝情報」や「後天的に獲得した遺伝情報」という意味を示しています。
例えば、私たちの体を構成する細胞は全て同じ遺伝情報を持っていますが、皮膚や神経や筋肉や肝臓など機能の異なる細胞になれるのは、それぞれの細胞において、使う遺伝子と使わない遺伝子に違いがあるからです。約3万個の遺伝子の全てが発現しているわけではなく、発現している遺伝子の違いによって細胞の種類が決まります。このように、DNAの塩基配列(=遺伝情報)が同じなのに、使う遺伝子と使わない遺伝子に目印をつけて、細胞に変化を生じさせる現象がエピジェネティクスです。
また、一卵性双生児は全く同じ遺伝子情報(DNA配列)を持っているにもかかわらず、その身体的特徴および性格や嗜好に違いがあり、病気の発症にも差が見られることが知られています。このような一卵性双生児の違いは幼少期には小さく、成長するに従って大きくなることから、環境の違いなどが遺伝子発現の違いを引き起こしていることを示唆しており、この現象もエピジェネティクスの例と言えます。
エピジェネティクスという言葉は1940年代から使われていますが、エピジェネティクスの研究が盛んになってきたのは10年くらい前からです。2003年に人間の全遺伝子配列の解析が終了し、ヒトゲノムの地図が完成したあと、現在はエピゲノム地図を作るプロジェクトが進行中です。メチル化することによって遺伝子発現が抑えられる場所の全てをについて、ゲノム地図の上に印をつけることが目標となっています。
エピジェネティクスによる遺伝情報の調節が解明されれば、正常な発生や老化のメカニズム、がんや生活習慣病などの発症メカニズム、さらには人間の健康に対する環境の影響などが理解できるようになると期待されています。
【発がんメカニズムとエピジェネティクス】
がん(癌)は、体内の一部の細胞が何らかの原因によって無制限に増殖するようになり、周囲の正常組織を破壊し、さらに他の臓器に転移して障害をもたらし、放置すれば宿主である人間を死にいたらしめる病気です。
細胞の増殖や死は遺伝子によって厳密に調節されており、自分勝手に増殖を続けることはありませんが、細胞増殖や死に関連する遺伝子の構造や発現に異常が起こると、無制限に増殖し、他の臓器に転移する悪性細胞(がん細胞)になります。
約3万個ある遺伝子のうち、どういう遺伝子に異常が起こると正常細胞ががん化するかが、がん研究の中心課題になっています。がんの発生に関与する「がん遺伝子」という遺伝子が知られています。このがん遺伝子の本来の役割は、正常な細胞を増殖させることですが、異常(遺伝子変異や過剰発現)を起こすと無制限に細胞を増殖させることに荷担してしまいます。
さらに、細胞のがん化を防いでいる「がん抑制遺伝子」も多数見つかっています。がん抑制遺伝子は、老朽化した細胞の死(アポトーシス)をうながし、細胞が増えすぎないようにコントロールする役割や、傷ついたDNAを修復させる役割をもった遺伝子です。このようながん抑制遺伝子の働きが弱まると、変異した細胞のDNA修復が妨げられたり、アポトーシス(遺伝子で制御された生理的な細胞死)で除去されなくなったりします。
つまり、がん遺伝子とかがん抑制遺伝子というのは、正常細胞の増殖・分化・細胞死に関わる遺伝子がDNA変異は発現異常の結果、機能異常をきたしたものです。
正常細胞の増殖に対して、がん遺伝子はアクセルの役割を果たし、がん抑制遺伝子がブレーキの役目を果たしています。正常細胞は必要なときに分裂し、必要がなくなると停止するという制御機構が正しく働いていますが、がん細胞がこのようなコントロールができない理由は、細胞増殖のアクセルとブレーキがともに故障しているからです。発がんに関係している人間の遺伝子として、100種類以上が知られており、そのうちの十数個の遺伝子の異常(突然変異や発現異常)が起こった時に、正常な増殖制御を行ううえでの限界が訪れ、がんが発生すると考えられています。
がん遺伝子やがん抑制遺伝子の働きの異常を引き起こす原因として、遺伝子の突然変異、すなわちDNAの塩基配列の異常(変異)があります。DNAに傷がついて間違った塩基に変換したり、遺伝子が途中で切れたりすることをDNAの「変異」と呼び、DNA変異を引き起こす物質を変異原物質とよびます。環境中には、たばこ・紫外線・ウイルス・食品添加物など変異原物質が充満しています。変異原物質は、体内でのエネルギー産生や物質代謝の過程でも作られます。
DNAは4種類の塩基(アデニン、グアニン、シトシン、チミン)の配列によってタンパク質のアミノ酸配列が決まるので、この塩基配列に欠損があったり、異なる塩基に置き換わったりすると、アミノ酸配列(つまり、タンパク質の構造)に変化が起こり、細胞の機能がおかしくなります。
最近までは、遺伝子の突然変異によるがん遺伝子やがん抑制遺伝子の機能異常が細胞のがん化の主な原因と考える研究者がほとんどでした。
しかし、最近の研究によって、遺伝子の変異とは関係ない、エピジェネティック(epigenetic)な機序によるがん遺伝子やがん抑制遺伝子の発現異常による発がんメカニズムの重要性が指摘されるようになりました。つまり、DNAの変異とは別に、DNAのメチル化や、DNAに結合するタンパク質のヒストンの修飾(アセチル化など)によって遺伝子発現が変化し、細胞ががん化するという機序です。
DNAのCpG(Cはシトシン塩基、Gはグアニン塩基)という配列の部分でCに-CH3という分子(メチル基)がつくのがDNAメチル化です。遺伝子を使うか使わないかを制御している部分(プロモーター)がメチル化されると、その遺伝子は使うことができなくなります。
DNAのメチル化がたくさん起こっている状態をハイパーメチル化と言いますが、様々な種類のがんの細胞において、複数のがん関連遺伝子(がん抑制遺伝子など)上にハイパーメチル化が起こっていることが報告されています。がん抑制遺伝子の周囲にハイパーメチル化が起こっているということは、そのがん抑制遺伝子は働いていないということを意味します。つまり、DNAのハイパーメチル化によってがん抑制遺伝子の発現が抑制されると、その細胞はがん化しやすくなります。このように、細胞のがん化において、遺伝子の突然変異だけでなく、DNAのメチル化ががんの発症と密接にかかわっているという考え方を裏付ける証拠は続々と出てきています。
たとえば、乳がんの再発率とPITX2という遺伝子のメチル化の程度に大きな相関関係があることが報告されています。乳がんの治療後10年たっても乳がんが再発しなかった割合は、PITX2遺伝子のメチル化が少ない女性で90%だったのに対して、同遺伝子のメチル化が多い女性では65%しかいませんでした。つまり、PITX2はがんを抑制する遺伝子で、メチル化が少ない(PITX2が発現している)場合は再発が少なく、メチル化が多い(PITX2の発現が抑制されている)場合は再発率が高いということです。
がんになりやすいとされる生活習慣を長期間続けた人は、がん抑制遺伝子のまわりにメチル化が多く集まっているという報告もあります。
タバコを吸う人は肺がんを抑える遺伝子のまわりにハイパーメチル化が起こっているという報告があります。今までは、タバコはタールなどの変異原物質の作用によって遺伝子の突然変異を起こすことが細胞のがん化の原因と考えられていましたが、DNAのメチル化などのエピジェネティックなメカニズムも重要と考える研究者が増えているようです。
様々ながんで、多くのがん抑制遺伝子がDNAメチル化異常により使えない状態になっていることが報告されています。一部のがんでは、がん抑制遺伝子がDNAメチル化異常によって不活化される場合の方が、突然変異や染色体欠失によって不活化される場合よりも多いという指摘もあります。
【がん予防とエピジェネティクス】
遺伝子変異というのは命令書に誤字脱字や欠損があるようなものです。命令の文面に間違いがあれば、間違った命令が出されます。エピジェネティクスによる遺伝子発現の抑制というのは、DNAの指示書は正しいのですが、その指示書が封筒に入れられて封をされた状態で、その文面が読めない状況です。
誤字脱字や欠損があると、正確な情報は得られません。しかし、封筒に入れられてみれない状況であれば、その封を開けることができれば、指示を読むことが可能になります。
同様に、DNAの突然変異が起こると、それを外から人為的に修復することは極めて困難ですが、DNAのメチル化は可逆的に変更できることが明らかになっているので、正常化させることは可能です。
一度決定された遺伝子発現の状態が、食物や環境や生活習慣などの外部からの影響を受けて変化するという「エピジェネティクスの可塑性」は、病気の治療に利用できるのではない かと考えられ、異常な遺伝子発現を正常な遺伝子発現の状態に戻すといったエピジェネティクスに関する基礎研究が進められています。
がん抑制遺伝子のメチル化がおこれば、そのがん抑制遺伝子はオフになり、発がんしやすくなります。しかし、このメチル化は薬などで可逆的に変更できる可能性があり、オフになっているがん抑制遺伝子を再びオンにしてがん細胞の増殖を抑制したり、死滅させることができると考えられています。
エピジェネティクスを標的としたがん治療薬の開発が進められています。特に、DNAメチル基転移酵素の阻害薬やヒストン脱アセチル化酵素の阻害薬において成果が示されていて、すでに治療に使用されている薬もあります。
DNAメチル基転移酵素の阻害薬はDNAのメチル化を阻害することによって、がん抑制遺伝子などがん細胞の増殖を抑える遺伝子の発現を高める効果があります。
ヒストンのアセチル化はDNAとヒストンの結合を緩くすることによって遺伝子の転写を促進します。つまり、ヒストン脱アセチル化酵素の阻害薬は、遺伝子の発現を高める効果があります。
このように、DNAのハイパーメチル化やヒストンの脱アセチル化によってがん抑制遺伝子の発現が抑えられた状態を阻害することによって、がん細胞の増殖の抑制やアポトーシスの促進が期待できます。2009年5月現在で、商品として市場に出ているエピジェネティクス医薬品は3品あり、いずれも米国で承認されています。現在臨床試験中のエピジェネティクス医薬品も多数あります。つまり、エピジェネティクスをターゲットにしたがんの予防や治療が有効であることを示しています。
さて、食品のがん予防効果ががん治療効果に関しても、エピジェネティクスの観点からの研究結果が報告されるようになってきました。最近まで、食品や薬草や漢方薬の抗がん作用の機序として、抗酸化作用、免疫増強作用、細胞増殖のシグナル伝達の阻害作用、抗炎症作用などが定番でした。しかし、最近では、エピジェネティクスをターゲットにした作用機序も注目されています。
大豆や大麦に含まれるルナシンというポリペプチドがヒストンのアセチル化を調整することによって抗がん効果を発揮する可能性を243話で紹介しています。
多くのがん抑制遺伝子は細胞のがん化の過程で発現抑制(サイレンシング)されていることから、DNAメチル化を阻害することによりこれらのがん抑制遺伝子を再び発現させる試みがなされています。食品や薬草や漢方薬など天然成分のがん予防効果や抗腫瘍効果もエピジェネティクスの観点から検討されています。
例えば、緑茶に含まれるエピガロ・カテキン・ガレート(EGCG)が、がん抑制遺伝子のメチル化を阻害してがん抑制遺伝子の働きを高めることが報告されています。EGCGのがん予防効果は今まで主に抗酸化作用によるものと考えられてきましたが、DNAメチル化の阻害でがん抑制遺伝子の活性を高める作用も関与しているかもしれないということです。その他、ウコンのクルクミンや、赤ぶどうの皮に含まれるレスベラトロール、アブラナ科野菜のスルフォラファン、大豆のゲニステインなど、がん予防効果が報告されている様々な成分についても、DNAメチル化やヒストンのアセチル化の調節などエピジェネティクスに作用する結果が報告されています。
漢方薬の抗がん作用についても、エピジェネティクスの観点からの効果がある可能性は十分にあります。
がんの漢方治療は、抗がん剤のような副作用が無いのに、がん細胞の増殖抑制や、がん細胞の性質をおとなしくするような効果があります。時には劇的に効く場合もあります。抗酸化や免疫増強や細胞増殖のシグナル伝達だけでは説明がつかないことも多く、遺伝子発現に作用して増殖や転移を抑えている可能性は十分にあると思います。
| « 248)乳がん患... | 250)食品や生... » |



