がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
410)医療大麻を考える(その1):カンナビジオールの抗がん作用
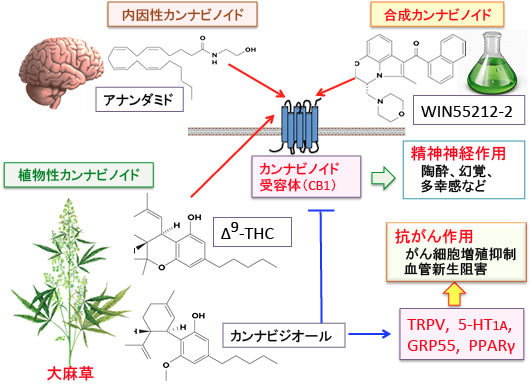
図:カンナビノイド受容体は7回膜貫通型のGタンパク質共役型受容体でCB1とCB2の2種類がある。CB1は中枢神経系に多く発現し、CB2は免疫細胞に多く発現している。内因性カンナビノイド(アナンダミドなど)はCB1受容体に作用して中枢神経系において様々な神経伝達調節を行っており、記憶・認知、運動制御、食欲調節、報酬系の制御、鎮痛など多岐にわたる生理作用を担っている。大麻草に含まれるΔ9-テトラヒドロカンナビノール(Δ9-THC)や合成カンナビノイド(WIN55212-2など)はCB1受容体に結合して様々な精神神経作用(陶酔、幻覚、多幸感など)を示すので、麻薬として使用が禁止されている。大麻草に含まれるカンナビジオール(cannabidiol)はCB1受容体のアンタゴニスト(拮抗薬)として作用するので精神神経作用は示さない。カンナビジオールはCa透過性イオンチャネルのTRPV(transient receptor potential vanilloid type)、セロトニン受容体の5-HT1A、GRP55、PPARγ(ペルオキシソーム増殖因子活性化受容体γ)などに作用して様々な生理作用を示す。医療大麻が抗がん作用を示すことは多くの研究によって報告されているが、大麻(マリファナ)やΔ9-THCは大麻取締法や麻薬取締法などによって日本では現時点では使用は不可能である。カンナビジオールの抗腫瘍作用が多くの研究で示されている。規制対象外の大麻草由来成分のカンナビジオールのがん治療における利用が注目されている。
410)医療大麻を考える(その1):カンナビジオールの抗がん作用
【体内の細胞には大麻成分カンナビノイドの受容体がある】
漢方治療や薬草を使った民間療法やハーブ治療の効果を否定する医者は多くいます。「漢方薬やハーブが病気に効くわけがない」という意見です。
しかし、ケシの未熟果に含まれるモルヒネやコデインなどのアヘンアルカロイド(オピオイド)や、大麻草に含まれるカンナビノイド(大麻草に含まれる薬効成分の総称)の強力で特異的な薬理作用を理解すれば、病気の治療に有効な植物成分の存在は否定できないはずです。
また、植物の中には、どんな抗がん剤よりも致死量が少ない毒性の強い成分も存在します。このような毒は動物を殺すこともできますが、適量を使用すれば薬にもなります。
動けない植物は動物から食べられて全滅しないように毒を持つようになったと考えられており、このような成分が古くから病気の治療に多く利用されています(309話参照)。
つまり、「漢方薬やハーブが効かない」と言っている人は、単に薬理学の知識がないことを自ら明かしているだけです。
オピオイド受容体は最初はアヘンに含まれるモルヒネなどのアヘンアルカロイドが結合する細胞の受容体として見つかり、その後、このオピオイド受容体に結合する内因性オピオイドとしてβエンドルフィンやエンケファリンなどのいわゆる脳内麻薬(内因性オピオイド)が発見されました(脳内麻薬については153話、269話参照)。
そして、これらの内因性オピオイドとオピオイド受容体が生体機能の調節に重要な役割を担っていることが明らかになっています。
大麻草(マリファナ)に含まれるカンナビノイドが結合する受容体としてCB1とCB2の2種類が見つかっており、このCB1やCB2に結合する内因性カンナビノイドとしてアナンダミド(Anandamide; N-arachidonoylethanolamide; AEA)や2-アラキドノイルグリセロール(2-arachidonoylglycerol; 2-AG)などが知られています。
つまり、体内には内因性カンナビノイド(AEAや2-AGなど)と、それらを合成する酵素や分解する酵素、内因性カンナビノイドが結合するカンナビノイド受容体によって内因性カンナビノイド・システムが構成されています。
カンナビノイド受容体は7回膜貫通型のGタンパク質共役型受容体でCB1とCB2の2種類があります。CB1は中枢神経系に多く発現し、CB2は免疫細胞に多く発現していますが、カンナビノイド受容体(CB1とCB2)は多くの組織の細胞に存在し、多彩な生理機能の調節に関与しています。
内因性カンナビノイド(AEAや2-AGなど)はCB1受容体に作用して中枢神経系において様々な神経伝達調節を行っており、記憶・認知、運動制御、食欲調節、報酬系の制御、鎮痛など多岐にわたる生理作用を担っています。
内因性カンナビノイドのアナンダミドと2-アラキドノイルグリセロールは細胞膜のリン脂質からホスホリパーゼによって生成されるアラキドン酸の代謝産物です。
つまり、内因性カンナビノイドは生理的あるいは病的刺激によってオンデマンド(要求に応じて)に細胞膜のリン脂質を分解して合成・分泌されて、カンナビノイド受容体を刺激して生理作用を示します。
この内因性カンナビノイド・システムが関与している疾患として、多発性硬化症、脊髄損傷、神経性疼痛、がん、動脈硬化、脳卒中、心筋梗塞、高血圧、緑内障、肥満、メタボリック症候群、骨粗鬆症などが報告されています。内因性カンナビノイド・システムは神経細胞の損傷などに対して細胞を保護する作用や回復を促進する作用に関与しています。
つまり、これらの疾患の治療に内因性カンナビノイド・システムの制御(活性化や阻害など)が有効である可能性が示唆されているのです。
現在、カンナビノイド受容体に作用する物質として、生体内で合成される内因性カンナビノイド(アナンダミド、2-アラキドノイルグリセロールなど)、大麻草(Cannabis sative)に含まれる植物性カンナビノイド(テトラヒドロカンナビノール)、医薬品の開発目的で合成されている合成カンナビノイドなどがあります。
オピオイド受容体もカンナビノイド受容体も、動物が植物成分を薬効として利用するために存在する訳ではありません。もともと生体内で内因性のリガンド(受容体に結合して活性化する成分)があって特異的な受容体との間にシグナル伝達系を作っていたものが、その受容体に結合する成分が植物にたまたま含まれていたというだけです。
恐らく、このような植物成分は、動物に対する毒として存在しているものと考えられます。動物に有毒な成分を持っている植物は生存や繁栄に有利になるので、このような毒を持った植物の進化は促進されると考えられます。そして、このような植物毒を人間は医療に利用してきました。
大麻も古くから医薬品として人類が使用してきました。1850年から1937年まで、アメリカ薬局方は大麻草を100種類以上の疾病に効く主要な医薬品と記述しています。日本でも、敗戦直後まで医療大麻があり「インド大麻草チンキ」などの名前で薬局で販売されていました。
しかし、世界保健機関による麻薬単一条約(1961年制定、日本は1964年に加盟)や日本では大麻取締法(1948年制定)によって医療への利用も禁止されています。世界中のほぼ全ての国で大麻は非合法化されています。(しかし、少量の所持や個人での使用は処罰しない「大麻の非犯罪化」を認めている国はあります。)
その主な理由は、カンナビノイドの主要な成分であるテトラヒドロカンナビノール(THC)に陶酔作用などの精神作用があり麻薬として規制されているためです。しかし、最近の研究によってTHCのような精神作用が全く無いカンナビノイドに抗がん作用があることが報告されるようになっています。
このような精神作用のないカンナビノイドは規制がないため、合法的に使用ができます。米国などではすでにネット上で販売されています。
規制されていないカンナビノイドのがん治療における有用性について数回に分けて考察します。
今回は、カンナビジオールの抗がん作用について幾つかの論文を紹介します。
【カンナビジオールは前立腺がん細胞のアポトーシスを誘導する】
精神作用がないカンナビノイドの抗がん作用については、最近多くの研究があります。前立腺がんについては以下のような論文があります。
Non-THC cannabinoids inhibit prostate carcinoma growth in vitro and in vivo: pro-apoptotic effects and underlying mechanisms.(非-THCカンアビノイドが前立腺がんの増殖をin vitroおよびin vivoで阻害する:アポトーシス誘導作用とその作用メカニズム)Br J Pharmacol. 168(1): 79-102, 2013年
THCというのはテトラヒドロカンナビノール(tetrahydrocannabinol)のことで大麻の最も代表的な薬効成分です。しかし、このTHCには陶酔作用などの精神作用があるため、使用は困難です。日本では大麻取締法や麻薬取締法で医療目的であっても大麻やTHCを所有することも使用することも禁止されています。
カンナビノイド(Cannabinoids)というのは大麻に含まれる成分の総称です。このカンナビノイドにはTHCのように精神作用を有するものの他に、精神作用のないカンナビノイドもあります。
Non-THC cannabinoids(非-THC カンナビノイド)というのは精神作用のないカンナビノイドを意味しています。つまり、精神作用のないカンナビノイド(=カンナビジオール)が前立腺がん細胞の増殖を抑え、アポトーシスを誘導するという論文です。要旨の日本語訳を以下に記載します。
【要旨】
研究の背景と目的:カンナビノイド受容体を活性化すると前立腺がん細胞のアポトーシスを誘導できる。しかし、Δ9-テトラヒドロカンナビノール(Δ9-tetrahydrocannabinol:THC))以外の、カンナビノイド受容体に結合活性を持たないカンナビノイドについては、抗腫瘍効果については検討されていない。これらのカンナビノイドには、アンドロゲン受容体依存性の前立腺がんの生存に必要なtransient receptor potential melastatin type-8 (TRPM8)の活性を阻害するものが知られている。
実験方法:アンドロゲン受容体陽性前立腺がん細胞(LNCapと22RV1)とアンドロゲン受容体陰性前立腺がん細胞(DU-145とPC-3)を用いて、細胞生存率や細胞周期やアポトーシス誘導に対する、純粋なカンナビノイド成分あるいはある種のカンナビノイドを豊富に含むカンナビス(大麻)株の作用を検討した。
主な結果:カンナビジオール(Cannabidiol)は前立腺がん細胞の生存率を顕著に低下させた。他の物質は培養液から血清を24時間除去した細胞において生存率を減少させる効果を示した。
血清を添加した培地では、ある種のカンナビノイドを豊富に含むカンナビス(大麻)株のエキスの方が、純粋なカンナビノイドよりも有効であった。カンナビジオールを多く含むカンナビス(大麻株)のエキスを、LNCaPとDU-145細胞を移植したマウスに腹腔内投与するとビカルタミド(bicalutamide;商品名カソデックスという抗アンドロゲン剤)とドセタキセル(docetaxel:商品名タキソテールという抗がん剤)の抗腫瘍効果を増強し、LNCaPを移植した動物実験では単独で腫瘍を縮小した。
カンナビジオールは1-10 µMの濃度でアポトーシスを誘導し、内因性のアポトーシス経路のマーカー(PUMAとCHOPの発現と細胞内カルシウムイオン)の上昇を認めた。
LNCaP細胞においては、カンナビジオールのアポトーシス誘導作用はTRPM8の阻害とアンドロゲン受容体の発現抑制とp53の発生化と活性酸素の産生亢進が関与していた。アンドロゲンに不応性の神経内分泌細胞様に分化してLNCaP細胞はカンナビジオール誘導性のアポトーシスにより感受性が高かった。
結論:これらの結果は、前立腺がんの治療にカンナビジオールの臨床的効果を検討する必要性を示唆している。
大麻草は学名をCannabis sativa L(カンナビス サティーヴァ エル)という1年草の草です。この大麻草に含まれる成分にカンナビノイドと総称される物質があり、様々な薬理作用が知られています。
医療大麻はがん患者の痛みや倦怠感、抗がん剤治療に関連した吐き気や嘔吐の軽減に有効であることが報告されています。米国では一部の州で医療大麻の使用が許可されていますが、日本では大麻取締法により医療目的でも大麻は所持しただけで逮捕される状況です。
大麻取締法の第4条には、「大麻から製造された医薬品を施用し、又は施用のため交付すること。」「大麻から製造された医薬品の施用を受けること。」の両方が禁止(「何人も次に掲げる行為をしてはならない」と記載)されています。医療目的であっても大麻および大麻由来の製品を使用すれば医者も患者も両方が逮捕されます。このため、世界では許可する国が増えている医療大麻も、日本では臨床試験すらもできない状況になっています。
カンナビノイド受容体(CR1、CR2)のアゴニスト(受容体に働いて作用を発揮する作動薬)になるTHCや合成カンナビノイドや内因性カンナビノイドががん細胞の増殖を抑えることは良く知られています。
カンナビジオールはある種のカンナビスに多く含まれていますが、CB1やCB2への結合活性は低く、TRPV1チャンネルを活性化するなどまだ十分に作用機序は判っていません。この論文では前立腺がん細胞のTRPM8の阻害作用が報告されています。
TRP(Transient Receptor Potential)タンパク質はCa2+透過型陽イオンチャンネルを形成し、細胞質内へのCa2+流入を制御して広範な生理現象を制御しており、何十種類というサブタイプがあってTRPファミリーを形成しています。
TRPファミリータンパク質についてはあまりに複雑なので、これ以上はここでは触れませんが、カンナビノイドの作用機序にはTRP(Transient Receptor Potential)タンパク質を介した細胞内Ca2+イオンの制御が関連しているようです。
カンナビジオールがカンナビノイド受容体CB1とCB2に非依存性のメカニズムで抗腫瘍作用を示すことは複数の論文で報告されています。
この論文では、12種類の精製したカンナビノイドと幾つかのカンナビス株の粗抽出エキスの作用を検討し、カンナビノイドはTRPM8チャンネルの発現と活性を阻害することを報告しています。そしてこのチャンネルは前立腺がんの生存に重要な役割を担っているので、カンナビノイドが前立腺がんの増殖を阻止しアポトーシスを誘導すると言っています。
その他にも複数の機序で前立腺がんの増殖を抑制すること、アンドロゲン依存性のものよりより悪性度の増したホルモン不応性のものがカンナビジオールの感受性が高いことを報告しています。
カンナビジオールの作用機序は細胞の種類によっても異なるようです。いずれにしても、カンナビジオールが前立腺がんの増殖を抑制しアポトーシスを誘導する可能性が示唆されています。
【カンナビジオールは乳がん細胞の増殖を抑制する】
次のような論文があります。これは前述の前立腺がん細胞の論文と同じ研究グループの報告です。
Antitumor Activity of Plant Cannabinoids with Emphasis on the Effect of Cannabidiol on Human Breast Carcinoma.(ヒト乳がん細胞の対するカンナビジオールの効果を主体にした植物成分カンナビノイドの抗腫瘍効果)J Pharmacol Exp Ther. 318(3): 1375-1387, 2006年
【要旨】
Δ9-テトラヒドロカンナビノール(THC)は様々な種類のがん細胞に対して抗腫瘍効果を示すが、精神作用の副作用があるために、がん治療における使用には限界がある。THC以外の植物カンナビノール、すなわちcannabidiol, cannabigerol, cannabichromene, cannabidiol acid、THC acidについて、それらの抗腫瘍効果を検討し、カンナビジオール(cannabidiol)あるいはTHCを多く含む大麻草(カンナビス)の粗抽出エキスが精製したカンナビノイドよりも勝っているかどうかを検討した。
多数の培養がん細胞株を用いた実験の結果、5種類の天然のカンナビノイドのうち、カンナビジオールが最も抗腫瘍活性が高く(IC50は6.0~10.6μM)、正常細胞への毒性は少なかった。
カンナビジオールの豊富なカンナビス粗抽出エキス(cannabidiol-rich extract)はカンナビジオールと同等の抗腫瘍活性を示し、カンナビゲロール(cannabigerol)とカンナビクロメン(cannabichromene)がそれに続いた。
カンナビジオールおよびカンナビジオールを豊富に含む大麻草粗抽出エキスは、免疫不全マウスにヒト乳がん細胞細胞MDA-MB-231を移植する実験系やがん遺伝子K-rasで形質転換したラットの甲状腺上皮細胞を移植する実験系において腫瘍細胞の増殖および転移を阻害した。
作用機序に関する幾つかの実験結果より、抗腫瘍作用のメカニズムは細胞の種類によって異なることが示唆された。
しかしながら、少なくとも MDA-MB-231細胞に関しては、カンナビジオールの作用機序は、カンナビノイド受容体CB2とvanilloid transient receptor potential vanilloid type-1受容体の直接および間接的な活性化、カンナビノイド受容体およびvanilloid 受容体に非依存的な細胞内カルシウムイオンと活性酸素種の上昇が関連していることが示唆された。
これらの結果は、カンナビジオールおよびカンナビジオールを含む大麻草エキスのがん治療における利用をさらに検討する必要性を示唆している。
大麻草エキスが抗がん作用を示すことは多くの研究で明らかになっています。しかし、大麻草の主成分であるテトラヒドロカンナビノール(THC)には陶酔作用などの精神症状を引き起こすため、がん治療への応用は限られています。THCの作用はがん患者の消耗(wasting)や吐き気・嘔吐や疼痛の緩和の目的は有用ですが、THC自体は麻薬取締法で規制されているため、THCのがん治療への応用は日本では現時点では不可能です。
そこで、THC以外の精神作用のないカンナビノイドに抗がん作用があるかどうかを検討したのが、この研究の目的です。
がん細胞の種類によってカンナビノイドの作用は異なるのですが、多くの種類のがん細胞株を検討した結果、THCよりもカンナビジオールの方が抗がん作用が強いことがこの研究で明らかになっています。そして、カンナビゲロール(cannabigerol)やカンナビクロメン(cannabichromene)も同様に抗腫瘍活性を示し、その活性はTHCよりも高いことが示されました。
また、それぞれの純粋な(精製した)カンナビノイドよりも、カンナビジオールなどを含む大麻草粗抽出エキスの方が抗腫瘍活性が高いことが示されています。
これは、大麻取締法で規制されていない産業用大麻草(繊維を取る目的の大麻でヘンプ[Hemp]と呼ばれる)の茎から抽出したエキスにはTHCはほとんど含まれず、カンナビジオールが多く含まれるので、このような合法的なヘンプ抽出エキスががん治療に使える根拠になります。
実際に、移植腫瘍を用いた実験系で、カンナビジオールおよびカンナビジオールを多く含むヘンプ抽出エキスはがん細胞の増殖や転移を有意に抑制する効果が認められました。
カンナビジオールの抗腫瘍効果のメカニズムの詳細はまだ不明です。
カンナビノール受容体のCB1とCB2への結合活性(アフィニティー)が弱いので、カンナビノール受容体を介さないメカニズムでの説明が必要です。その一つがvanilloid 受容体の活性化です。
この論文ではTRPV1受容体の活性化や内因性カンナビノイドのアナンダミド(anandamide)の不活性化の阻害の機序が示されています。
ただし、MDA-MB-231細胞での検討では、カンナビジオールの抗腫瘍効果はカンナビノイド受容体CB2とTRPV1受容体の活性化を介した機序が示唆されています(CB2およびTRPV1の拮抗阻害剤を添加するとカンナビジオールの抗がん作用が減弱するため)
しかし、CB2やTRPV1受容体とは関係無いメカニズムの関与も示唆されています。
カンナビジオールによるがん細胞のアポトーシスは抗酸化剤の添加で阻止されることから、細胞内での活性酸素の産生増加が関与している可能性が示唆されています。
活性酸素の産生増加と関連して細胞内カルシウムの流入の増加がアポトーシス誘導と関連していることが示唆されています。
つまり、カンナビジオールは細胞内の活性酸素の発生を増やし、Ca2+透過型陽イオンチャンネルであるTRPV1受容体を活性化してカルシウムの細胞内流入を増やして細胞死を誘導する機序が推測されています。しかし、詳しいメカニズムはまだ不明という方が正しいようです。
以上のように、従来は、カンナビノイドの抗腫瘍効果は精神作用があるテトラヒドロカンナビノール(THC)の作用が主体と考えられており、そのためカンナビノイドのがん治療への利用が制限されていました。しかし、精神作用のないカンナビジオールの方がTHCよりも抗腫瘍活性が高い可能性が複数の論文で指摘されています。
同様な論文は、別のがん種を用いた実験、別の研究グループからの報告などで多数報告されています。
【カンナビジオールは抗腫瘍免疫を高める】
次のような論文があります。
Cannabinoids increase lung cancer cell lysis by lymphokine-activated killer cells via upregulation of ICAM-1.(カンナビノイドはICAM-1の発現亢進を介してリンフォカイン活性化キラー細胞による肺がん細胞死を促進する)Biochem Pharmacol. 2014 Jul 25. pii: S0006-2952(14)00420-1. doi: 10.1016/j.bcp.2014.07.014. [Epub ahead of print]
【要旨】
カンナビノイドは肺がん細胞の細胞間接着分子-1(intercellular adhesion molecule 1;ICAM-1)の発現を亢進し、これが肺がん細胞の浸潤や転移を抑制する作用の一部になっていることが報告されている。
肺がん細胞株(A549、H460)と肺がん患者から採取した転移がん細胞を用いて、カンナビノイド誘導性のICAM-1発現亢進が、リンフォカイン活性化キラー細胞(LAK細胞)とがん細胞の接着、およびLAK細胞を介する細胞死誘導にどのような効果を示すかを検討した。
精神作用を持たないカンナビノイドの一種であるカンナビジオールは、肺がん細胞とLAK細胞の接着を促進し、LAK細胞による肺がん細胞の細胞死誘導を亢進した。この作用は抗ICAM-1抗体を添加してICAM-1とLAK細胞の接着を阻害すると消失した。
また、特異的siRNA(RNA干渉を起こす短い二本鎖RNA)やカンナビノイド受容体(CB1,CB2)のアンタゴニスト(拮抗薬)やtransient receptor potential vanilloid 1受容体のアンタゴニスト(拮抗薬)によってカンナビジオール誘導性のICAM-1発現亢進を阻害すると、カンナビジオールによる肺がん細胞の細胞死は阻止された。
さらに、リンパ球機能関連抗原1(lymphocyte function associated antigen-1 ;LFA-1;リンパ球表面の インテグリン細胞接着分子)に対する抗体でLAK細胞を前処理すると、カンナビジオールによる肺がん細胞死は阻止された。これは肺がん細胞のICAM-1とLAK細胞のLFA-1のクロスリンクが、肺がん細胞の細胞死に重要なプロセルであることを示している。
ICAK-1依存性の肺がん細胞死の誘導は、植物カンナビノイドのΔ9-テトラヒドロカンナビノール(THC)や内因性カンナビノイドの類縁体であるR(+)-methanandamide(MA) でも観察された。
最後に、それぞれのカンナビノイドは非腫瘍性の気管支上皮細胞(BEAS-2B)に対しては、ICAM-1の発現をほとんど(CBD、THC)あるいは全く(MA)亢進せず、LAK誘導性の細胞死も亢進しなかった。
これらの結果より、カンナビノイドによって誘導される肺がん細胞のICAM-1の発現亢進は、LAK細胞による細胞死を促進することが示された。これは、カンナビノイドによる抗腫瘍効果の新規のメカニズムと思われる。
カンナビジオールには、がん細胞の直接的な増殖抑制やアポトーシス誘導、免疫細胞を介した抗腫瘍効果の他に、血管新生阻害作用や抗炎症作用なども報告されています。
カンナビノイド受容体CB1には精神作用の他に、心臓機能を抑制する作用などネガティブな作用もあります。むしろ、CB1受容体に作用しない、あるいはCB1受容体を拮抗阻害することが報告されているカンナビジオールの方がより有用性があるという意見が最近は増えています。
【カンナビジオールは合法的に使用できる】
大麻取締法の第一条には 『この法律で「大麻」とは、大麻草(カンナビス・サティバ・エル)及びその製品をいう。ただし、大麻草の成熟した茎及びその製品(樹脂を除く。)並びに大麻草の種子及びその製品を除く。』となっています。つまり、繊維を取る目的の農業用麻(agricultural hemp)あるいは産業用麻(Industrial hemp)の茎および種子から抽出した製品は大麻取締法の規制の対象になりません。
カンナビジオール自体は麻薬取締法や大麻取締法で規制されていないため、がん治療に利用できます。
カンナビジオールを多く含むサプリメント(CBDオイル)もネット上で販売されています。
医療大麻は進行がん患者の消耗や痛み、抗がん剤治療による吐き気や嘔吐の軽減に著効を示します。このような効果にはカンナビ受容体のCB1やCB2へのアゴニスト作用(受容体に結合して活性化する作用)が重要のように思われます。したがって、CB1やCB2受容体へのアゴニスト活性がほとんど無いカンナビジオールは痛みや吐き気や消耗を軽減する効果は少ないかもしれません。しかし、実際は、抗がん剤治療の副作用軽減などがん治療へ併用する有用性が多数報告されています。
がん細胞の増殖抑制やアポトーシス誘導や血管新生阻害作用はTHCより高いので、むしろカンナビジオールを主体にして、併用治療を工夫して抗腫瘍活性を高める方法はかなり効果が期待できそうです。
世界各国では、医療大麻を認める国が増えています。医療大麻で、進行がん患者の症状が劇的に改善したり、進行した腫瘍が消滅した例も経験されているようです。YouTubeには進行した脳腫瘍が治癒した小児の例を紹介したテレビ報道なども出ています。
もし、医療大麻が非常に有効な治療法であるならば(多くの研究者はそう考えている)、日本で医療大麻が病気の治療に使えない状況は憲法違反(日本国憲法で保証されている国民の生存権や幸福追求権に違反) であるという主張は容易に納得できます。
しかし、大麻取締法を執行している厚生労働省には法律を変える権限はなく、全くの悪法だと判っていても、官僚はそれを守り続けなければならないと思っています。多くの人や団体が大麻取締法の改正のために運動しています。医療大麻を使えるように医療関係者もそろそろ行動すべき時期に来たと思います。
| « 409)カフェイ... | 411)医療大麻... » |




