がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
405)匙を投げられてからのがん治療
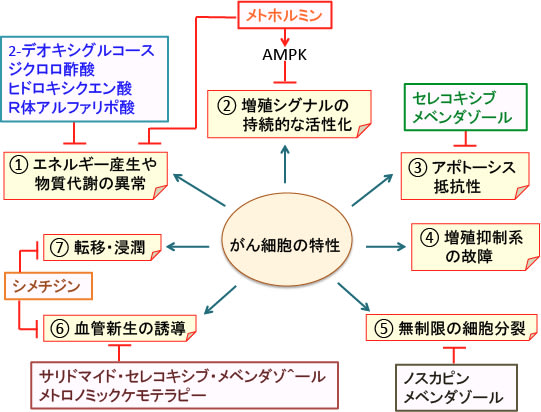
図:がん細胞は正常細胞と異なる特性を多く持っている。がん細胞に特徴的な性質をターゲットにするとがん細胞の増殖を抑え、死滅させることができる。図に示した医薬品やサプリメント以外にも有効なものは数多く存在する。これらを組み合わせることによってがん細胞の増殖を抑制する研究が行われている。
405)匙を投げられてからのがん治療
【標準治療は進行がんの治療をしたがらない】
個々のがん患者さんの状況には大きな差があります。がんが早期で手術によって根治が期待できる場合もあれば、再発や転移によって余命数ヶ月の宣告を受ける場合もあります。
西洋医学は「根治できるがん」の治療は得意です。手術や放射線治療などで確実にがん組織を除去あるいは死滅させる治療法は進歩しています。転移していない段階の早期のがんであれば、多くは標準治療で根治ができます。
しかし、転移が見つかったり再発がんのように「根治が難しいがん」に対しては、西洋医学はあきらめが早いように思います。がん治療の専門性が高い病院ほど、匙を投げるのが早く、緩和ケアを勧めて一般病院やホスピスへの転院を促すようになります。
このようながん専門病院は、診察や治療待ちの患者が多いので、「治せる患者」を優先し、「進行した患者」や「末期がんの患者」のような治療が困難(面倒)な患者さんに対しては緩和ケア専門の施設に紹介して、早くがん治療を打ち切りたいと思っています。
セカンドオピニオンを受けても、大きな病院ほど末期がんの患者さんには冷たいようです。『治る見込みはないので、これ以上治療をしても意味がない』と門前払いしています。
がん専門性の高い病院ほど、治る見込みのない患者さんには来てほしくないと思っており、これががん難民を作り出している理由の一つになっています。
本来であれば、治療が困難な患者さんを専門性の高い病院が治療するべきですが、延命治療は面倒で時間と手間がかかる割に結果が伴わない(多くは効かない)ので、やりたくないと思っているからです。
表向きは、『根治可能な患者さんに医療資源を向けるために、余命数ヶ月の進行がんや末期がんの患者さんを専門病院が治療を行うのは医療資源の無駄だ』という理屈になっていますが、標準治療には『治る見込みの少ない患者をなんとか救おう』と全力を尽くす考えが無いだけのようにも思います。
したがって、医者が匙を投げたあとは、自分で治療法を見つけるしかありません。そのため、「がんが治る」と宣伝されているサプリメントを購入したり、漢方治療や免疫治療などの代替医療を試しています。既存の医薬品を組み合わせたがん治療も行われています(402話参照)。
物質特許の切れた既存の医薬品やサプリメントを使ったがん治療の研究を、製薬会社は行いません。新薬しか儲けにならないからです。このような研究は公的な研究費を使って細々と行われています。
新薬の開発では製薬会社が何十億円も何百億円も開発につぎ込むので、臨床試験の数も論文も数多くあります。一方、特許の取れない薬やサプリメントを使ったがん治療に関する研究は少数しかありません。
論文が少ないと効果が乏しいように考えるかもしれませんが、これは単に研究費が公的なものに限られるからです。実はこのような研究者にとって金銭的利益にならないがん治療法に関する論文はがん代替医療の宝庫になっています。(400話参照)
【無駄で過剰な診療が行われる理由】
「標準治療」や「保険診療」というと、有効性のエビデンス(証拠)が確立されている治療法だと多くの人は思います。しかし、がんや糖尿病やうつの治療など多くの医療分野において、本当にそうなのかと疑ってみる余地は大いにあります。
無駄な治療や過剰な治療(検査も含めて)の存在や、従来の薬と効果にあまり差がないのに高額な新薬を使う傾向があるなど、標準治療や保険診療には問題点が多くあります。
その最大の原因は、医療の世界が製薬産業に牛耳られているという構図にあります。
利益を求める製薬産業は、医師たちを学会ぐるみで取込み、高額で過剰な医療に誘導しています。
がんや糖尿病や精神疾患など専門家が集まって個々の学会が設立されます。学会は研究成果を発表し議論することによって、標準的な治療法を確立し広める最大の役割を担っています。しかし、学会やそれに所属する医師たちは製薬企業に取り込まれて、製薬産業が意図する方向で標準治療を確立し、広めています。つまり、製薬産業の利権のために、医師が利用され、過剰診療が発生していると言われています。
このことは多くの医師が気づいていますが、なぜか事態は変わりません。最近になって、製薬企業と大学病院の医師たちの癒着による「論文捏造」の事件が明るみになって、製薬産業の利権追求がいかに医療を歪めているかが世間に知られるようになってきました。しかし、これは氷山の一角であり、多くの領域で過剰診療や高額な薬の無駄な使用が行われています。
【最大耐用量を投与する抗がん剤治療は本当にエビデンスがあるのか】
保険診療を行っていれば、たとえ高額な薬を使っても高額療養費制度(402話参照)によって1ヶ月の自己負担は数万円レベルなので、医師は患者さんに気兼ねなく高額の薬を使う傾向にあります。
自費診療でがん治療を行っていると、その効果が費用に見合わなければ、患者さんは治療を受けようと来院しませんし、治療を始めても効果を実感しなければ止めてしまいます。自費診療でがん治療を行うためには、費用対効果の高い(安価な薬で有効性のエビデンスのある)治療法を追求しなければなりません。
私は、がんの補完代替医療を専門にした自由診療のクリニックを開設して12年になります。
12年前と比べて、最近、『抗がん剤治療を受けたくない』からという理由で来院される方が多くなったような気がします。
数年くらい前までは、抗がん剤治療の副作用軽減や抗腫瘍効果増強の方法を求めて、漢方薬やサプリメントの相談がほとんどでした。抗がん剤を受けたくないから代替医療を受けたいという理由は少なかったように思います。
最近は、積極的に「抗がん剤は受けたくないから」という理由で、代替医療を選ぶ方が多く来院しています。
これは、抗がん剤の問題点を言及した書籍がベストセラーになったためかもしれません。抗がん剤治療のデメリットについては週刊誌などでも時々記事になっています。
抗がん剤治療の歴史が長くなると、家族の方や知人が抗がん剤治療を受けたのを知っているという患者さんも増えています。そして、その多くが、抗がん剤治療で悪い結果を経験した方が多くいます。
「家族が抗がん剤治療を受けたが、後悔する結果に終わったので、自分は抗がん剤治療を受けない選択を選ぶ」という患者さんが増えています。
医師による抗がん剤治療の説明でも、メリットとデメリットをはっきりと説明するようになっています。進行がんの抗がん剤治療は延命治療であって根治は望めないことを説明しています。
つまり、抗がん剤治療の欠点や問題点が知れ渡った結果、抗がん剤治療を積極的に拒否する患者さんが増えたのかもしれません。
確かに、今の抗がん剤治療には多くの問題点があります。他に有効な方法が無いので消去法で実施されることになりますが、進行がんの抗がん剤治療は有効性のエビデンスが本当にあるのかまだ議論されている段階の治療法なのです。
本質的な問題点は、抗がん剤治療に代わるものが無いという現実です。いろんな代替医療も確実性や有効性で満足いくものでなければ、消去法で抗がん剤治療しか無いということになります。
しかし、毒性の強い抗がん剤治療と同等あるいはそれ以上の効果が期待でき、副作用が少ない治療法があれば、標準治療の代替となります。
このような治療法が広まることは製薬産業にとっては好ましいことではないので何とか阻止しようとします。しかし、高額な新薬に頼ったがん治療でもなかなか治療成績が上がらないので、最近は、製薬産業の利権から離れて、物質特許が切れた安価な既存薬を組み合わせた「体にやさしいがん治療」の研究が盛んになっています。
【メトロノミック・ケモテラピーをベースにしたがん治療】
メトロノミック・ケモテラピー(Metronomic Chemotherapy)については397話で解説しています。
通常の抗がん剤治療は、副作用に耐えられる最大量(最大耐用量)の抗がん剤を投与します。この場合、正常組織へのダメージも強いので、正常組織のダメージを回復させるために抗がん剤投与の間に休薬期間が必要ですが、この休薬期間に腫瘍血管が急速に再生し、生き残ったがん細胞が増殖します。抗がん剤が効きにくい強いがん細胞が選択的に生き残るので、がん組織は次第に抗がん剤が効きにくい細胞が多くなってきます。
一方、休薬期間を設けないで、メトロノームのように定期的に頻回に低用量の抗がん剤を投与するメトロノミック・ケモテラピー(Metronomic Chemotherapy)では、血管新生が抑制されて抗腫瘍効果を発揮します。低用量の抗がん剤投与は副作用が少なく、免疫系組織の抑制も回避できます。低用量の抗がん剤投与は腫瘍免疫を抑制する制御性T細胞や骨髄由来抑制細胞の活性を阻害する作用があり、その結果、がん細胞を排除する抗腫瘍免疫が増強されます(403話参照)。
メトロノミック・ケモテラピーだけでは抗腫瘍効果に限界があるので、その他の副作用の少ない方法を併用することによって、抗腫瘍効果を高める工夫が必要です。
この場合、がん細胞の特徴(正常細胞との違い)を理解しておくことが重要です。
つまり、がん細胞は①代謝の異常(グルコースの取込みや解糖系や脂肪酸合成の亢進など)、②増殖シグナル伝達系の持続的な活性化、③細胞増殖の抑制や停止の制御系の故障、④アポトーシスに対する抵抗性、⑤無制限の細胞分裂、⑥血管新生の誘導、⑦転移と浸潤などの特徴があります(下図)。

図:がん細胞は正常細胞と異なる特性を多く持っている。このようながん細胞に特徴的な性質をターゲットにするとがん細胞の増殖を抑え、死滅させることができる。
がん細胞の特性をターゲットにして、それを阻害あるいは是正するとがん細胞の増殖を抑制できます。壊れているものを正常にするのは困難ですが、働きが亢進しているものは阻害剤や抑制剤で働きを低下させることができます。
がんの代替医療において、ターゲットとなるものとして、ワールブルグ効果(がん細胞におけるグルコースの取込みと解糖系の亢進)、脂肪酸合成亢進、アポトーシス抵抗性(Bcl-2の発現や活性の亢進)、血管新生(血管内皮細胞増殖因子(VEGF)の産生亢進)、炎症(シクロオキシゲナーゼ-2(COX-2)や活性酸素や炎症性サイトカインの産生増加)、細胞分裂に必要な微小管などがあります(402話参照)。これらのターゲットに作用する既存薬を組み合わせると、副作用が少ない方法でがん細胞の増殖を抑制できます。
肝臓転移した乳がんがメトロノミック・ケモテラピーで長期間生存した症例の報告があります。
Long-term complete response in a patient with liver metastases from breast cancer treated with metronomic chemotherapy.(メトロノミック・ケモテラピーで治療した乳がんの肝臓転移の患者における長期間の完全奏功)Tumori. 100(3):79e-82e.2014年 doi: 10.1700/1578.17238.
【要旨】
背景:幾つかの抗がん剤は低用量で使用すると血管系に作用する可能性が多くの研究で指摘されている。このレポートでは、メトロノミック・ケモテラピーによって長期間に渡ってがんの増殖を抑制できた症例を報告する。
症例提示:患者は62歳の女性で左側の乳がんに対して乳房切除が2007年7月に行われた。肝臓転移に対してファーストラインの抗がん剤治療としてドキソルビシンとパクリタキセルによる21日間サイクルの投与が行われた。6サイクルの治療後のCT検査では部分奏功を認めた。ドキソルビシンとパクリタキセルによる抗がん剤治療を中止し、シクロホスファミド(50mg/日経口)とメソトレキセート(2.5mg x 2回/日、週2日)によるメトロノミック・ケモテラピーに変更した。この維持療法を開始してから6ヶ月後のCT検査で完全奏功を認めた。
患者の原発部位の病理検査で血管内皮増殖因子受容体2(VEGFR2)の過剰発現を認めた。
メトロノミック・ケモテラピーはまだ継続中であるが、60ヶ月経過して現在も完全奏功の状態を維持している。
結論:この症例はメトロノミック・ケモテラピーが維持療法として有効であり、特に毒性(副作用)を認めずに長期間の治療が可能であることを示している。腫瘍におけるVEGFR2の発現量が多い場合は、メトロノミック・ケモテラピーによる血管新生阻害作用が奏功する可能性を示唆する。
完全奏功(complete response)というのは、がん組織が目に見えないレベルに縮小(消滅)することです。顕微鏡レベルで残っている可能性はありますが、がん組織が消滅した状態が続けば延命できます。
メトロノミック・ケモテラピーで著効を示した症例報告や、メトロノミック・ケモテラピーの有効性や通常の抗がん剤治療より有効であることを示す臨床試験の結果も得られています。
最大耐用量を投与する通常の抗がん剤治療は白血病やリンパ腫や精巣腫瘍のような一部のがんには有効ですが、肺がんや膵臓がんや乳がんなど多くの固形がんにはあまり効果がなく、副作用のデメリットの方が高いことが指摘されています。
私自身は、抗がん剤治療の有用性は認めていますが、標準治療で行われている最大耐用量を投与する抗がん剤治療は一部の腫瘍(抗がん剤感受性の高い腫瘍)を除いて、多くの場合間違っているというのが、基本的な立場です。
その主な根拠は、最大耐用量を投与すると一時的には縮小しても、がん組織が傷を受けると正常組織における修復反応と同様に、炎症細胞の浸潤や血管新生が誘導されて、結果的にがん細胞の増殖が促進するからです。
今まで、抗がん剤治療を受けているがん患者さんを多数診てきて、総合的な評価は、標準治療の抗がん剤治療は一時的な縮小を目標にするため、長期の延命はむしろ犠牲にしていると思っています。通常の抗がん剤治療は何もしないよりかは延命していますが、メトロノミック・ケモテラピーや副作用の少ない治療を組み合わせた治療よりも勝っているとは思えないというのが最近の印象です。
前述の論文で使用されているシクロホスファミド(50mg/日経口)とメソトレキセート(2.5mg x 2回/日、週2日)を薬価ベースで計算すると1ヶ月分で約2000円です。この低用量のシクロホスファミド(商品名エンドキサン)とメソトレキセートと使ったメトロノミック・ケモテラピーをベースにして、さらに血管新生阻害、エネルギー産生阻害(グルコース取り込みや解糖系の阻害)、脂肪酸合成やメバロン酸経路の阻害、微小管重合阻害、抗炎症作用などの作用を持った薬などを併用すると、がんの縮小効果を高めることができます。
【臨床例での有効性が報告されている方法を併用する】
がん治療に使える既存の医薬品やサプリメントについては402話や404話で紹介しています。そこでは、2-デオキシグルコース、ジクロロ酢酸ナトリウム、メトホルミン、メベンダゾール、セレコキシブ、サリドマイド、シンバスタチン、ノスカピンなどの既存の医薬品や、アルファリポ酸やヒドロキシクエン酸のようなサプリメントを紹介しています。
その他にもまだ多くの薬があります。例えば、ヒスタミンH2受容体拮抗薬のシメチジンは、大腸がんの手術後に服用して全死亡率を半分に減少させるほどの転移・再発予防効果が臨床試験で明らかになっています。ビタミンD3は1日に2000~4000 国際単位でがん患者の生存率を顕著に高めることが報告されています(394話参照)。
また、漢方薬は、抗炎症、免疫増強、血管新生阻害、脂肪合成阻害などの薬効成分をもった生薬が報告されています。このような薬効を持った生薬を組み合わせた漢方薬も有効です。脂肪酸合成酵素(FAS)の阻害剤ががん治療薬として有望視されていますが、生薬成分中にFAS阻害作用のあるものが多く見つかっています。(FASについては343話参照)
これらを複数組み合わせることによって、がん細胞の増殖を抑制し、延命するという治療戦略は有効です。
【血管新生阻害によるがん細胞の低酸素適応を阻害する方法】
低用量のシクロホスファミドとメソトレキセートを使ったメトロノミック・ケモテラピーは血管新生を阻害してがん細胞の増殖を抑える効果が主体と考えられています。
血管新生が阻害されるとがん組織は酸素不足になって低酸素誘導因子-1(Hypoxia-inducible factor 1; HIF-1)の発現誘導と活性亢進によって、がん細胞は低酸素状態に適応するようになります。
HIF-1は解糖系酵素の産生を増やし、ピルピン酸脱水素酵素キナーゼを活性化してピルビン酸脱水素酵素の活性を阻害し、がん細胞の解糖系代謝を亢進します。HIF-1の活性阻害については364話で解説しています。
HIF-1の活性を阻害する方法としてジクロロ酢酸ナトリウムやジインドリルメタンやメトホルミンなどが有効です。
ジインドリルメタンはHIF-1の発現量を減少させるという報告や、STAT3活性を抑制することによってHIF-1の活性を抑制などの報告があります。
ジクロロ酢酸ナトリウムでピルビン酸脱水素酵素キナーゼを阻害してミトコンドリアを活性化するとがん細胞のHIF-1αシグナル系と血管新生が阻害されることが報告されています。(364話参照)
マウスの移植腫瘍を使った実験で、VEGFに対するモノクローナル抗体のベバシズマブ(アバスチン)投与による低酸素適応をジクロロ酢酸ナトリウムが阻害して、抗腫瘍効果を示す結果も報告されています(以下の論文)。
Dichloroacetate Reverses the Hypoxic Adaptation to Bevacizumab and Enhances its Antitumor Effects in Mouse Xenografts.(マウス移植腫瘍においてベバシズマブに対する低酸素適応をジクロロ酢酸ナトリウムは阻止して抗腫瘍効果を増強する)J Mol Med (Berl). 91(6): 749–758.2013年
この論文では、ベバシズマブ(アバスチン)のような血管新生阻害剤とジクロロ酢酸ナトリウムの併用は相乗的に働いて顕著な抗腫瘍効果を示すことを報告しています。
その他、様々な抗がん剤に対する感受性を高める効果が多数報告されています。
ジクロロ酢酸ナトリウムを服用するとビタミンB1を消耗するので、ビタミンB1を補います。
高用量のビタミンB1はそれだけでジクロロ酢酸ナトリウムと同様の効果(ピルビン酸脱水素酵素の活性化)を示すことが報告されています。(以下の論文)
High-dose vitamin B1 reduces proliferation in cancer cell lines analogous to dichloroacetate. (高用量のビタミンB1はジクロロ酢酸ナトリウムと類似の機序で培養がん細胞株の増殖を低下させる)Cancer Chemother Pharmacol. 2014 Mar;73(3):585-94.
ビタミンB1はピルビン酸脱水素酵素複合体の補酵素として働きます。がん細胞ではピルビン酸脱水素酵素の活性が低下しており、ピルビン酸脱水素酵素の活性を高めるとがん細胞が死にやすくなることが報告されています。この論文では高用量のビタミンB1はジクロロ酢酸ナトリウムと同様にピルビン酸脱水素酵素の活性を高めてがん細胞の増殖を抑制する効果を報告しています。
ピルビン酸脱水素酵素を活性化してミトコンドリアの活性を高める方法として、ジクロロ酢酸ナトリウムの他にR体αリポ酸(265話参照)とビタミンB1が有効です。この3種類を併用するとがん細胞のミトコンドリアの活性を高めて、細胞死を誘導できます。
メトホルミンはミトコンドリアの呼吸酵素複合体1を阻害してATP産生を低下させ、AMP活性化プロテインキナーゼ(AMPK)を活性化することによってHIF-1の活性を抑制する作用があります。
【メトホルミンと2-デオキシグルコース】
ジクロロ酢酸ナトリウムと併用して抗腫瘍効果を高める薬の一つがメトホルミンです。
メトホルミンは2型糖尿病の治療薬ですが、インスリン感受性を高めて血糖を下げる、つまりインスリン分泌を刺激するのではなく分泌を低下させる作用があるので、糖尿病が無くても(血糖値が正常でも)服用できる薬です。
メトホルミンは多彩な作用がありますが、基本はミトコンドリアにおける呼吸酵素複合体1の活性を阻害してATPの産生を低下させる作用と考えられています。
ATPの産生が阻害されるとAMPが増えて、AMP活性化プロテインキナーゼ(AMPK)が活性化され、物質合成(同化)が抑制されて異化が促進されるので、がん細胞の増殖が抑制されます。さらにAMPKには脂肪合成抑制やHIF-1の活性抑制などの作用もあります。
最近の報告では、メトホルミンによってミトコンドリアでのATP産生が低下すると、がん細胞は解糖系でのエネルギー産生を増やす可能性が指摘されています。
したがって、がん細胞の解糖系を阻害する2−デオキシ-D-グルコースやケトン食の併用はメトホルミンの抗腫瘍効果を高めます。
実際に、2−デオキシ-D-グルコースとメトホルミンの併用ががん細胞の増殖抑制やアポトーシス誘導に相乗的に作用することが報告されています。(368話参照)
【メトホルミンとジクロロ酢酸の相乗効果】
メトホルミンとジクロロ酢酸の抗がん作用は併用することによって相乗効果が期待できます。以下のような論文が今月発表されています。
Dichloroacetate enhances apoptotic cell death via oxidative damage and attenuates lactate production in metformin-treated breast cancer cells.(メトホルミンで治療した乳がん細胞において、ジクロロ酢酸は酸化傷害によるアポトーシスを促進し、乳酸産生を低下させる)Breast Cancer Res Treat. 2014 Sep 12. [Epub ahead of print]
【要旨】
乳がん細胞における代謝の特徴を治療に利用することが注目されている。乳がんに対して確実な治療効果を示すことが報告されているメトホルミンはミトコンドリアの呼吸鎖の複合体1を阻害して活性酸素の産生を増やしてがん細胞を死滅させる。
呼吸酵素複合体1を阻害すると、解糖系における乳酸の産生が増える。乳酸の産生増加はがん組織の酸性化などによってがんの治療効果を弱めるので予後を悪くする。
乳酸の産生を抑制すればメトホルミンによるがん細胞のアポトーシス誘導作用は増強されると予想される。乳酸アシドーシスの治療に使われるジクロロ酢酸は、ピルビン酸脱水素酵素キナーゼを阻害することによってピルビン酸脱水素酵素(ピルビン酸をアセチルCoAに変換する酵素)を活性化してミトコンドリアの活性を高める。
そこで、メトホルミンとジクロロ酢酸は乳がん細胞のアポトーシス誘導において相乗効果が得られるかどうかとそのメカニズムを検討した。
実験の結果、ジクロロ酢酸をメトホルミンを併用すると、乳がん細胞のアポトーシス誘導を相乗的に高めることができた。
メトホルミンによる酸化傷害はジクロロ酢酸ナトリウムによって増強され、メトホルミン投与によって誘導される乳酸産生は阻止された。
すなわち、メトホルミンとジクロロ酢酸の併用はがん細胞の酸化傷害を増強し、乳酸の産生を減らし、カスパーゼ依存性のアポトーシスを増強させる。したがって、この組合せは乳がんの治療法として効果が期待できる。
この論文の結果をまとめると以下の図のようになります。

がん細胞では、HIF-1(低酸素誘導因子-1)の作用によって乳酸脱水素酵素やピルビン酸脱水素酵素キナーゼ(ピルビン酸脱水素酵素をリン酸化して阻害する酵素)の活性が亢進しているため、ミトコンドリアでのATP産生は低下し、解糖系が亢進して乳酸の産生が増えています。
メトホルミンはミトコンドリアの呼吸酵素複合体1をターゲットにして阻害するため、ATP産生が阻害され、同時に活性酸素の発生が増えます。活性酸素が増えるとミトコンドリアが破綻して細胞のアポトーシスが起こります。
メトホルミンでミトコンドリアでのATP産生が低下すると、それを代償するために解糖系が亢進し乳酸の産生が増えます。ジクロロ酢酸はピルビン酸脱水素酵素キナーゼを阻害する作用によってピルビン酸脱水素酵素を活性化してミトコンドリアでのTCA回路を回します。その結果、メトホルミンによって生じる乳酸の産生増加が阻止され、ミトコンドリアでの活性酸素の産生が増えて、アポトーシスが増強されます。
また、乳酸の産生が減れば、がん組織の産生化が軽減され、様々なメカニズムでがん細胞の増殖が抑制できます。(359話、403話参照)
つまり、この2つの薬を併用するとがん細胞のアポトーシス誘導が増強されるというメカニズムです。別の研究グループから同様な報告があります。
Sensitization of metformin-cytotoxicity by dichloroacetate via reprogramming glucose metabolism in cancer cells.(がん細胞におけるグルコース代謝の再プログラミングを介するジクロロ酢酸によるメトホルミンの細胞毒性の増強)Cancer Lett. 2014 May 1;346(2):300-8. doi: 10.1016/j.canlet.2014.01.015. Epub 2014 Jan 27.
【要旨】
メトホルミンによる細胞毒性の感受性を高める効果を検討する目的で、がん細胞をピルビン酸脱水素酵素キナーゼの阻害剤であるジクロロ酢酸で処理した。
メトホルミンの細胞毒性は主にグルコースの使用可能性(availability)とペントースリン酸経路によて産生され還元能(NADPH)に依存しているが、ジクロロ酢酸を同時に投与すると、ジクロロ酢酸によるピルビン酸脱水素酵素キナーゼの阻害とミトコンドリアでの呼吸の亢進によってグルコース代謝の再プログラミング(=正常化)が起こり、メトホルミンの細胞毒性が増強される。
グルコースとグルタチオンの濃度が高い状態でも、ジクロロ酢酸の同時投与は細胞死を誘導する。
以上をまとめると、ジクロロ酢酸はグルコース代謝を再プログラミング(正常化)して、好気生解糖からミトコンドリアでの呼吸に変更することによって、メトホルミンの細胞毒性を増強する。
グルコース代謝の再プログラミング(reprogramming)というのは、がん細胞の特徴であるワールブルグ効果(酸素があっても解糖系でのグルコース代謝が亢進し、ミトコンドリアでの代謝が低下している)を正常化(初期化)するということです。ジクロロ酢酸はピルビン酸脱水素酵素キナーゼを阻害してピルビン酸脱水素酵素の活性を高めることによってミトコンドリアでの呼吸(酸素を使ったATP産生)が活性化され、解糖系でのATP産生は抑制されることになります。
一方、メトホルミンはミトコンドリアの呼吸酵素複合体1の働きを阻害するので、ATP産生は阻害され、活性酸素の発生が増加します。
がん細胞ではもともとミトコンドリアでの酸素を使った代謝が低下しているので、メトホルミン単独では細胞を死滅させる作用が弱いのですが、ジクロロ酢酸でミトコンドリアにおける酸素利用を高めれば、がん細胞は酸化傷害によって死滅するというストーリーです。
ここまでをまとめると、メトロノミックケモテラピー(低用量のシクロホスファミドとメソトレキセート)、ジクロロ酢酸ナトリウム、ジインドリルメタン、メトホルミン、2-デオキシグルコースの組合せはがん細胞のエネルギー代謝と血管新生を阻害して腫瘍を縮小する効果が期待できます。さらに、脂肪酸合成を阻害するR体アルファリポ酸やヒドロキシクエン酸やスタチン(404話参照)、微小管形成阻害や血管新生阻害作用などの抗腫瘍効果を示すメベンダゾール(401話参照)、COX-2阻害剤のセレコックス、ヒスタミンH2受容体阻害剤のシメチジンなどを併用するとさらに抗腫瘍効果を高めることができます。(トップの図)
画像をクリックするとサイトに移行します。
| « 404)スタチン... | 406)ケモカイ... » |





