同じ病原体をターゲットにしたワクチンでも、複数の種類が存在するものがあります。
日本で承認されているワクチンで例を挙げると、
(日本脳炎ワクチン)
① ジェービックV®(JEBIK-V:微研)
② エンセバック®(Encevac:KMB)
(四種混合ワクチン)
① スクエアキッズ®(Square kids:第一三共)IPVはSalk株
② テトラビック®(Tetrabik:微研)IPVはSabin株
③ クアトロバック®(Quattrovac:KMB)IPVはSabin株
(B型肝炎ワクチン)
① ビームゲン®(BIMMGEN:KMB)遺伝子型Cワクチン
② ヘプタバックスII®(Heptavac-II:MSD)遺伝子型Aワクチン
(ロタウイルスワクチン)
① ロタリックス®(Rotarix:GSK)2回投与
② ロタテック®(Rotateq:MSD)3回投与
(HPVワクチン)
① サーバリックス®(Cervarix:GSK)
② ガーダシル®(Gardasil:MSD)
※ 略号解説;
(微研)阪大微生物病研究会
(KMB)KMバイオロジクス(旧名:化血研)
(GSK)グラクソ・スミスクライン
(第一三共)第一三共バイオテック(旧名:北里第一三共)
※ ジャパンワクチン(北里第一三共+GSK)は2018年に解散
等々。
すべて不活化ワクチンで、十分な免疫を得る手目には複数回接種する必要があります。
すると、という素朴な疑問が発生します。
「複数回接種の中で、メーカーの異なるワクチンを混在させてもよいか?」
もちろん、可能であれば単一のワクチンで済ませるのが基本ですが、やんごとなき事情もありえます。
実は答えが用意されています。
上記の例では、
(日本脳炎ワクチン)可
(四種混合ワクチン)可
(B型肝炎ワクチン)可
(ロタウイルスワクチン)不可
となっています。
入れ替えても問題ないことを「互換性がある」と表現します。
ロタウイルスワクチンのみ不可で「互換性がない」ということになります。
以上、日本で承認されているワクチンは、互換性の有無が判明しているので、混乱せずに済みます。
海外との出入りが多くなった昨今、日本で生まれて途中で外国へ行く子ども、逆に外国から日本に来る子どもも増えてきました。
そこで新たな疑問が発生しました;
「日本のワクチンと海外のワクチンを同じ物として考えてもよいか?」
日本製ワクチンと外国製ワクチンの互換性については、残念ながら十分な情報がありません。
臨床現場で困っています。
どこかが情報を集めて発信、あるいはネット上で閲覧できるようにして欲しいと常々感じてきました。
そして先日、強力な情報源を見つけました。
「海外渡航者のためのワクチンガイドライン/ガイダンス2019」(協和企画、2019年9月発行)
という本です。
日本渡航医学会が作成し、初版は2010年に発行され、私も所有していますが、ワクチン行政はコロコロ変わるので、内容が古くなって参考になりません。
今回は待望の改訂です。
早速購入して読んでみると・・・その中に、日本製と海外製のワクチン互換性に関する記述を見つけました。
画期的です!
こんな本を待っていました!
日本渡航医学会の先生方、ありがとうございます。
前提として以下の文章から始まります;
「互換性が確認されていない異なる製造会社、異なる抗原のワクチンで接種を継続する場合は、被接種者の感染リスク、希望や予算、エビデンス、ワクチン学の理論、医療者の経験など、限られた情報で最良の選択をするのが現実的であり、判断が困難な場合には専門家への相談が望ましい。
世界標準に近い、アメリカの考え方も参考になります
★ アメリカの考え方
・アメリカでは、同一製造会社の同一成分のワクチンであれば、有効性と安全性の臨床試験に基づいて、単価ワクチンと混合ワクチン(DPT、DPT-IPV、DPT-IPV-Hibなど)は互換性があると考えられている。
・Hib、B型肝炎、A型肝炎、ロタウイルス、4価結合型髄膜炎菌ワクチンは、異なる製造会社での互換性が確認されている。
・互換性が不明である場合は、利用可能なワクチンで接種すべきである。
下線部(私が引きました)の文章は、非常に重みがあります。
さて、私の疑問に関する該当箇所を引用・抜粋させていただき、以下のようにまとめました;
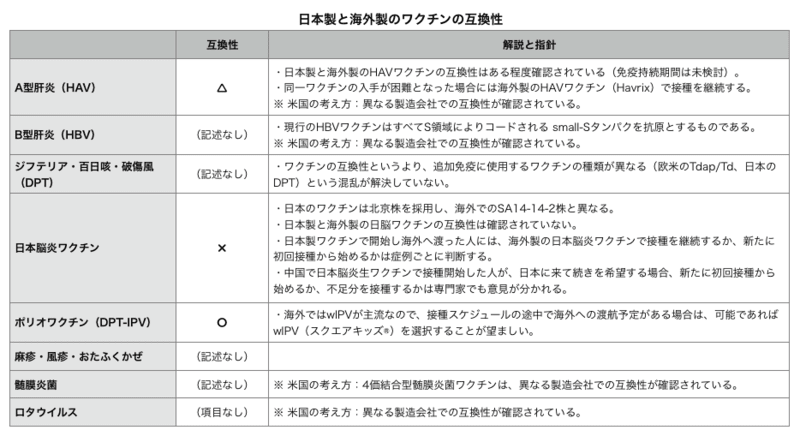
問題になるのは、日本脳炎ワクチン。
接種スケジュールの途中で、日本から海外(主にアジア)へ、あるいは海外から日本へ移動する人に対して、既接種をカウントするか、新たに最初から接種しなおすか、専門家の間でも意見が分かれ、混乱状態のようですね。
他には、A型肝炎ワクチンが△で、短期的な抗体上昇を評価すると互換性がありますが、長期的な免疫持続期間のデータがないという状況です。
(記述なし)のワクチンは、問題ないと考えていいのでしょうか・・・。
<各論>
【A型肝炎(HAV)ワクチン】
(互換性)
・日本製と海外製のHAVワクチンの互換性はある程度確認されている。
・同一ワクチンの入手が困難となった場合には海外製のA型肝炎ワクチン(Havrix)で接種を継続することを提案する(推奨度:2、エビデンスレベル:C)。
(わが国と国際標準との差異)
・エイムゲン®(日本のHAVワクチン)の遺伝子型はIIIB、海外製品の遺伝子型はIA(あるいはB)と異なる。
・エイムゲン®のみ3回接種で、海外ワクチンは2回接種。
・皮下注射はエイムゲン®のみ、海外ワクチンは筋肉内注射。
・海外のHAVワクチン同士では互換性に問題がないことが報告されているが、日本のHAVワクチンと海外のHAVワクチンとの互換性を検討した研究(注1&2)は少ない。
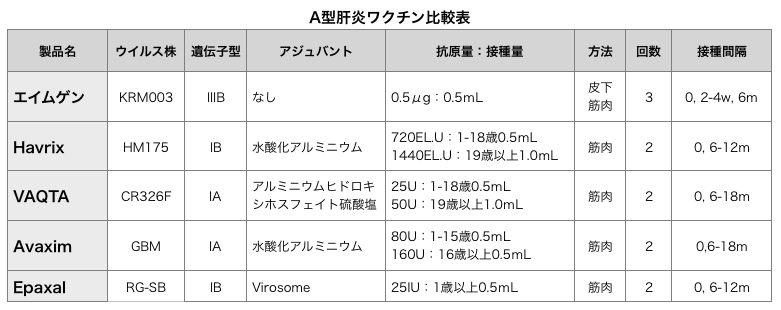
注1)Vaccine. 2017; 35;6412-5
日本製HAVワクチン(エイムゲン)を2回接種した20歳以上の成人20例に対して、米国製HAVワクチン(HAVRIX)を1回追加接種した結果、全例で有効な抗体価上昇が得られた。ただし、免疫持続期間が不明。
注2)日本渡航医会誌 2015; 9: 48-50
エイムゲン®を1回接種してHAVRIXを1回追加接種した成人23例に対し、①エイムゲン®3回、②HAVRIX2回、③エイムゲン®2回、④HAVRIX1回の対照群を比較した結果、各ワクチンの規定回数を完遂した①および②群と同等の抗体価上昇が得られた。ただし免疫持続期間が不明であることが課題である。
【B型肝炎(HBV)ワクチン】
(互換性に関する記述なし)
(参考)現行のHBVワクチン(遺伝子組み換ワクチン)は、すべてS領域によりコードされるsmall-Sタンパクを抗原とするものである。これに対し、Pre-S2とSによりコードされる middle-Sタンパクからなる“Pre-S2含有”ワクチンが開発されたが、現在まで市販されるに至っていない。
【日本脳炎ワクチン】
(互換性)
・日本製と海外製の日本脳炎ワクチンの互換性は確認されていない。
・日本製ワクチン(エンセバック®、ジェービックV®)で接種を開始し海外へ行った人に対し、同一ワクチンの入手が困難となった場合には、海外製の日本脳炎ワクチンで接種を継続するか、最初から接種を開始するか、症例ごとに判断する(推奨度:ー、エビデンスレベル:D)。
・中国で日本脳炎生ワクチン(乙型脳炎減毒活疫苗、SA14-14-2株)を接種した人が、日本で日本製の乾燥細胞培養日本脳炎ワクチン(北京株)で接種を継続する場合は互換性が確認されていないため、新たに初回接種から開始するか、不足分を接種するかは、専門家でも意見が分かれる。前者は過剰接種による副反応を、後者は不十分な免疫獲得を考慮する必要がある。
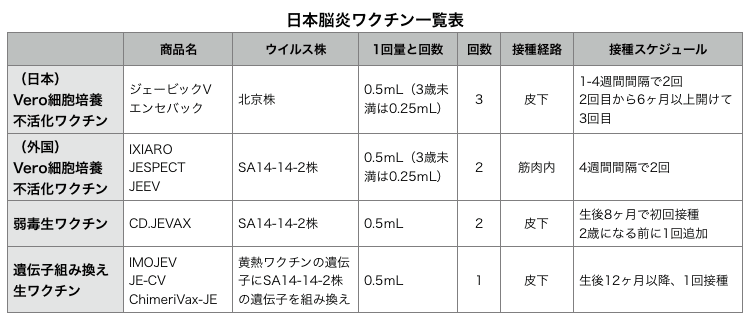
(わが国と国際標準の差異)
・諸外国で流通する日本脳炎不活化ワクチン株はSA14-14-2株で、日本の北京株と異なる。また、日本は皮下注射であるが、諸外国では筋肉内注射である。
・不活化ワクチンは北米、欧州、オーストラリアで流通している。
・生ワクチンは中国、ネパール、インド、スリランカ、韓国などで使用されている。
・中国本土では、中国国産の生ワクチン、不活化ワクチンが流通している。1960年代後半に開発されたラット腎細胞培養不活化ワクチン接種が開始され、2010年まで使用されたが、実際には2004年に開発されたVero細胞由来不活化ワクチンに取って代わられていった。一方、生ワクチンは1988年に流通開始し、現在では韓国やインド、ネパールなどに輸出されている。2007年以降は全省において無償で生ワクチンの接種を受けることができるようになった。不活化ワクチンも接種可能だが、費用は自己負担となる。
・香港ではIMOJEV、IXIAROが、台湾ではIMOJEVが流通している。
・マウス脳由来ワクチン接種後の追加接種としてVero細胞由来不活化ワクチン、弱毒生ワクチン、組み換え生ワクチンを接種した安全性や有効性において特に問題ないとする報告はいくつか確認できる。
・日本国内で遺伝子組み換え生ワクチンを使用すると「カルタヘナ法」に抵触する恐れがある。
【ポリオワクチン/四種混合ワクチン】
(互換性)
・日本ではポリオ生ワクチン(OPV)の生産は2014年に終了した。
・単独の不活化ワクチン(IPV)はイモバックスポリオ®のみであり選択の余地はない。
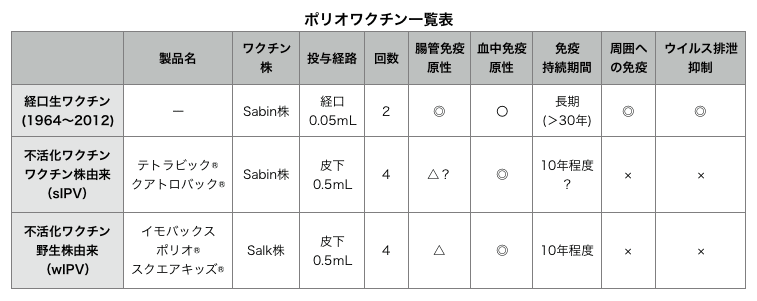
・四種混合ワクチンとして組み込まれているIPVには2種類ある;
(DPT-wIPV)野生株由来のSalk株(wIPV)→ スクエアキッズ®
(DPT-sIPV)ワクチン株由来のSabin株(sIPV)→ テトラビック®、クアトロバック®
・海外ではほぼwIPVなので、接種の途中で海外に渡航予定がある場合は、可能であればwIPVを選択することが望ましい。
※ 本書には記載はないが、DPT-wIPV と DPT-sIPV は互換性があるとされており、混在しても問題ない。
【麻疹・風疹・おたふくかぜワクチン】
(互換性に関する記述なし)
【髄膜炎菌ワクチン】
(互換性に関する記述なし)
(わが国と国際標準の差異)
・髄膜炎菌ワクチンは3種類存在する;①多糖体ワクチン、②結合型ワクチン、③B群に対するワクチン。
・多糖体ワクチンは2歳未満では抗体反応が悪く効果が期待できないため、2歳以上の小児に接種する。このため現在は主に結合型ワクチンが使用されている。
・日本ではメナクトラ®(4価の結合型ワクチン)が2015年から販売されている。添付文書上は、接種対象が限定されていない(日本の臨床試験は2〜55歳対象に実施された)。
日本で承認されているワクチンで例を挙げると、
(日本脳炎ワクチン)
① ジェービックV®(JEBIK-V:微研)
② エンセバック®(Encevac:KMB)
(四種混合ワクチン)
① スクエアキッズ®(Square kids:第一三共)IPVはSalk株
② テトラビック®(Tetrabik:微研)IPVはSabin株
③ クアトロバック®(Quattrovac:KMB)IPVはSabin株
(B型肝炎ワクチン)
① ビームゲン®(BIMMGEN:KMB)遺伝子型Cワクチン
② ヘプタバックスII®(Heptavac-II:MSD)遺伝子型Aワクチン
(ロタウイルスワクチン)
① ロタリックス®(Rotarix:GSK)2回投与
② ロタテック®(Rotateq:MSD)3回投与
(HPVワクチン)
① サーバリックス®(Cervarix:GSK)
② ガーダシル®(Gardasil:MSD)
※ 略号解説;
(微研)阪大微生物病研究会
(KMB)KMバイオロジクス(旧名:化血研)
(GSK)グラクソ・スミスクライン
(第一三共)第一三共バイオテック(旧名:北里第一三共)
※ ジャパンワクチン(北里第一三共+GSK)は2018年に解散
等々。
すべて不活化ワクチンで、十分な免疫を得る手目には複数回接種する必要があります。
すると、という素朴な疑問が発生します。
「複数回接種の中で、メーカーの異なるワクチンを混在させてもよいか?」
もちろん、可能であれば単一のワクチンで済ませるのが基本ですが、やんごとなき事情もありえます。
実は答えが用意されています。
上記の例では、
(日本脳炎ワクチン)可
(四種混合ワクチン)可
(B型肝炎ワクチン)可
(ロタウイルスワクチン)不可
となっています。
入れ替えても問題ないことを「互換性がある」と表現します。
ロタウイルスワクチンのみ不可で「互換性がない」ということになります。
以上、日本で承認されているワクチンは、互換性の有無が判明しているので、混乱せずに済みます。
海外との出入りが多くなった昨今、日本で生まれて途中で外国へ行く子ども、逆に外国から日本に来る子どもも増えてきました。
そこで新たな疑問が発生しました;
「日本のワクチンと海外のワクチンを同じ物として考えてもよいか?」
日本製ワクチンと外国製ワクチンの互換性については、残念ながら十分な情報がありません。
臨床現場で困っています。
どこかが情報を集めて発信、あるいはネット上で閲覧できるようにして欲しいと常々感じてきました。
そして先日、強力な情報源を見つけました。
「海外渡航者のためのワクチンガイドライン/ガイダンス2019」(協和企画、2019年9月発行)
という本です。
日本渡航医学会が作成し、初版は2010年に発行され、私も所有していますが、ワクチン行政はコロコロ変わるので、内容が古くなって参考になりません。
今回は待望の改訂です。
早速購入して読んでみると・・・その中に、日本製と海外製のワクチン互換性に関する記述を見つけました。
画期的です!
こんな本を待っていました!
日本渡航医学会の先生方、ありがとうございます。
前提として以下の文章から始まります;
「互換性が確認されていない異なる製造会社、異なる抗原のワクチンで接種を継続する場合は、被接種者の感染リスク、希望や予算、エビデンス、ワクチン学の理論、医療者の経験など、限られた情報で最良の選択をするのが現実的であり、判断が困難な場合には専門家への相談が望ましい。
世界標準に近い、アメリカの考え方も参考になります
★ アメリカの考え方
・アメリカでは、同一製造会社の同一成分のワクチンであれば、有効性と安全性の臨床試験に基づいて、単価ワクチンと混合ワクチン(DPT、DPT-IPV、DPT-IPV-Hibなど)は互換性があると考えられている。
・Hib、B型肝炎、A型肝炎、ロタウイルス、4価結合型髄膜炎菌ワクチンは、異なる製造会社での互換性が確認されている。
・互換性が不明である場合は、利用可能なワクチンで接種すべきである。
下線部(私が引きました)の文章は、非常に重みがあります。
さて、私の疑問に関する該当箇所を引用・抜粋させていただき、以下のようにまとめました;

問題になるのは、日本脳炎ワクチン。
接種スケジュールの途中で、日本から海外(主にアジア)へ、あるいは海外から日本へ移動する人に対して、既接種をカウントするか、新たに最初から接種しなおすか、専門家の間でも意見が分かれ、混乱状態のようですね。
他には、A型肝炎ワクチンが△で、短期的な抗体上昇を評価すると互換性がありますが、長期的な免疫持続期間のデータがないという状況です。
(記述なし)のワクチンは、問題ないと考えていいのでしょうか・・・。
<各論>
【A型肝炎(HAV)ワクチン】
(互換性)
・日本製と海外製のHAVワクチンの互換性はある程度確認されている。
・同一ワクチンの入手が困難となった場合には海外製のA型肝炎ワクチン(Havrix)で接種を継続することを提案する(推奨度:2、エビデンスレベル:C)。
(わが国と国際標準との差異)
・エイムゲン®(日本のHAVワクチン)の遺伝子型はIIIB、海外製品の遺伝子型はIA(あるいはB)と異なる。
・エイムゲン®のみ3回接種で、海外ワクチンは2回接種。
・皮下注射はエイムゲン®のみ、海外ワクチンは筋肉内注射。
・海外のHAVワクチン同士では互換性に問題がないことが報告されているが、日本のHAVワクチンと海外のHAVワクチンとの互換性を検討した研究(注1&2)は少ない。

注1)Vaccine. 2017; 35;6412-5
日本製HAVワクチン(エイムゲン)を2回接種した20歳以上の成人20例に対して、米国製HAVワクチン(HAVRIX)を1回追加接種した結果、全例で有効な抗体価上昇が得られた。ただし、免疫持続期間が不明。
注2)日本渡航医会誌 2015; 9: 48-50
エイムゲン®を1回接種してHAVRIXを1回追加接種した成人23例に対し、①エイムゲン®3回、②HAVRIX2回、③エイムゲン®2回、④HAVRIX1回の対照群を比較した結果、各ワクチンの規定回数を完遂した①および②群と同等の抗体価上昇が得られた。ただし免疫持続期間が不明であることが課題である。
【B型肝炎(HBV)ワクチン】
(互換性に関する記述なし)
(参考)現行のHBVワクチン(遺伝子組み換ワクチン)は、すべてS領域によりコードされるsmall-Sタンパクを抗原とするものである。これに対し、Pre-S2とSによりコードされる middle-Sタンパクからなる“Pre-S2含有”ワクチンが開発されたが、現在まで市販されるに至っていない。
【日本脳炎ワクチン】
(互換性)
・日本製と海外製の日本脳炎ワクチンの互換性は確認されていない。
・日本製ワクチン(エンセバック®、ジェービックV®)で接種を開始し海外へ行った人に対し、同一ワクチンの入手が困難となった場合には、海外製の日本脳炎ワクチンで接種を継続するか、最初から接種を開始するか、症例ごとに判断する(推奨度:ー、エビデンスレベル:D)。
・中国で日本脳炎生ワクチン(乙型脳炎減毒活疫苗、SA14-14-2株)を接種した人が、日本で日本製の乾燥細胞培養日本脳炎ワクチン(北京株)で接種を継続する場合は互換性が確認されていないため、新たに初回接種から開始するか、不足分を接種するかは、専門家でも意見が分かれる。前者は過剰接種による副反応を、後者は不十分な免疫獲得を考慮する必要がある。

(わが国と国際標準の差異)
・諸外国で流通する日本脳炎不活化ワクチン株はSA14-14-2株で、日本の北京株と異なる。また、日本は皮下注射であるが、諸外国では筋肉内注射である。
・不活化ワクチンは北米、欧州、オーストラリアで流通している。
・生ワクチンは中国、ネパール、インド、スリランカ、韓国などで使用されている。
・中国本土では、中国国産の生ワクチン、不活化ワクチンが流通している。1960年代後半に開発されたラット腎細胞培養不活化ワクチン接種が開始され、2010年まで使用されたが、実際には2004年に開発されたVero細胞由来不活化ワクチンに取って代わられていった。一方、生ワクチンは1988年に流通開始し、現在では韓国やインド、ネパールなどに輸出されている。2007年以降は全省において無償で生ワクチンの接種を受けることができるようになった。不活化ワクチンも接種可能だが、費用は自己負担となる。
・香港ではIMOJEV、IXIAROが、台湾ではIMOJEVが流通している。
・マウス脳由来ワクチン接種後の追加接種としてVero細胞由来不活化ワクチン、弱毒生ワクチン、組み換え生ワクチンを接種した安全性や有効性において特に問題ないとする報告はいくつか確認できる。
・日本国内で遺伝子組み換え生ワクチンを使用すると「カルタヘナ法」に抵触する恐れがある。
【ポリオワクチン/四種混合ワクチン】
(互換性)
・日本ではポリオ生ワクチン(OPV)の生産は2014年に終了した。
・単独の不活化ワクチン(IPV)はイモバックスポリオ®のみであり選択の余地はない。
・四種混合ワクチンとして組み込まれているIPVには2種類ある;
(DPT-wIPV)野生株由来のSalk株(wIPV)→ スクエアキッズ®
(DPT-sIPV)ワクチン株由来のSabin株(sIPV)→ テトラビック®、クアトロバック®
・海外ではほぼwIPVなので、接種の途中で海外に渡航予定がある場合は、可能であればwIPVを選択することが望ましい。
※ 本書には記載はないが、DPT-wIPV と DPT-sIPV は互換性があるとされており、混在しても問題ない。

【麻疹・風疹・おたふくかぜワクチン】
(互換性に関する記述なし)
【髄膜炎菌ワクチン】
(互換性に関する記述なし)
(わが国と国際標準の差異)
・髄膜炎菌ワクチンは3種類存在する;①多糖体ワクチン、②結合型ワクチン、③B群に対するワクチン。
・多糖体ワクチンは2歳未満では抗体反応が悪く効果が期待できないため、2歳以上の小児に接種する。このため現在は主に結合型ワクチンが使用されている。
・日本ではメナクトラ®(4価の結合型ワクチン)が2015年から販売されている。添付文書上は、接種対象が限定されていない(日本の臨床試験は2〜55歳対象に実施された)。















