今回のキーワードは,ワクチン接種者へのインセンティブ,アストラゼネカワクチン変異株に予防効果なし,神経疾患に対するワクチンの考え方,入院患者の後遺症としての認知機能障害の頻度38%!,持続脳波モニタリング異常は予後不良,COVID-19に伴う急性虚血性脳卒中の特徴,多発性硬化症における予後予測因子,ICU患者に対する標準量以上の予防的抗凝固療法は支持されない,です.
緊急事態宣言が解除されることになり,対策の5本柱(①飲食店対策,②変異ウイルス対策,③PCR検査の強化,④ワクチン接種の推進,⑤医療提供体制の充実)が発表されましたが,第4波への不安を感じた人が多いのではないでしょうか.「数値」や「期限」といった目標が不明確であることが一因ではないかと思います.目標設定の基本は「SMARTの法則」,すなわちSpecific(具体的で),Measurable(測定可能で),Assignable(役割や権限の割り当てができていて),Realistic(現実的な目標であり),Time-related(期限が設定されている)という5つの因子を考えて初めて,目標達成の可能性を最大限に高めることができます.例えば④ワクチン接種の推進では,次に示すイスラエルのような具体的な戦略が必要になってきます.
◆ワクチン接種を促進するイスラエルにおける「グリーンパス」.
人口930万人のイスラエルでは,ファイザーワクチンの十分な供給を受け,2020年12月20日に接種を開始し,2021年2月20日までに,16歳以上の国民の40%,60歳以上の国民の80%以上が2回のワクチン接種を受けた.また接種率を高めるためのインセンティブモデルとして「グリーンパス」が導入された(図1;写真はJapanTimesより).2回目の接種から1週間経過したなど,免疫を獲得した個人に対して,社会的,文化的,スポーツ的なイベントや,ジム,ホテル,レストランへの入場を6ヶ月間に限定して許可するというものだ.COVID-19確定患者と接触した後や,海外旅行から帰国した後,10~14日間の隔離も免除される.この政策の目的は,集団免疫に達するのに十分な割合である「全国民の95%の接種率」を達成しようとするものである.ただしワクチン接種の有無による差別につながりうるという倫理的・法的問題があり,賛否両論がある.いずれにしてもイスラエルは,より高い接種率を達成するためのインセンティブ制度を開発したい他国にとって有益な情報となる.→ 日本でも,接種率向上のためのインセンティブモデルについて議論を早く開始する必要がある.
JAMA. March 15, 2021.(doi.org/10.1001/jama.2021.4300)

◆アストラゼネカワクチンに変異株B.1.351に対する予防効果なし.
南アフリカで最初に確認されたB.1.351(501Y.V2)変異株を含む,新たな変異株に対するワクチンの有効性を検討した研究が報告された.アストラゼネカのChAdOx1 nCoV-19ワクチン(AZD1222)の安全性と有効性を評価するため,南アフリカにおいて多施設共同二重盲検無作為化対照試験が実施された.18歳から65歳未満の参加者に対し,ワクチンまたは偽薬を21~35日の間隔で2回接種するよう1:1に割り付けた.主要評価項目の解析では,軽度から中等度の COVID-19が,偽薬接種者で23/717 名(3.2%),ワクチン接種者で19/750 名(2.5%)に認められ,有効率は 21.9%と低かった(図2).42名のCOVID-19のうち,39名(92.9%)がB.1.351変異株によるもので,副次評価項目として解析したこの変異株に対するワクチンの有効性は10.4%であった.重篤な有害事象の発生率は,両群で同等であった.アストラゼネカワクチンを 2 回接種しても,B.1.351 変異株による軽度から中等度の COVID-19に対する予防効果は認められない.
New Engl J Med. March 16, 2021(doi.org/10.1056/NEJMoa2102214)

◆神経疾患に対するワクチンの考え方.
米国神経学会(American Neurological Association;ANA)がワクチンに関する疑問を米国国立神経疾患・脳卒中研究所(NINDS)のAvindra Nath博士に質問した内容がAnn Neurol誌に掲載されている.重要な点を抜き出す.
1.COVID-19ワクチン接種を禁忌とする神経疾患はない.
2.免疫抑制剤使用中の患者では,COVID-19罹患後の重症化リスクが高くなる可能性がある.よってこれらの患者ではワクチン接種は特に重要となる.
3.免疫抑制剤の中には,ワクチン抗原に対する免疫反応を減弱するものもある.これらの患者では,ワクチンの接種時期が重要である.多発性硬化症患者に対する最近のガイドラインでは,免疫反応を最大化するため,接種タイミングを治療開始前または治療サイクルの終了間際にすることが推奨されている.
4.個人レベルでも集団レベルでも,ワクチン接種のメリットは,神経系の副反応をきたすリスクをはるかに上回る.ただしワクチンと神経系の副反応との関連を明らかにするためには,前向き研究が必要である.
Ann Neurol. March 12, 2021(doi.org/10.1002/ana.26065)
◆入院患者の後遺症としての認知機能障害の頻度は38%!
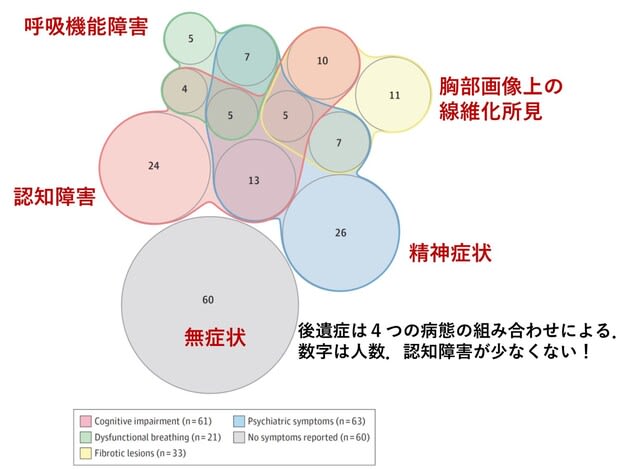
フランスから,2020年3月から5月までに大学病院に入院したCOVID-19患者の4ヵ月後の状況が報告された.対象となる834名のうち,478名(平均年齢61歳)が電話による調査を受けた.244名の患者(51%)が罹患前になかった症状を少なくとも1つ申告した,その内訳は疲労が31%,認知機能に関する訴えが21%,新たに発症した呼吸困難が16%であった.177名の患者(37%)にはさらなる評価が行われた.20項目のMultidimensional Fatigue Inventoryスコア(n=130)の中央値は,意欲の低下が4.5,精神的疲労が3.7であった(1が最高,5が最悪).108/171名(63%)の患者に胸部CTでの肺の異常所見を認めた.MoCAにより評価した認知機能障害は61/159名(38.4%)に認められた(図3).元ICU患者94名では,不安,抑うつ,心的外傷後の症状がそれぞれ23%,18%,7%に認められた.→ 認知機能障害の合併頻度が高く,かなりショッキングなデータと言える.
JAMA. Mar 17, 2021(doi.org/10.1001/jama.2021.3331)
◆持続脳波モニタリングの異常所見は予後不良予測因子である.
米国からの報告.連続脳波モニタリングを受けたCOVID-19患者197名において,脳波異常の有病率と予後不良予測因子を後方視的に検討した論文が報告された.結果として,脳波異常をみとめるけいれん発作は19名(9.6%)に認められ,そのうち11名(5.6%)は非痙攣性てんかん重積発作(NCSE)であった.またてんかん性脳波異常を96名(48.7%)に認めた(発作時もしくは発作間欠期).画像上の既存の頭蓋内病変は,NCSEと関連していた(14.3%対3.7%,オッズ比4.33,p=0.02).多変量解析では,脳波異常をみとめるけいれん発作は,院内死亡の独立した予測因子であった(ハザード比4.06,p<0.01)(図4).競合リスク分析では,NCSEを認めると,入院期間が長期化した(30日後の退院率は,NCSEありvs.なし:0.21対0.43).以上より,持続脳波を評価するようなCOVID-19患者において,てんかん性脳波異常は約半数に認められ,かつ不良な予後と関連していた.
Ann Neurol. March 11, 2021(doi.org/10.1002/ana.26060)

◆COVID-19に伴う急性虚血性脳卒中の特徴.
COVID-19患者における急性虚血性脳卒中(AIS)の合併は予後不良であるという既報がある.米国の458病院から,2020年2月~6月に入院したAIS患者4万1971名(COVID-19あり:1143名,COVID-19なし:4万828名)を特定し,臨床的特徴,治療,転帰を比較した研究が報告された.COVID-19群では,COVID-19なし群と比較して,若く,黒人,ヒスパニック系,アジア人である可能性が高く,NIHSSスコアが高く,大血管閉塞の割合が高かった.血栓溶解療法と血栓回収術の実施率は両群間で同等であった.COVID-19群では,CT撮影までの時間(中央値55分 vs 35分,P<0.001),穿刺までの時間(中央値59分 vs 46分,P<0.001),血管内治療までの時間(中央値114分 vs 90分,P=0.002)が長かった.調整モデルでは,COVID-19群は,modified Rankin Scaleスコアが 2 以下で退院するオッズが低く(オッズ比,0.65,P<0.001),院内死亡のオッズが高かった(オッズ比,4.34,P<0.001).以上より, COVID-19患者におけるAISは,通常のものと比べて,年齢が若く,脳卒中の重症度が高く,評価と治療に要する時間が長く,罹患率と死亡率が不良であることが分かった.
Stroke. Mar 17, 2021(doi.org/10.1161/STROKEAHA.121.034301)
◆多発性硬化症における予後予測因子.
多発性硬化症(MS)におけるCOVID-19感染後の危険因子について,北米の大規模コホート研究(COVID-19 Infections in MS Registry)が報告された.重症度は4段階に分類した(入院不要,入院のみ,ICU/人工呼吸器装着,死亡).患者1626名のうち,1345名(82.7%)がPCR陽性,残りは臨床的にCOVID-19が強く疑われる症例であった.女性が74.0%,平均年齢47.7歳,再発寛解型MSが80.4%であった.全体の死亡率は3.3%.歩行障害と高齢であることは,入院不要の患者と比較して,すべての臨床的重症度のオッズの上昇と関連していた(歩行障害:入院のみ,オッズ比2.8,ICU /人工呼吸器3.5,死亡25.4,年齢[10年ごと]:入院のみ1.3,ICU /人工呼吸器1.3,死亡1.8).年齢が10歳上がるごとに,入院のみ,ICU/人工呼吸器のリスクが各々30%増加し,死亡リスクは76.5%も増加した.男性は,入院リスクが41%,死亡リスクが3倍以上増加した.心血管疾患は入院リスクを91%,死亡リスクを3倍以上増加させた.疾患修飾薬の使用のない患者と比較し,リツキシマブは入院リスクを4.5倍増加させたが,他の重症度とは関連なし.オクレリズマブ(CD20 モノクローナル抗体)は入院リスクをわずかに上昇させた(1.63).フマル酸塩とナタリズマブは,それぞれICU/人工呼吸器リスクを低下させた.過去2カ月間のグルココルチコイドの使用は,入院リスクを約2倍,死亡リスクを4倍に増加させた.
JAMA Neurol. March 19, 2021(doi.org/10.1001/jamaneurol.2021.0688)
◆ICU患者に対する標準量以上の予防的抗凝固療法は支持されない.
重症COVID-19では血栓症がしばしば認められる.これに対して標準量を超える容量の抗凝固薬が経験的に使用されることがあるが,その有効性のエビデンスは十分ではない.イランから,ICUに入院した患者を対象に,中等量(エノキサパリン=クレキサン®,1 mg/kg/日)(n = 276)と,標準量(エノキサパリン,40 mg/日,体重とクレアチニンクリアランスに応じて調整)(n = 286)の予防的抗凝固療法を比較した研究が報告された.主要評価項目は,静脈または動脈血栓症,ECMOによる治療,または 30 日以内の死亡率の複合とした.対象は562名であった.主要評価項目は,中間用量投与群では126名(45.7%),標準用量投与群では126名(44.1%)に発生した(絶対リスク差,1.5%,オッズ比1.06,P = 0.70)(図5).大出血は,中間用量投与群で2.5%,標準用量群で1.4%に発生し(リスク差,1.1%;オッズ比,1.83),非劣性基準を満たさなかった.重度の血小板減少症は,中用量群でのみ発生した(6例対0例,P = 0.01).以上より,ICU入院COVID-19患者に対して,中等量の予防的抗凝固療法は支持されない.
JAMA. March 18, 2021. doi:10.1001/jama.2021.4152

緊急事態宣言が解除されることになり,対策の5本柱(①飲食店対策,②変異ウイルス対策,③PCR検査の強化,④ワクチン接種の推進,⑤医療提供体制の充実)が発表されましたが,第4波への不安を感じた人が多いのではないでしょうか.「数値」や「期限」といった目標が不明確であることが一因ではないかと思います.目標設定の基本は「SMARTの法則」,すなわちSpecific(具体的で),Measurable(測定可能で),Assignable(役割や権限の割り当てができていて),Realistic(現実的な目標であり),Time-related(期限が設定されている)という5つの因子を考えて初めて,目標達成の可能性を最大限に高めることができます.例えば④ワクチン接種の推進では,次に示すイスラエルのような具体的な戦略が必要になってきます.
◆ワクチン接種を促進するイスラエルにおける「グリーンパス」.
人口930万人のイスラエルでは,ファイザーワクチンの十分な供給を受け,2020年12月20日に接種を開始し,2021年2月20日までに,16歳以上の国民の40%,60歳以上の国民の80%以上が2回のワクチン接種を受けた.また接種率を高めるためのインセンティブモデルとして「グリーンパス」が導入された(図1;写真はJapanTimesより).2回目の接種から1週間経過したなど,免疫を獲得した個人に対して,社会的,文化的,スポーツ的なイベントや,ジム,ホテル,レストランへの入場を6ヶ月間に限定して許可するというものだ.COVID-19確定患者と接触した後や,海外旅行から帰国した後,10~14日間の隔離も免除される.この政策の目的は,集団免疫に達するのに十分な割合である「全国民の95%の接種率」を達成しようとするものである.ただしワクチン接種の有無による差別につながりうるという倫理的・法的問題があり,賛否両論がある.いずれにしてもイスラエルは,より高い接種率を達成するためのインセンティブ制度を開発したい他国にとって有益な情報となる.→ 日本でも,接種率向上のためのインセンティブモデルについて議論を早く開始する必要がある.
JAMA. March 15, 2021.(doi.org/10.1001/jama.2021.4300)

◆アストラゼネカワクチンに変異株B.1.351に対する予防効果なし.
南アフリカで最初に確認されたB.1.351(501Y.V2)変異株を含む,新たな変異株に対するワクチンの有効性を検討した研究が報告された.アストラゼネカのChAdOx1 nCoV-19ワクチン(AZD1222)の安全性と有効性を評価するため,南アフリカにおいて多施設共同二重盲検無作為化対照試験が実施された.18歳から65歳未満の参加者に対し,ワクチンまたは偽薬を21~35日の間隔で2回接種するよう1:1に割り付けた.主要評価項目の解析では,軽度から中等度の COVID-19が,偽薬接種者で23/717 名(3.2%),ワクチン接種者で19/750 名(2.5%)に認められ,有効率は 21.9%と低かった(図2).42名のCOVID-19のうち,39名(92.9%)がB.1.351変異株によるもので,副次評価項目として解析したこの変異株に対するワクチンの有効性は10.4%であった.重篤な有害事象の発生率は,両群で同等であった.アストラゼネカワクチンを 2 回接種しても,B.1.351 変異株による軽度から中等度の COVID-19に対する予防効果は認められない.
New Engl J Med. March 16, 2021(doi.org/10.1056/NEJMoa2102214)

◆神経疾患に対するワクチンの考え方.
米国神経学会(American Neurological Association;ANA)がワクチンに関する疑問を米国国立神経疾患・脳卒中研究所(NINDS)のAvindra Nath博士に質問した内容がAnn Neurol誌に掲載されている.重要な点を抜き出す.
1.COVID-19ワクチン接種を禁忌とする神経疾患はない.
2.免疫抑制剤使用中の患者では,COVID-19罹患後の重症化リスクが高くなる可能性がある.よってこれらの患者ではワクチン接種は特に重要となる.
3.免疫抑制剤の中には,ワクチン抗原に対する免疫反応を減弱するものもある.これらの患者では,ワクチンの接種時期が重要である.多発性硬化症患者に対する最近のガイドラインでは,免疫反応を最大化するため,接種タイミングを治療開始前または治療サイクルの終了間際にすることが推奨されている.
4.個人レベルでも集団レベルでも,ワクチン接種のメリットは,神経系の副反応をきたすリスクをはるかに上回る.ただしワクチンと神経系の副反応との関連を明らかにするためには,前向き研究が必要である.
Ann Neurol. March 12, 2021(doi.org/10.1002/ana.26065)
◆入院患者の後遺症としての認知機能障害の頻度は38%!
フランスから,2020年3月から5月までに大学病院に入院したCOVID-19患者の4ヵ月後の状況が報告された.対象となる834名のうち,478名(平均年齢61歳)が電話による調査を受けた.244名の患者(51%)が罹患前になかった症状を少なくとも1つ申告した,その内訳は疲労が31%,認知機能に関する訴えが21%,新たに発症した呼吸困難が16%であった.177名の患者(37%)にはさらなる評価が行われた.20項目のMultidimensional Fatigue Inventoryスコア(n=130)の中央値は,意欲の低下が4.5,精神的疲労が3.7であった(1が最高,5が最悪).108/171名(63%)の患者に胸部CTでの肺の異常所見を認めた.MoCAにより評価した認知機能障害は61/159名(38.4%)に認められた(図3).元ICU患者94名では,不安,抑うつ,心的外傷後の症状がそれぞれ23%,18%,7%に認められた.→ 認知機能障害の合併頻度が高く,かなりショッキングなデータと言える.
JAMA. Mar 17, 2021(doi.org/10.1001/jama.2021.3331)

◆持続脳波モニタリングの異常所見は予後不良予測因子である.
米国からの報告.連続脳波モニタリングを受けたCOVID-19患者197名において,脳波異常の有病率と予後不良予測因子を後方視的に検討した論文が報告された.結果として,脳波異常をみとめるけいれん発作は19名(9.6%)に認められ,そのうち11名(5.6%)は非痙攣性てんかん重積発作(NCSE)であった.またてんかん性脳波異常を96名(48.7%)に認めた(発作時もしくは発作間欠期).画像上の既存の頭蓋内病変は,NCSEと関連していた(14.3%対3.7%,オッズ比4.33,p=0.02).多変量解析では,脳波異常をみとめるけいれん発作は,院内死亡の独立した予測因子であった(ハザード比4.06,p<0.01)(図4).競合リスク分析では,NCSEを認めると,入院期間が長期化した(30日後の退院率は,NCSEありvs.なし:0.21対0.43).以上より,持続脳波を評価するようなCOVID-19患者において,てんかん性脳波異常は約半数に認められ,かつ不良な予後と関連していた.
Ann Neurol. March 11, 2021(doi.org/10.1002/ana.26060)

◆COVID-19に伴う急性虚血性脳卒中の特徴.
COVID-19患者における急性虚血性脳卒中(AIS)の合併は予後不良であるという既報がある.米国の458病院から,2020年2月~6月に入院したAIS患者4万1971名(COVID-19あり:1143名,COVID-19なし:4万828名)を特定し,臨床的特徴,治療,転帰を比較した研究が報告された.COVID-19群では,COVID-19なし群と比較して,若く,黒人,ヒスパニック系,アジア人である可能性が高く,NIHSSスコアが高く,大血管閉塞の割合が高かった.血栓溶解療法と血栓回収術の実施率は両群間で同等であった.COVID-19群では,CT撮影までの時間(中央値55分 vs 35分,P<0.001),穿刺までの時間(中央値59分 vs 46分,P<0.001),血管内治療までの時間(中央値114分 vs 90分,P=0.002)が長かった.調整モデルでは,COVID-19群は,modified Rankin Scaleスコアが 2 以下で退院するオッズが低く(オッズ比,0.65,P<0.001),院内死亡のオッズが高かった(オッズ比,4.34,P<0.001).以上より, COVID-19患者におけるAISは,通常のものと比べて,年齢が若く,脳卒中の重症度が高く,評価と治療に要する時間が長く,罹患率と死亡率が不良であることが分かった.
Stroke. Mar 17, 2021(doi.org/10.1161/STROKEAHA.121.034301)
◆多発性硬化症における予後予測因子.
多発性硬化症(MS)におけるCOVID-19感染後の危険因子について,北米の大規模コホート研究(COVID-19 Infections in MS Registry)が報告された.重症度は4段階に分類した(入院不要,入院のみ,ICU/人工呼吸器装着,死亡).患者1626名のうち,1345名(82.7%)がPCR陽性,残りは臨床的にCOVID-19が強く疑われる症例であった.女性が74.0%,平均年齢47.7歳,再発寛解型MSが80.4%であった.全体の死亡率は3.3%.歩行障害と高齢であることは,入院不要の患者と比較して,すべての臨床的重症度のオッズの上昇と関連していた(歩行障害:入院のみ,オッズ比2.8,ICU /人工呼吸器3.5,死亡25.4,年齢[10年ごと]:入院のみ1.3,ICU /人工呼吸器1.3,死亡1.8).年齢が10歳上がるごとに,入院のみ,ICU/人工呼吸器のリスクが各々30%増加し,死亡リスクは76.5%も増加した.男性は,入院リスクが41%,死亡リスクが3倍以上増加した.心血管疾患は入院リスクを91%,死亡リスクを3倍以上増加させた.疾患修飾薬の使用のない患者と比較し,リツキシマブは入院リスクを4.5倍増加させたが,他の重症度とは関連なし.オクレリズマブ(CD20 モノクローナル抗体)は入院リスクをわずかに上昇させた(1.63).フマル酸塩とナタリズマブは,それぞれICU/人工呼吸器リスクを低下させた.過去2カ月間のグルココルチコイドの使用は,入院リスクを約2倍,死亡リスクを4倍に増加させた.
JAMA Neurol. March 19, 2021(doi.org/10.1001/jamaneurol.2021.0688)
◆ICU患者に対する標準量以上の予防的抗凝固療法は支持されない.
重症COVID-19では血栓症がしばしば認められる.これに対して標準量を超える容量の抗凝固薬が経験的に使用されることがあるが,その有効性のエビデンスは十分ではない.イランから,ICUに入院した患者を対象に,中等量(エノキサパリン=クレキサン®,1 mg/kg/日)(n = 276)と,標準量(エノキサパリン,40 mg/日,体重とクレアチニンクリアランスに応じて調整)(n = 286)の予防的抗凝固療法を比較した研究が報告された.主要評価項目は,静脈または動脈血栓症,ECMOによる治療,または 30 日以内の死亡率の複合とした.対象は562名であった.主要評価項目は,中間用量投与群では126名(45.7%),標準用量投与群では126名(44.1%)に発生した(絶対リスク差,1.5%,オッズ比1.06,P = 0.70)(図5).大出血は,中間用量投与群で2.5%,標準用量群で1.4%に発生し(リスク差,1.1%;オッズ比,1.83),非劣性基準を満たさなかった.重度の血小板減少症は,中用量群でのみ発生した(6例対0例,P = 0.01).以上より,ICU入院COVID-19患者に対して,中等量の予防的抗凝固療法は支持されない.
JAMA. March 18, 2021. doi:10.1001/jama.2021.4152


























