今回のキーワードは,COVID-19は自己免疫性疾患の発症リスクを上昇させ,ワクチン接種はリスクを軽減する,COVID-19後の認知症候群は記憶障害と注意・遂行障害を,疲労,不安,うつとともに認める,入院患者の認知機能障害を予測する血液バイオマーカーが2つ同定された,オミクロン株によるlong COVIDの発症率は18.2%である,long COVIDの有力な病態機序としてミトコンドリア障害が明らかにされた,Long COVIDの発症の有無に,急性期のSARS-CoV-2抗体価やT細胞免疫の差は無関係である,です.
COVID-19に伴う2型糖尿病の発症リスク増加とワクチンによる抑制が報告されていますが,自己免疫性疾患のリスクも増加し,多発性硬化症ではハザード比2.66,抗リン脂質抗体症候群2.12,免疫介在性血小板減少症2.10などと報告されました.これらもワクチン接種により抑制できます.またオミクロン株によるlong COVIDの罹患率もワクチンの接種回数が少ないと上昇することも報告されました.ワクチンは一部のひとには重篤な副反応を起こしてしまいますが,集団で見るとこれらのような明らかな効果があります.現在,第9波が猛威を振るっています.最新の正しい情報を理解して,ワクチンを接種するかどうかを判断する必要があります.
またフォーローしてきたCOVID-19後の認知障害もいよいよスコーピングレビューが発表され,「記憶障害と注意・遂行障害を,疲労,不安,うつとともに認める」という臨床像が明確になってきました.フィブリノゲンとD-ダイマーが入院患者の認知症発症リスクを予測できることも判明しましたので,臨床現場で評価し,その後の対応に役立てることができそうです.
◆COVID-19は自己免疫性疾患の発症リスクを上昇させ,ワクチン接種はリスクを軽減する.
香港からCOVID-19と自己免疫疾患の関連,およびCOVID-19ワクチン接種の予防効果を検討した後方視的コホート研究が報告された.対象はCOVID-19患者102万8721人と非COVID患者316万8467人であった.調整ハザード比は,多発性硬化症2.66,類天疱瘡2.39,抗リン脂質抗体症候群2.12,免疫介在性血小板減少症2.10,悪性貧血1.72,血管炎1.46,乾癬1.42,脊椎関節炎1.32,バセドウ病1.30であった(いずれも有意差あり)(図1).またワクチンの2回接種は,類天疱瘡,抗リン脂質抗体症候群,免疫介在性血小板減少症,バセドウ病,自己免疫性関節炎のリスクを減少させた.以上より,COVID-19は様々な自己免疫性疾患の発症リスクの上昇と関連し,そのリスクはワクチン接種によって軽減される可能性が示唆された.
eClinMed. August 16, 2023(doi.org/10.1016/j.eclinm.2023.102154)

◆COVID-19後の認知症候群は,記憶障害と注意・遂行障害を,疲労,不安,うつとともに認める.
イタリアからCOVID-19患者に伴う認知機能障害に関するスコーピングレビューが報告された.180件の研究が対象となったが,うち3分の1のみが認知機能障害の定義を行っていた.最も多く報告された認知機能障害は,前向性記憶障害>注意・遂行障害>ブレインフォグで(図2),精神症状ではうつ,不安,睡眠障害であった.ほとんどの研究で全身症状として疲労を認めていた.36の研究では認知機能検査が行われていたが,認知機能障害は被験者の39%に認められ,最も頻度の高い領域は注意・遂行機能(90%)と記憶(67%)であった.またCOVID-19罹患後の認知症候群の病名に関する合意は得られていなかった.症状発現の時期やその持続期間についてはまだ議論が続いている.症状に関する客観的評価方法もまだ標準化されていない.
Eur J Neurol. 2023 Aug 4.(doi.org/10.1111/ene.16027)

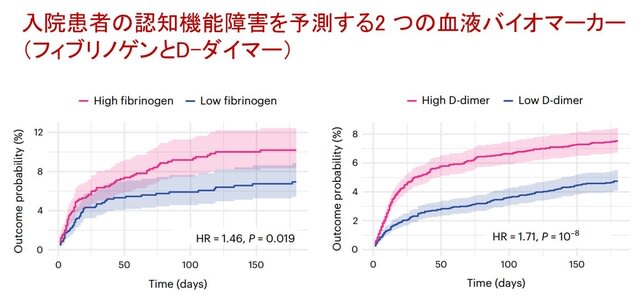
◆入院患者の認知機能障害を予測する血液バイオマーカーが2つ同定された.
英国から,2020年1月から2021年11月までにCOVID-19により入院した1837人を調べ,認知機能障害発症に関与する血液バイオマーカーを検討した研究が報告された.認知機能に対する医師による客観的評価と患者による主観的評価は,6カ月後と12カ月後に行われた.この結果,2種類の血液バイオマーカーが特定された.1つ目は,CRPに対するフィブリノゲンの上昇で,客観的認知障害と主観的認知障害の両方と相関した.2つ目は,CRPに対するDダイマーの上昇で,主観的な認知障害だけでなく,疲労や息切れとも関連があった.これらの知見は,米国で1万7911人の電子カルテを用いて行われた別のコホートでも確認された(図3).メカニズムとして,前者は炎症物質としての直接作用(フィブリノゲンは急性相タンパク質のひとつ)や過凝固状態が,後者は脳や肺血管の微小血栓が関与している可能性が推測される.
Nat Med (2023). https://doi.org/10.1038/s41591-023-02525-y
◆オミクロン株によるlong COVIDの発症率は18.2%である.
オーストラリアから,ワクチン接種を行っている集団におけるlong COVIDの特徴を明らかにした研究が報告された.2022年7月~8月にオーストラリアで実施されたオミクロン株感染者1万1697人(94.0%が3回以上ワクチン接種)の90日後の追跡調査を行った.Long COVIDの基準を満たしたのは18.2%で,中央値で6つの症状を報告し,疲労(70.6%),ブレインフォグ(59.6%),記憶障害・混乱(32.5%)が多かった.17.9%が就労/就学困難であった.Long COVIDの予測因子は,女性,50~69歳,既往症,ワクチン接種回数が少ないことであった.
medRxiv. August 09, 2023.(doi.org/10.1101/2023.08.06.23293706)
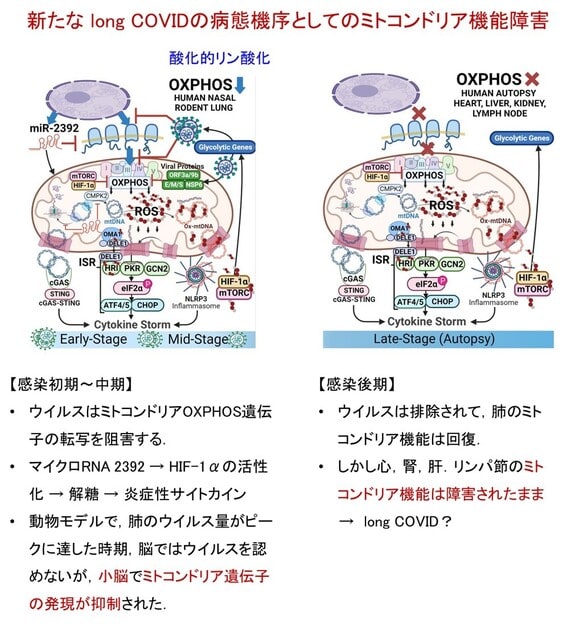
◆long COVIDの有力な病態機序としてミトコンドリア障害が明らかにされた.
米国より,SARS-CoV-2ウイルスタンパク質が宿主のミトコンドリアタンパク質と結合し,酸化的リン酸化(OXPHOS)を阻害することが示された.2つの動物モデル(ハムスターとマウス)と,患者700人の鼻咽頭サンプルと35人の剖検検体を用いて検討した.感染後,ミトコンドリアの遺伝子発現は抑制され,OXPHOS複合体全体が阻害されてエネルギー産生機能不全を誘発され,異なるエネルギー産生の代替経路(解糖系)が強制的に作られた(図4左).かつシグナルの下流で免疫反応を活性化された.この変化は全身の多くの臓器,特に心,肝,腎,リンパ節で起きていた.またウイルスが除去された慢性期でも,持続的なOXPHOS阻害が生じていた(図4右).これらはlong COVIDの多臓器症状に関与している可能性がある.著者らは治療の可能性としてmTOR阻害薬ラパマイシンに言及している.またLong COVIDの予防に有効であることが示されているメトホルミンは同じ経路で作用する.またミトコンドリア機能を制御するマイクロRNA2392も治療標的となる可能性がある.
Sci Transl Med. 2023 Aug 9;15(708):eabq1533.(doi.org/10.1126/scitranslmed.abq1533)
◆Long COVIDの発症の有無に,急性期のSARS-CoV-2抗体価やT細胞免疫の差は無関係である.
Long COVIDの機序として,初期免疫反応が過剰あるいは不十分であった可能性が指摘されている.英国からの第1波感染時に軽症または無症状のCOVID-19に罹患した医療従事者86人を対象とし,long COVIDと非long COVIDの2群に分け,ウイルスに対する液性免疫と細胞性免疫を解析した.この結果,感染後18週までの期間において,スパイクRBDや核蛋白に対する抗体反応,ウイルス中和反応,T細胞反応に差は認めなかった.また抗体低下のプロファイルにも差はなかった.またワクチン2回接種後の1年後の解析でも,2群間にSARS-CoV-2免疫に差は認めなかった.以上より,軽症または無症状の急性感染後のSARS-CoV-2ウイルスに対する免疫パラメーターにおける量的な差はLong COVIDの発症に寄与していないと考えられる.
Nat Commun. 2023 Aug 23;14(1):5139.(doi: 10.1038/s41467-023-40460-1)
COVID-19に伴う2型糖尿病の発症リスク増加とワクチンによる抑制が報告されていますが,自己免疫性疾患のリスクも増加し,多発性硬化症ではハザード比2.66,抗リン脂質抗体症候群2.12,免疫介在性血小板減少症2.10などと報告されました.これらもワクチン接種により抑制できます.またオミクロン株によるlong COVIDの罹患率もワクチンの接種回数が少ないと上昇することも報告されました.ワクチンは一部のひとには重篤な副反応を起こしてしまいますが,集団で見るとこれらのような明らかな効果があります.現在,第9波が猛威を振るっています.最新の正しい情報を理解して,ワクチンを接種するかどうかを判断する必要があります.
またフォーローしてきたCOVID-19後の認知障害もいよいよスコーピングレビューが発表され,「記憶障害と注意・遂行障害を,疲労,不安,うつとともに認める」という臨床像が明確になってきました.フィブリノゲンとD-ダイマーが入院患者の認知症発症リスクを予測できることも判明しましたので,臨床現場で評価し,その後の対応に役立てることができそうです.
◆COVID-19は自己免疫性疾患の発症リスクを上昇させ,ワクチン接種はリスクを軽減する.
香港からCOVID-19と自己免疫疾患の関連,およびCOVID-19ワクチン接種の予防効果を検討した後方視的コホート研究が報告された.対象はCOVID-19患者102万8721人と非COVID患者316万8467人であった.調整ハザード比は,多発性硬化症2.66,類天疱瘡2.39,抗リン脂質抗体症候群2.12,免疫介在性血小板減少症2.10,悪性貧血1.72,血管炎1.46,乾癬1.42,脊椎関節炎1.32,バセドウ病1.30であった(いずれも有意差あり)(図1).またワクチンの2回接種は,類天疱瘡,抗リン脂質抗体症候群,免疫介在性血小板減少症,バセドウ病,自己免疫性関節炎のリスクを減少させた.以上より,COVID-19は様々な自己免疫性疾患の発症リスクの上昇と関連し,そのリスクはワクチン接種によって軽減される可能性が示唆された.
eClinMed. August 16, 2023(doi.org/10.1016/j.eclinm.2023.102154)

◆COVID-19後の認知症候群は,記憶障害と注意・遂行障害を,疲労,不安,うつとともに認める.
イタリアからCOVID-19患者に伴う認知機能障害に関するスコーピングレビューが報告された.180件の研究が対象となったが,うち3分の1のみが認知機能障害の定義を行っていた.最も多く報告された認知機能障害は,前向性記憶障害>注意・遂行障害>ブレインフォグで(図2),精神症状ではうつ,不安,睡眠障害であった.ほとんどの研究で全身症状として疲労を認めていた.36の研究では認知機能検査が行われていたが,認知機能障害は被験者の39%に認められ,最も頻度の高い領域は注意・遂行機能(90%)と記憶(67%)であった.またCOVID-19罹患後の認知症候群の病名に関する合意は得られていなかった.症状発現の時期やその持続期間についてはまだ議論が続いている.症状に関する客観的評価方法もまだ標準化されていない.
Eur J Neurol. 2023 Aug 4.(doi.org/10.1111/ene.16027)

◆入院患者の認知機能障害を予測する血液バイオマーカーが2つ同定された.
英国から,2020年1月から2021年11月までにCOVID-19により入院した1837人を調べ,認知機能障害発症に関与する血液バイオマーカーを検討した研究が報告された.認知機能に対する医師による客観的評価と患者による主観的評価は,6カ月後と12カ月後に行われた.この結果,2種類の血液バイオマーカーが特定された.1つ目は,CRPに対するフィブリノゲンの上昇で,客観的認知障害と主観的認知障害の両方と相関した.2つ目は,CRPに対するDダイマーの上昇で,主観的な認知障害だけでなく,疲労や息切れとも関連があった.これらの知見は,米国で1万7911人の電子カルテを用いて行われた別のコホートでも確認された(図3).メカニズムとして,前者は炎症物質としての直接作用(フィブリノゲンは急性相タンパク質のひとつ)や過凝固状態が,後者は脳や肺血管の微小血栓が関与している可能性が推測される.
Nat Med (2023). https://doi.org/10.1038/s41591-023-02525-y

◆オミクロン株によるlong COVIDの発症率は18.2%である.
オーストラリアから,ワクチン接種を行っている集団におけるlong COVIDの特徴を明らかにした研究が報告された.2022年7月~8月にオーストラリアで実施されたオミクロン株感染者1万1697人(94.0%が3回以上ワクチン接種)の90日後の追跡調査を行った.Long COVIDの基準を満たしたのは18.2%で,中央値で6つの症状を報告し,疲労(70.6%),ブレインフォグ(59.6%),記憶障害・混乱(32.5%)が多かった.17.9%が就労/就学困難であった.Long COVIDの予測因子は,女性,50~69歳,既往症,ワクチン接種回数が少ないことであった.
medRxiv. August 09, 2023.(doi.org/10.1101/2023.08.06.23293706)
◆long COVIDの有力な病態機序としてミトコンドリア障害が明らかにされた.
米国より,SARS-CoV-2ウイルスタンパク質が宿主のミトコンドリアタンパク質と結合し,酸化的リン酸化(OXPHOS)を阻害することが示された.2つの動物モデル(ハムスターとマウス)と,患者700人の鼻咽頭サンプルと35人の剖検検体を用いて検討した.感染後,ミトコンドリアの遺伝子発現は抑制され,OXPHOS複合体全体が阻害されてエネルギー産生機能不全を誘発され,異なるエネルギー産生の代替経路(解糖系)が強制的に作られた(図4左).かつシグナルの下流で免疫反応を活性化された.この変化は全身の多くの臓器,特に心,肝,腎,リンパ節で起きていた.またウイルスが除去された慢性期でも,持続的なOXPHOS阻害が生じていた(図4右).これらはlong COVIDの多臓器症状に関与している可能性がある.著者らは治療の可能性としてmTOR阻害薬ラパマイシンに言及している.またLong COVIDの予防に有効であることが示されているメトホルミンは同じ経路で作用する.またミトコンドリア機能を制御するマイクロRNA2392も治療標的となる可能性がある.
Sci Transl Med. 2023 Aug 9;15(708):eabq1533.(doi.org/10.1126/scitranslmed.abq1533)

◆Long COVIDの発症の有無に,急性期のSARS-CoV-2抗体価やT細胞免疫の差は無関係である.
Long COVIDの機序として,初期免疫反応が過剰あるいは不十分であった可能性が指摘されている.英国からの第1波感染時に軽症または無症状のCOVID-19に罹患した医療従事者86人を対象とし,long COVIDと非long COVIDの2群に分け,ウイルスに対する液性免疫と細胞性免疫を解析した.この結果,感染後18週までの期間において,スパイクRBDや核蛋白に対する抗体反応,ウイルス中和反応,T細胞反応に差は認めなかった.また抗体低下のプロファイルにも差はなかった.またワクチン2回接種後の1年後の解析でも,2群間にSARS-CoV-2免疫に差は認めなかった.以上より,軽症または無症状の急性感染後のSARS-CoV-2ウイルスに対する免疫パラメーターにおける量的な差はLong COVIDの発症に寄与していないと考えられる.
Nat Commun. 2023 Aug 23;14(1):5139.(doi: 10.1038/s41467-023-40460-1)

























