
彦根藩二代当主である井伊直孝公をお寺の門前で手招き雷雨から救ったと
伝えられる招と、井伊軍団のシンボルとも言える赤備え(戦国時代の井伊
軍団編成の一種、あらゆる武具を朱りにした部隊編成のこと)と兜(かぶ
と)を合体させて生まれたキャラクタ-
【季語と短歌:11月19日】
神無月比良に冠雪冬に入る ![]()
高山 宇 (赤鬼)

⬛ 世界最高の蓄熱密度 低温蓄熱ゲル開発
拝跪されて廃棄されていた低温排熱の回収・再利用を推進し、カーボンニ
ュートラル社会の実現に貢献
11 月14日、三菱電機株式会社と国立大学法人東京科学大学は、水を主成
分とする感温性※2の高分子ゲル※3を利用して、30℃~60℃の低温の熱
を世界最高※4の蓄熱密度※5(562kJ/L)で蓄えることのできる蓄熱材を
開発した。

開発した蓄熱材は、これまで工場、自動車、オフィスや住宅環境等から大
気中に廃棄されていた低温排熱の回収・再利用に有効で、化石燃料の消費
量を削減し、省エネルギー化や脱炭素化によるカーボンニュートラル社会
の実現に貢献。
地球規模での温暖化やエネルギー危機が拡大する中、政府が2020年に発表
した「2050年カーボンニュートラル」宣言、および2021年に発表した「
2030年度の温室効果ガスの排出量46%削減(2013 年度比)」の実現に向
け、省エネルギー化の推進が求められています。中でも、新たな省エネル
ギー技術の開発と導入普及が重要課題となっており、経済産業省は「用途
に応じた開発と蓄熱密度の向上、使用材料の削減、低コスト材料の採用等
による蓄熱運用の低コスト化が必要」。排熱の有効活用を図るためには、
特に80℃以下の低温排熱を高密度(333kJ/L以上※7)に蓄えられる安価
な材料を用いた蓄熱材が求められていますが、一般的に蓄熱温度が低くな
るほど蓄熱密度が低くなるため、これまでほとんど開発されていなかった。
研究グループは今回、安価な水を主成分とし、人などの生体の細胞質にみ
られる高分子が混み合った環境(高分子混雑環境)を模倣することで、低
温でも高密度に蓄熱できる新しい感温性高分子ゲルを利用した蓄熱材を開
発した。温めると高分子が膨らんだ構造から縮んだ構造へと変化し、高分
子混雑環境を形成。高分子混雑環境下にある水分子は配列構造が乱れて高
エネルギー化し、熱を貯める容量が大きくなるため、低温の熱を高密度に
蓄えられるようになることを世界で初めて実証。これは、三菱電機が保有
する分子シミュレーション技術や蓄熱材構造の解析・評価技術とScience
Tokyo が保有する階層構造ポリマー合成技術、蓄熱材の合成技術により実
現したもの。
【要点】
・ 低温の熱でも高密度に蓄えられる蓄熱材料として、水を主成分とした新
しい感温性高分子ゲルを開発
・ 60℃以下の蓄熱温度において世界最高の蓄熱密度を実現、均質化によ
る大量合成試作に成功
【概要】
1. 低温の熱でも高密度に蓄えられる蓄熱材料として、水を主成分とした新
しい感温性高分子ゲルを開発
人などの生体の細胞質には高分子が高濃度で存在し、「高分子混雑環境」
が形成されている。高分子混雑環境下にある水分子は高分子間の狭い空間
に閉じ込められ、配列構造が乱れることがこれまでにも知られていた。水
分子は配列性が低くなるほど、エネルギーが高くなる性質を持つため、高
分子混雑環境の有無を制御することができれば、水分子のエネルギーの高
低も制御が可能になり、そのエネルギーの差分だけ蓄熱密度を高くできる
のではないかという仮説を立てた。 高分子混雑環境の有無を制御するため
に、温度によって親水性と疎水性に変化する感温性高分子を利用すること
に着目しましたが、従来の感温性高分子は高分子混雑環境を形成すること
ができなかった。そこで、三菱電機が独自に開発してきた分子シミュレー
ション技術を駆使して、感温性高分子の組成と構造を検討した結果、高分
子濃度が高い組成により、高分子混雑環境の温度制御が可能な、水を主成
分とするこれまでにない感温性の高分子ゲルの設計・開発に成功した。
開発した感温性高分子ゲルは放熱時(低温時)に親水性であるため、感温
性高分子ゲルと水は分離せずに混ざりあい、多くの水分子は感温性高分子
ゲル内に高配列で存在。
感温性高分子ゲルが温められると疎水性への構造相転移反応が起こり、高
分子鎖が縮む。高分子鎖が縮んで高分子混雑環境になると、高分子から離
れた網目構造の中心付近にいた水分子は高分子の狭い網目構造に束縛され
ないため、すり抜けて感温性高分子ゲルの外側に飛び出し、感温性高分子
ゲルと水は分離する。一方、高分子の近くにいた水分子は高分子の狭い網
目構造に束縛され閉じ込められることで水素結合反応が弱くなり、水分子
の配列構造が乱れて高エネルギー化する。このように、感温性高分子ゲル
の構造相転移反応と、水分子間の水素結合反応からなる連成反応による水
分子の高エネルギー化を利用し、高密度に蓄熱できることを世界で初めて
実証した。 また、この感温性高分子ゲルは、化学物質管理促進法の指定物
質を使わず、安全で安価な水(構成比6割~9割)と無毒で不燃性の感温性
高分子で構成されており、入手しやすく安心して使える素材。 
2. 60℃以下の蓄熱温度において世界最高の蓄熱密度を実現、均質化による
大量合成に成功
三菱電機とScience Tokyo(旧 東京工業大学)は2016年から共同研究を行
ってきた。高い階層構造ポリマー合成技術を保有するScience Tokyoにお
いて、感温性高分子ゲルの合成法を検討し、合成原料の選定と合成反応経
路の設計を実施しました。三菱電機では、感温性高分子ゲルをラボレベル
で合成、評価し、60℃以下の低い蓄熱温度で世界最高※4の蓄熱密度(562
kJ/L)を実現しました。また、Science Tokyoが開発した合成反応制御技
術により、感温性高分子ゲルの均質化を実現し、大量合成試作でもラボレ
ベルと同等の蓄熱密度を確認した。
蓄熱温度が30℃~60℃(温度差30℃)における蓄熱材ごとの蓄熱密度を
比較したところ、温水で125kJ/L、市販品である脂肪酸で225kJ/L、パラ
フィンで260kJ/Lであるのに対し、今回開発した感温性高分子ゲルは562
kJ/Lと2倍以上の圧倒的な蓄熱密度を有す。
【関連特許】
1. 特許第6704553号 蓄熱装置 三菱電機株式会社
【要約】 図1のごとく、蓄熱装置は、水、有機溶媒、及び水又は有機溶媒
の化合物からなる群から選択される溶媒と、感温性高分子とからなる感温
性高分子ゲルを有する蓄熱材が封入された容器と、容器に収容され、加熱
冷却用流体と熱交換して蓄熱材を加熱又は冷却して蓄熱材に温熱又は冷熱
を蓄えると共に、熱利用流体と熱交換して蓄熱材から吸熱して蓄熱材から
放熱させる熱交換器と、を備え、蓄熱材は、下限臨界溶液温度を境界とし
て親水性と疎水性とが可逆的に変化するものであり、親水性と疎水性との
変化の過程において感温性高分子ゲルに含まれる溶媒が液体状態を維持す
るものである。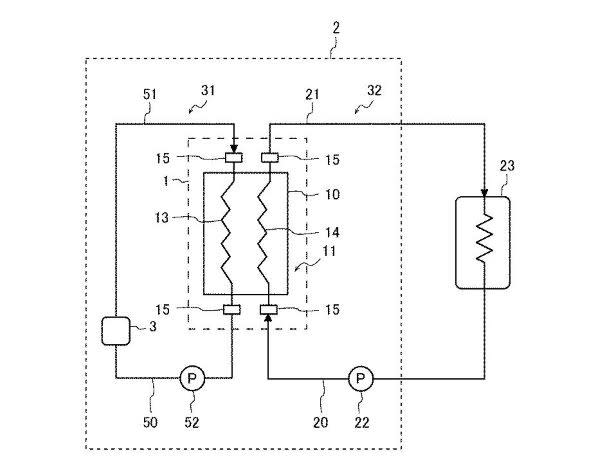
図1. 蓄熱システムを示す回路図

図2 蓄熱装置を示す断面図 図3 蓄熱装置を示す斜視図
1 蓄熱装置、2 蓄熱システム、3 熱源、10 容器、11 熱交換器、
12 フィン、13 加熱冷却配管、14 熱利用配管、15 継手、20
戻り配管、21 往き配管、22 循環ポンプ、23 放熱端末、31 熱源
回路、32 利用回路、50 入口配管、51 出口配管、52 加熱冷却ポ
ンプ、60 蓄熱材、61 感温性高分子、62 水。
【発明の効果】
本発明によれば、蓄熱材は、下限臨界溶液温度を境界として親水性と疎水
性とが可逆的に変化するものであり、親水性と疎水性との変化の過程にお
いて感温性高分子ゲルに含まれる溶媒が液体状態を維持する。このため、
大型化が抑制される。また、蓄熱装置は、蓄熱材に冷熱を蓄えることがで
きる。このように、蓄熱装置は、冷却機器に適用され且つ大型化が抑制さ
れる。
【特許請求の範囲】【請求項1】
水、有機溶媒、及び水又は有機溶媒の化合物からなる群から選択される
溶媒と、感温性高分子とからなる感温性高分子ゲルを有する蓄熱材が封入
された容器と、前記容器に収容され、加熱冷却用流体と熱交換して前記蓄
熱材を加熱又は冷却して前記蓄熱材に温熱又は冷熱を蓄えると共に、熱利
用流体と熱交換して前記蓄熱材から吸熱して前記蓄熱材から放熱させる熱
交換器と、を備え、前記蓄熱材は、下限臨界溶液温度を境界として親水性
と疎水性とが可逆的に変化するものであり、親水性と疎水性との変化の過
程において前記感温性高分子ゲルに含まれる前記溶媒が液体状態を維持す
るものであり、 前記感温性高分子は、架橋構造を有すると共に、ヒドロ
キシ基、スルホン酸基、オキシスルホン酸基、リン酸基及びオキシリン酸
基からなる群から選択される一種以上の官能基を分子末端に有し、 前記感
温性高分子を構成する繰り返し単位と、前記官能基と、前記架橋構造の単
位とのモル比が、99:0.5:0.5~70:20:10である 蓄熱装
置。
【請求項2】 前記熱交換器は、 前記加熱冷却用流体が流れる加熱冷却配
管と、前記熱利用流体が流れる熱利用配管と、を有する請求項1記載の蓄
熱装置。
【請求項3】 前記感温性高分子ゲルは、 下記一般式(1)【化1】


(式中、R1は、水素原子又はメチル基を表し、R2は、N-3-イソプロ
ポキシプロピル基又はN-1-メトキシメチルプロピル基を表し、Xは、
共有結合手を表すか又はヒドロキシ基、スルホン酸基、オキシスルホン酸
基、リン酸基及びオキシリン酸基からなる群から選択される一種以上の官
能基を表し、*は、共有結合手を表す)又は 上記一般式(2![]() )【化2】(
)【化2】(
式中、R1は、水素原子又はメチル基を表し、R2は、N-3-イソプロ
ポキシプロピル基又はN-1-メトキシメチルプロピル基を表し、Xは、
共有結合手を表すか又はヒドロキシ基、スルホン酸基、オキシスルホン酸
基、リン酸基及びオキシリン酸基からなる群から選択される一種以上の官
能基を表し、*は、共有結合手を表す)で表される構成単位と、
![]()
(式中、*は、共有結合手を表し、qは、1~3の整数を表す)で表され
る構成単位と、を含み、前記一般式(1)又は前記一般式(2)で表され
る構成単位の共有結合手と前記一般式(3)で表される構成単位の共有結
合手とが結合した架橋構造を有し、前記一般式(1)又は前記一般式(2)
で表される構成単位と、前記官能基であるXと、前記一般式(3)で表さ
れる構成単位とのモル比が、99:0.5:0.5~70:23:7であ
る 請求項1又は2記載の蓄熱装置。
※ 事業化に当たって、コンパクトがダウンサイジング化できるか想定し
応用展開できるかのビジョン化と用途戦略の是非が大切なり、環境エネ
ルギーへのインパクトを見積(経済的貢献)喧伝する段階にある発明で
ある考えられる。大変面白い実用課題である。
【海水有価物回収水素製造並びに炭素化合物製造事業論 ⑤】
2. 特開2024-77350 炭素および水素の製造方法 三菱マテリアル株式
会社他 ②
【発明を実施するための形態】【0023】
まず最初に、本実施形態の炭素および水素の製造方法で用いる還元剤につ
いて説明する。
還元剤は、後述する二酸化炭素分解工程S1において、二酸化炭素と反応
させることによって、二酸化炭素を還元して炭素と酸素に分解する材料で
ある。本実施形態で用いる還元剤は、Fe3O4-δ(但し、δは1以上4未
満)で表されるマグネタイト(四酸化三鉄)の酸素欠陥鉄酸化物、ヘマタ
イトや使用済みカイロ(主成分は水酸化鉄)の酸素欠陥鉄酸化物、または
酸素完全欠陥鉄を用いる。

図1は、マグネタイトの1/4単位格子の結晶構造を示す模式図である。
マグネタイトは、結晶学的に、スピネル型結晶格子構造を有し、酸素イオ
ン(O2-)が立方最密充填配置にされ、その隙間(Asite、Bsit
e)に、+3価の鉄(Fe+3)、+2価の鉄(Fe2+)が2:1の割合
で配置されている。マグネタイトは、一般式としてFe3O4で表される。
【0025】本実施形態で用いる還元剤は、このようなマグネタイトの結
晶構造、即ちスピネル型結晶格子構造を保った状態で、図1に示す任意の位
置の酸素イオンを離脱させることで得られる酸素欠陥鉄酸化物(1≦δ<
4未満)、またはマグネタイトを完全に還元することで得られるスピネル
型結晶格子構造を保った酸素完全欠陥鉄(δ=4)、またはヘマタイトや使
用済みカイロを還元することで得られるスピネル型結晶格子構造を保った
酸素欠陥鉄酸化物、またはヘマタイトや使用済みカイロを完全に還元する
ことで得られるスピネル型結晶格子構造を保った酸素完全欠陥鉄である。
こうした還元剤は、後述する還元剤再生工程S4において生成される。
【0026】マグネタイトを還元することで得られるスピネル型結晶格子
構造を保った酸素欠陥鉄酸化物は、Fe3O4-δで表され、マグネタイト
から離脱させた酸素イオン(O2-)の離脱割合によって、δが1以上4未
満の範囲にされる。また、マグネタイトから酸素イオンを全て離脱させた
(即ち、δ=4)ものが、上述した酸素完全欠陥鉄となる。
【0027】 δは酸素欠陥度とされ、マグネタイトの結晶構造、即ちスピ
ネル型結晶格子構造を保った状態の酸素欠陥鉄酸化物のマグネタイトに対
する酸素の欠陥割合である。こうした酸素欠陥度δは、還元剤再生工程S4
においてマグネタイトが水素と反応する前の質量と、反応後の質量との差
分を計測し、質量の減少量(差分)がマグネタイトから離脱した酸素量(
この離脱した酸素の格子中の配置位置が原子空孔、即ち欠陥となる)と等
しいことから、この質量の減少量から酸素欠陥度δ(δ=1~4)を算出す
ることができる。
【0028】そして、マグネタイトから酸素イオンが離脱した部位は、ス
ピネル型結晶格子構造を保った状態で原子空孔となり、離脱分だけカチオ
ンが結晶格子内に多く閉じ込められ、格子間隔が拡がった状態になる。こ
のような酸素離脱による原子空孔が、還元剤として二酸化炭素の脱酸素反
応(還元反応)を生じさせる。
【0029】本実施形態の還元剤(酸素欠陥鉄酸化物、酸素完全欠陥鉄)
は、平均粒子径が、例えば1μmよりも大きければよく、1μm以上20μm
未満であることが好ましく、また、50μmを超え200μm未満であるこ
とも好ましい。
【0030】還元剤の平均粒子径が1μmよりも小さいものにした場合は、
実験結果によれば、二酸化炭素を分解する際に一酸化炭素の生成割合が高
くなり、炭素の回収率が低くなる可能性がある。平均粒子径が1μm以上の
還元剤を用いることで、高い炭素回収率が維持できると同時に、還元剤粒
子の凝集性が低くなるため、反応器の壁面への固着現象などのトラブルが
回避でき、ロータリーキルンなどの工業用反応装置への適用が可能となる。
【0031】更に、還元剤の平均粒子径を20μm未満にすることで、高い
反応速度を維持することができる。また、還元剤の平均粒子径を50μmを
超え200μm以下にする場合、粒子の飛散性が下がり、流動化性能が良く
なるため、流動層などの工業用の反応装置への適用が可能となる。この場
合、ロータリーキルン式の反応装置と比べて、固-気接触性や伝熱性が良
く、設備費が低く、反応装置のサイズをコンパクトにすることができる。
図2は、本発明の一実施形態に係る炭素および水素の製造方法を段階的に
示したフローチャートである。本実施形態の炭素および水素の製造方法は、
表面に炭素を付着させたマグネタイトを生成する二酸化炭素分解工程S1
と、炭素と、塩化鉄とを生成する炭素分離工程S2と、マグネタイトと、
水素と、塩化水素ガスとを生成する水素製造工程S3と、還元剤を生成す
る還元剤再生工程S4と、を有する。こうした各工程で、マグネタイトや
これを還元させた還元剤を循環利用して、外部から供給される二酸化炭素
及び水から、炭素および水素を製造する。
【0033】<二酸化炭素分解工程S1>
二酸化炭素分解工程S1は、ロータリーキルンや気泡流動層などの反応装
置(二酸化炭素分解炉)を用いて、例えば、平均粒子径が1μm~500μ
m程度の粉末状の還元剤を攪拌しつつガス状の二酸化炭素に接触させるこ
とによって、二酸化炭素を分解(還元)する。そして、表面に炭素を付着
させたマグネタイトを生成する。
【0034】二酸化炭素分解工程S1に用いる反応装置としては、循環流
動層を用いることもできるが、気泡流動層と比較して、反応器全体の高さ
が高い、設備費が高い、粒子再循環ループの設計と操作が複雑、粒子の滞
留時間が短い(反応装置内での滞留時間は秒のオーダー)、使用できる還
元剤の粒子径が限られる、粒子の摩耗を促進される、高いガス流速の維持
や粉体の循環に必要なエネルギーコストが大きい、などのデメリットがあ
る。
【0035】この二酸化炭素分解工程S1に用いる二酸化炭素の供給源と
しては、例えば、二酸化炭素を多量に排出する施設、例えば製鉄所、火力
発電所、セメント工場、ゴミ焼却施設、バイオガス生成施設、天然ガス井
戸などから排出される二酸化炭素を用いればよい。また、還元剤は、後述
する還元剤再生工程S4から供給される。
【0036】二酸化炭素分解工程S1における反応温度は、300℃以上、
450℃以下、好ましくは350℃以上、400℃以下の範囲であればよ
い。このように、反応温度を300℃以上、450℃以下といった温度範
囲にすることで、還元剤がスピネル型結晶格子構造を維持することができ
る。反応温度が例えば500℃以上といった高温であると、マグネタイト
の繰り返し利用により、還元剤がスピネル型結晶格子構造を維持できなく
なる懸念がある。かつ反応する時の消費エネルギーが増える懸念がある。
【0037】二酸化炭素分解工程S1では、こうした反応温度範囲に昇温
させるために、二酸化炭素供給源である製鉄所、火力発電所、セメント工
場、ゴミ焼却施設などの稼働に伴って発生した熱(排熱)、再生可能エネ
ルギー、及び高温の熱を取り出せる原子炉である高温ガス炉の熱エネルギ
ーを熱源として有効利用することも好ましい。
【0038】二酸化炭素分解工程S1における反応圧力は、0.01MPa
以上、5MPa以下、好ましくは0.1MPa以上、1MPa以下の範囲
であればよい。反応圧力が0.01MPa以上であれば、実用プロセスと
して必要な反応速度を得ることができ、更に、0.1MPa以上であれば、
二酸化炭素濃度が低い実際の排気ガスへの直接対応も可能となる。また、
反応圧力が5MPa以下であれば、装置の製作コストを抑えることができ
る。
【0039】二酸化炭素分解工程S1では、反応温度、反応圧力を高める
ことによって、二酸化炭素の分解速度が高まり、二酸化炭素の処理効率を
高めることができる。一方、反応温度が高すぎると、還元剤のスピネル構
造が破壊されるおそれがある。
【0040】二酸化炭素分解工程S1での二酸化炭素の分解には、以下の
式(1)、(2)の2段階と式(3)の1段階の反応が生じる。
CO2+2e-→CO(中間生成物)+O2-・・・(1)
CO+2e-→C+O2-・・・(2)
CO2+2e-→C+2O2-・・・(3)
そして、上述した式(1)、(2)、(3)で生じた酸素は、以下の式
(4)、(5)で酸素欠陥鉄酸化物(式(4))や酸素完全欠陥鉄(式(
5))の原子空孔に挿入される。
Fe3O4-δ+δO2-→Fe3O4+2δe-(但し、δ=1以上4未満)
・・・(4)
3Fe+4O2-→Fe3O4+8e-・・・(5)
【0041】上記の式(1)によって得られた一酸化炭素(CO)は、水
素添加によって、メタン、メタノールなどの炭化水素や各種樹脂などの有
用な化成品を得るための原料として用いることができる。
【0042】二酸化炭素分解工程S1での上述した反応で、すべての二酸
化炭素を式(2)まで、または式(3)で反応させた場合には、最終的な
生成物としてガスの発生を伴わない。即ち、二酸化炭素中の酸素は、酸素
欠陥鉄酸化物、または酸素完全欠陥鉄に全て取り込まれると考えられる。
これを考慮して二酸化炭素と酸素欠陥鉄酸化物の反応は、式(6)、二酸
化炭素と酸素完全欠陥鉄の反応は、式(7)で表される。
2Fe3O4-δ+δCO2→2Fe3O4・δC(炭素付着マグネタイト。
但し、δ=1以上4未満)・・(6)
3Fe+2CO2→Fe3O4・2C(炭素付着マグネタイト)・・・(7)
【0043】二酸化炭素分解工程S1で還元剤として用いる酸素欠陥鉄酸
化物や酸素完全欠陥鉄が、二酸化炭素を炭素まで分解できるのは、これら
の還元剤が非平衡状態で形成される準安定な結晶構造であるスピネル型結
晶格子構造を有しており、室温においても酸素と徐々に反応し、酸素イオ
ンを取り組み、より安定なFe3O4に変化しようとするためである。即ち、
格子中に原子空孔を有する不安定なスピネル型結晶格子構造がより安定な
原子空孔のないスピネル型結晶格子構造に変化しようとすることから生じ
るものと考えられる。
【0044】こうした酸素欠陥鉄酸化物や酸素完全欠陥鉄の安定化(マグ
ネタイト化)の過程で、酸素イオンが結晶中に取り込まれると結晶は電気
的に中性を維持しようとするために、電子を結晶表面から放出しようとす
る。酸素欠陥鉄酸化物や酸素完全欠陥鉄では+2価のFe(Fe2+)が
電子を放出し得る原子として存在するが、酸素欠陥鉄酸化物や酸素完全欠
陥鉄の結晶の不安定性のために、通常と異なる還元ポテンシャルを生じて
いるものと考えられる。
【0045】二酸化炭素分解工程S1では、還元剤として用いる酸素欠陥
鉄酸化物や酸素完全欠陥鉄による二酸化炭素の分解能力を最大限にするた
め、反応環境における酸素濃度を5体積%以下に保つようにすることが好
ましい。
【0046】二酸化炭素分解工程S1における反応環境で酸素濃度が5体
積%よりも高いと、二酸化炭素を構成する酸素が還元剤(酸素欠陥鉄酸化
物、または酸素完全欠陥鉄)に取り込まれる前に、この還元剤の酸素欠陥
部位に、反応雰囲気中の酸素が取り込まれて、還元剤の二酸化炭素分解能
力が低下する懸念がある。
【0047】二酸化炭素分解工程S1で二酸化炭素の分解によって生じた
炭素は、粒子径が1μm以下のナノサイズの炭素として生成される。二酸
化炭素分解工程S1において、同一温度条件では、上述した式(1)の反
応速度は、式(2)の反応速度よりも遅いが、式(1)の反応速度を高め
ることによって式(2)の反応が迅速に進行するようになり、微細なナノ
サイズの炭素粒子を生成できる。式(1)と式(2)の反応速度は、酸素
欠陥度δを大きくすることと、反応温度、反応圧力を高くすることにより、
高めることができる。
【0048】こうしたナノサイズの炭素は、酸素欠陥鉄酸化物や酸素完全
欠陥鉄が酸化されて生じたマグネタイトの表面に付着する、あるいは表面
を覆うように生成される。こうした表面に炭素を付着させたマグネタイト
は、次の炭素分離工程S2に送られる。
【0049】一方、本実施形態では、二酸化炭素分解工程S1で二酸化炭
素の分解によって、還元剤はマグネタイト(Fe3O4)になる。本実施形
態では、炭素は、マグネタイトの表面に比較的強固に付着した状態で生じる。
【0050】<炭素分離工程S2>
炭素分離工程S2は、マグネタイトの塩化反応(マグネタイトから塩化鉄
(III)(FeCl3)と塩化鉄(II)(FeCl2)への転換)と炭素回収操作よ
り構成される。マグネタイトの塩化反応は、塩酸溶解による湿式塩化法と
塩化水素ガスによる乾式塩化法がある。
【0051】(湿式塩化)
マグネタイトの塩化反応を湿式塩化で行う場合、二酸化炭素分解工程S1
で得られた表面に炭素を付着させたマグネタイトと、塩酸(塩化水素の水
溶液)とを反応させることにより、マグネタイトを塩酸に溶解させ、塩酸
に不溶な炭素をマグネタイトから分離する。塩酸に溶解したマグネタイト
は、塩化水素との反応によって塩化鉄(塩化鉄(III)と塩化鉄(II))と水とを
生成する。
【0052】 塩酸に溶解させたマグネタイトと炭素の分離は、例えば、濾
過などの固液分離によって行えばよい。また、生成した塩化鉄(塩化鉄(III)
と塩化鉄(II)の混合物)は、次の水素製造工程S3に送られる。こうした湿
式塩化の場合、生成する酸化鉄が全て溶解されて炭素を分離することがで
きる。
【0053】 炭素分離工程S2(湿式塩化)で用いる塩酸は、塩化水素濃
度が例えば5質量%~37質量%の範囲のものを用いればよい。塩酸の塩
化水素濃度が5質量%未満では反応が遅くなる懸念がある。また、37質
量%を超える濃塩酸は塩化水素の揮発が速く取り扱いが難しい。炭素分離
工程S2(湿式塩化)における反応温度は、10℃以上、150℃以下、
好ましくは50℃以上、100℃以下の範囲であればよい。10℃未満で
は反応速度が遅く、また冷却設備が必要となる。150℃を超えると消費
エネルギーが多く、かつ溶液の蒸発が起きてしまって効率が悪い。炭素分
離工程S2(湿式塩化)では、こうした反応温度範囲に昇温させるために、
例えば、二酸化炭素分解工程S1と同様の熱源を有効利用することも好ま
しい。
【0054】炭素分離工程S2(湿式塩化)でのマグネタイトの塩化反応
は、以下の式(8)~(9)で表される。
2Fe3O4・δC+16HCl→4FeCl3+2FeCl2+8H2O+
δC(湿式塩化:10~150℃)(但し、δ=1~4)・・・(8)
2Fe3O4+16HCl→4FeCl3+2FeCl2+8H2O(湿
式塩化:10℃~150℃)・・・(9)
【0055】(乾式塩化)
マグネタイトの塩化反応を乾式塩化で行う場合、二酸化炭素分解工程S1
で得られた表面に炭素を付着させたマグネタイト、または水素製造工程S3
で得られたマグネタイトと、塩化水素ガスとを反応させることによって塩
化鉄(塩化鉄(III)と塩化鉄(II))と水とを生成する。
【0056】
炭素分離工程S2(乾式塩化)で用いる塩化水素ガスは、塩化水素濃度
が例えば50質量%~100質量%の範囲のものを用いればよい。塩化水
素の濃度が50質量%未満では反応が遅くなる懸念がある。炭素分離工程
S2(乾式塩化)における反応温度は、50℃以上、300℃以下、好ま
しくは80℃以上、200℃以下の範囲であればよい。50℃未満では反
応速度が遅く、また300℃を超えると消費エネルギーが多く効率が悪く
なると同時に、塩化反応が発熱反応であるため高温では反応の進行に不利
となる。炭素分離工程S2(乾式塩化)では、こうした反応温度範囲に昇
温させるために、例えば、二酸化炭素分解工程S1と同様の熱源を有効利
用することも好ましい。
【0057】炭素分離工程S2(乾式塩化)でのマグネタイトの塩化反応
は、以下の式(8)~(9)で表される。
2Fe3O4・δC+16HCl→4FeCl3+2FeCl2+8H2O
+δC(乾式塩化:50~300℃)(但し、δ=1~4)・・・(8)
2Fe3O4+16HCl→4FeCl3+2FeCl2+8H2O(乾
式塩化:50℃~300℃)・・・(9)
【0058】 消費エネルギーを低減するため、炭素が付着されていない
マグネタイト(水素製造工程S3で得られた単なる水素製造のために循環
されているマグネタイト)は、こうした塩化水素ガスによる乾式塩化を用
いることが好ましい。乾式塩化の場合、炭素付着マグネタイトを塩化水素
ガスによって塩化鉄に転換した後、生成物を水に溶解させることによって、
不溶成分として炭素を分離することができる。
【0059】炭素分離工程S2でマグネタイトから分離された炭素(炭素
材料)は、粒子径が1μm以下のナノサイズの炭素であり、粒子径が1μm
を超えるものは殆ど生成しない。こうしたナノサイズの炭素粉末は、純度
が例えば99%以上の高純度の炭素であり、カーボンブラック、活性炭と
して、ゴム補強用添加剤、電池材料、トナー、着色剤、導電材料、触媒、
吸着剤などの機能性の炭素材料に、または還元剤として、製鉄用コークス
代替などに直接用いることができる。また、人造黒鉛、カーボンファイバ
ー、カーボンナノチューブ等の炭素材料の製造原料として用いることがで
きる。
【0060】
<水素製造工程S3>
水素製造工程S3は、電解装置を用いて、炭素分離工程S2で得られた
塩化鉄(III)の還元反応(塩化鉄(III)から塩化鉄(II)への還元)を行う電解還
元過程S3-1と、この電解還元過程S3-1で得られた2価の塩化鉄と
水とを反応させて、マグネタイトと、水素と、塩化水素ガスとを生成する
加水分解過程S3-2と、を有している。この水素製造工程S3で生じた
マグネタイトは、次の還元剤再生工程S4に送られる。また、塩化水素は
、炭素分離工程S2で用いる塩酸の製造原料として用いることができる。
なお、塩化鉄(II)溶液の濃縮、乾燥、造粒等の操作は膜分離装置、蒸発装
置、晶析装置、スプレードライヤー等の装置を用いて、所定の粒子径を持
った塩化鉄(II)粒子にした後、水素、マグネタイト製造反応に送ることも
ある。
【0061】(電解還元過程S3-1)
図3は、水素製造工程S3を構成する電解還元過程S3-1で用いる電
解装置の一例を示す模式図である。本実施形態の電解装置10は、陰極槽
11と、陽極槽12と、陰極槽11および陽極槽12の間に形成される隔
壁13と、を有している。また、陰極槽11には、陰極電極(作用極)
21、および参照電極22が設けられ、また陽極槽12には、陽極電極
(対極)23が設けられている。更に、陰極電極21と陽極電極23との
間に電圧を印加する電源装置14が設けられている。

図3 水素製造工程S3を構成する電解還元過程S3-1で用いる電解装
置の一例を示す模式図
この項つづく

人間の未来 AIの未来 講談社(2018/02発売)
サイズ B6判/ページ数 226p/高さ 19cm
商品コード 9784062209724NDC分類 304C
コード C0095
出版社内容情報
世界と日本の未来を、二人の最高の知性が語り合う。「ひらめき」の正体、
で通用する人材をつくるには、人間は不老不死になれるか10年後、100年
後の世界と日本の未来を、ノーベル賞学者と国民栄誉賞棋士、最高の知性
を持つ二人がとことん語り合う!iPS細胞、将棋界とAIといった二人の
専門分野に加えて、「ひらめき」「勘」の正体、世界で通用する人材をつ
くるにはどうするか、人間は不老不死になれるかといった、人類の普遍的
なテーマについても熱く討論する
まえがきにかえて 羽生善治から山中伸弥さんへ
第1章 iPS細胞の最前線で何が起こっていますか?
第2章 なぜ棋士は人工知能に負けたのでしょうか?
第3章 人間は将来、AIに支配されるでしょうか?
第4章 先端医療がすべての病気に勝つ日は来ますか?
第5章 人間にできるけどAIにできないことは何ですか?
第6章 新しいアイデアはどこから生まれるのでしょうか?
第7章 どうすれば日本は人材大国になれるでしょうか?
第8章 十年後、百年後、この世界はどうなっていると思いますか?
あとがきにかえて 山中伸弥から羽生善治さんへ
ーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーー
人間の未来AIの未来 ⓵
遺伝子を「シュレッダーで破壊」!?
人間の「価値」が揺らぐこの時代の未来を見通すべく、“ノーベル賞科学
者”山中伸弥と“史上最強棋士”羽生善治が語り合う『人間の未来AIの未来』
(現代ビジネスオンライン版 2024.11.14)
◾意味づけするのは人間の仕事
AIって抜群に優秀な部下の一人なんですよ。膨大な知識を持っていて、い
つも冷静沈着。感情を交えずに「山中先生、これを選択した場合、このよ
うになる可能性が13パーセント高くなります」(笑)。とても貴重な情報
ではあるけれど、あくまでセカンドオピニオンというか、彼は部下の一人
であって意思決定者ではないと話す山中氏。それは医療の世界では決定的
に重要なこと。治療方針を最終的にどうするかは、患者さんと医師が決定
する。たとえば、末期がんの患者さんに対して、AI君は「このがんは、い
かなる治療をしても99・99パーセント効果がありません。だから治療は
中止して、ターミナルケア(終末期医療)に移行しましょう」と論理的に
言ってくるかもしない。と話す。
この項つづく
 混声合唱曲 日本大学合唱団
混声合唱曲 日本大学合唱団
『二十億光年の孤独』
曲:木下牧子/詩:谷川俊太郎
● 今日の言葉:



























※コメント投稿者のブログIDはブログ作成者のみに通知されます