今回のキーワードは,ダウン症候群のあるかたから学ぶ教訓,入院患者の厳しい長期的予後,長期の予後不良に関わる横隔膜病変,動物実験で示された脳へのウイルスの速やかな感染,遠隔で行うALSの集学的ケア,COVID-19感染重症筋無力症患者の国際的レジストリ,小児でCOVID-19による重症化がまれな理由,モデルナ社製ワクチンmRNA-1273の副作用です.
地域によって第3波による医療崩壊が現実のものになってきました.医療崩壊はCOVID-19患者さんの診療や救命が困難になるだけでなく,他の疾患に対する通常の診療ができなくなることが大きな問題です.また医療者は自らが感染し,診療から離脱したり,院内感染を起こしたりすることを恐れています.第3波は行動様式をコロナ前に戻しても良いのだという意識変化がもたらされたことにより生じたのではないかと思います.初心に戻り,感染予防の基本を「粘り強く」遵守することが必要だと思います.
◆ダウン症候群のあるかたから学ぶべき教訓.
スペインからの報告.ダウン症候群では,免疫機能障害,呼吸器感染症,慢性炎症,早期高齢化がみられ,さらにCOVID-19 の危険因子となる併存疾患の有病率が高いという特徴がある.このためCOVID-19に対してダウン症候群患者が脆弱である恐れがある.ところがスペインのTrisomy 21 Research Societyが行った調査によると,ダウン症候群におけるCOVID-19感染は,2020年3~5月の第1波後,そして9月に第2波が生じて以降も大幅に減少している.著者らは,この感染率の低下は,ダウン症の人が有する,身だしなみや衛生面での「粘り強さ」によって説明できるのではないかと議論している.この議論が正しいとすれば,ダウン症の人々が示す行動パターンは,感染拡大を避けるために有用な教訓,もしくは注意喚起として役立つであろう.
Lancet Neurol. Dec, 2020(doi.org/10.1016/S1474-4422(20)30401-4)
◆COVID-19入院患者の退院60日まで観察ではさまざまな予後が不良である.
COVID-19患者の入院中の転帰に関する報告は多いものの,退院後の長期の転帰はよく分かっていない.米国ミシガン州の38病院から,入院患者1648名(中央値62歳)の退院後 60 日間の転帰を明らかにした研究が報告された.398名(24.2%)が入院中に死亡した.退院した残1250名のうち,975名(78.0%)が自宅に帰り,158名(12.6%)が看護師のいる療養施設・リハビリテーション施設に退院した.退院後60日までに,さらに84名の患者(6.7%,ICU入室者の10.4%)が死亡した.以上よりコホート全体の死亡率は29.2%,ICU治療を受けた405名の死亡率は63.5%と高率であった.退院後60日以内に189名(病院生存者の15.1%)が再入院した.また65名は60日後でも味覚や嗅覚の喪失を認めた.入院前に就業していた195名のうち,78名は健康上の問題,または仕事を失って復職できなかった.28名が退院後にメンタルヘルスのケアを求めた.179名の患者が少なくとも軽度の経済的影響を受け,47名が貯蓄の大部分または全部を使い果たした.→ 国によって入院の条件も異なるため,単純に日本に当てはめられないものの,長期的なさまざまな予後が不良であることを考慮すると,とにかくCOVID-19を甘く見ず感染者を拡大させないこと,ならびに生存者を支援する制度をつくることが必要である.
Ann Intern Med. Nov 11, 2020(doi.org/10.7326/M20-5661)
◆長期の予後不良に関わる横隔膜筋症.
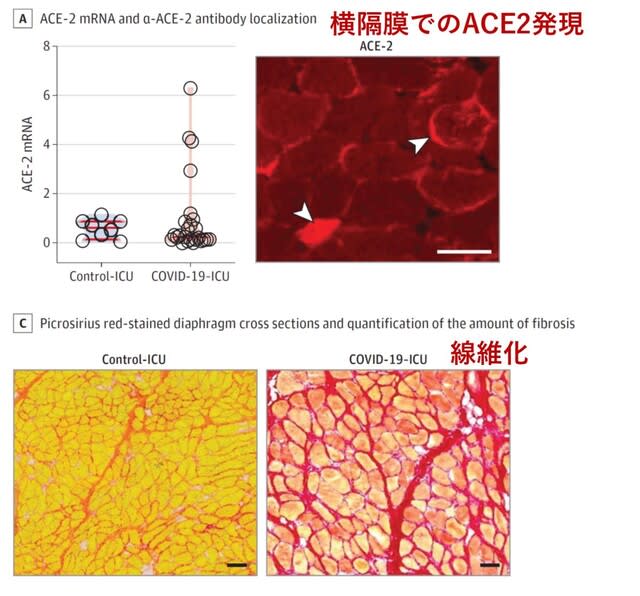
呼吸に関わる主要な筋である横隔膜に焦点を当てたオランダからの研究.COVID-19により死亡した26名(中央値71歳)の剖検時に横隔膜筋標本を採取した.対照群として,他の疾患で死亡した8名の剖検標本を使用した.COVID-19患者のうち24 例(92.3%)が侵襲的機械換気を受け,その中央値は12 日間であった.ACE2は主に筋線維膜に局在し(図1A),SARS-CoV-2ウイルスが横隔膜に感染するための入り口となると考えられた.実際に横隔膜でウイルスRNAが検出されたのは4名(15.4%)であった.ウイルスRNAは横隔膜の筋線維内に局在していた.発現遺伝子の解析では,線維化に関わるFGFシグナルが活性化していた.実際に免疫染色で,COVID-19患者では線維化が2倍以上高度であった(図1C).横隔膜筋障害がSARS-CoV-2ウイルスによる直接的な変化であるかは不明であるが,COVID-19感染に伴う高度の横隔膜筋障害がその脱力につながり,退院しても人工呼吸器離脱困難,持続的な呼吸困難,疲労につながる可能性がある.
JAMA Intern Med. Nov 16, 2020(doi.org/10.1001/jamainternmed.2020.6278)
◆動物実験で鼻粘膜への感染により,ウイルスは速やかに脳へ移行する.
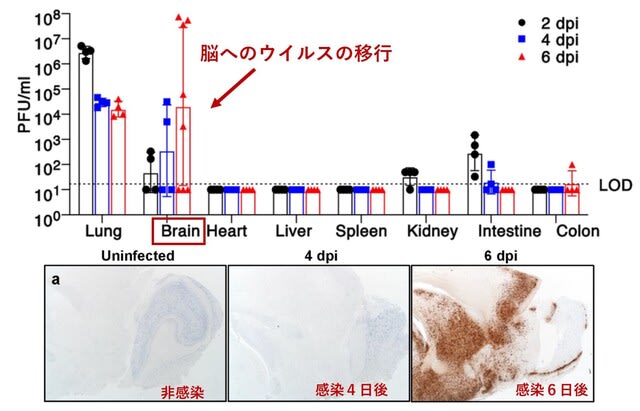
米国からの研究.上皮細胞特異性発現K18プロモーターにより,ヒトのACE2を発現するモデルマウスを作成し,感染実験を行った研究が報告された.この実験系では,SARS-CoV2ウイルスは上皮細胞にのみ感染し,嗅細胞には感染を認めないが,なんと脳では感染後2日,4日,6日と経時的に,他の臓器よりも多くウイルスが検出されるようになる(図2上).具体的には,ウイルス105 PFUを経鼻接種すると,5/8匹のマウス脳から感染性ウイルスが検出された.感染後4および6日目にウイルスヌクレオカプシド(N)タンパク質の免疫染色を行ったところ,4日後では染色されなかったが,6日後では嗅球,大脳皮質,馬尾・翼状突起,視床,視床下部,腹側線条体を含むいくつかの脳領域で染色が観察された(図2下).HE染色では,視床で細胞死と血栓が認められ,細胞死の病巣が変性上衣細胞に隣接して検出された.影響を受けた領域のほとんどが嗅球の二次的,三次的に連絡するのに対し,いくつかの領域,例えば,後眼球と舌下神経核のような領域は,直接連絡していない.この結果は,脳へのウイルス伝播における嗅球感染の役割を示唆するものの,ウイルスが他のルートで中枢神経系に入る可能性を示唆する.→ このデータを見ると,ヒトでもウイルスが脳に移行し,将来,再活性化する可能性があるのではないかと危惧される.
Nature. 2020 Nov 9.(doi.org/10.1038/s41586-020-2943-z)
◆神経難病のケア(1)ALSの集学的ケアは遠隔診療でも十分可能である.
集学的ALSケアは,生存期間を延長し,患者と介護者の生活の質を向上させる.しかしパンデミックにより,直接のケアが困難な状況になった.大流行が生じたイタリアから,第三次ALSセンターの遠隔医療の効果に関する検討が報告された.19名のALS患者を,脳神経内科医,管理栄養士(食事・体重モニタリング),心理士(心理的評価・支援),理学療法士(理学療法治療・機器の処方)から構成される集学的チームが,遠隔医療により診療を行った.結果的に,すべての患者は,リモートではあるものの医療の専門家と対面で話すことについて肯定的な認識を示し,チームが自分の問題を理解していることに満足していた.さまざまな医療行為が行われ,処方内容の変更が11/19例,非侵襲的陽圧呼吸(NPPV)管理の開始が2/19例,機器の処方が9/16例で行われた.ALSFRS-Rの月平均低下率は,遠隔医療開始前は0.88,開始後は0.49と改善した.体重と1日のカロリー摂取量も安定していた. 不安・うつスコアは改善し,QOLスコアも安定していた. → ALSの集学的ケアは遠隔診療でも十分可能であり,今後はさらに患者のニーズに応じた個別化プログラムを検討するとのこと!
Acta Neuropathol. Nov 13, 2020(doi.org/10.1111/ane.13373)
◆神経難病のケア(2)COVID-19に感染した重症筋無力症の国際的な患者登録(レジストリ)の開始.
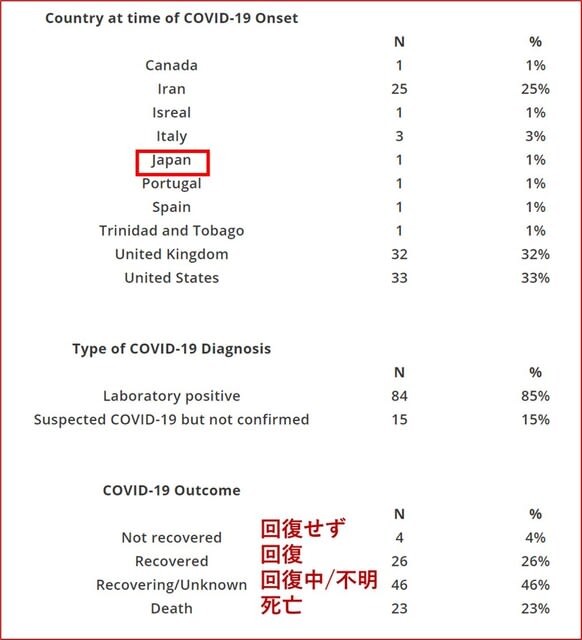
重症筋無力症患者は,免疫療法を行っていることからCOVID-19感染により予後が悪化するリスクがある.また感染自体が症状悪化の引き金となる.しかしリアルワールドで利用可能なエビデンスが乏しい.4月9日に,医師によるレジストリCOVID-19 Associated Risks and Effects in Myasthenia Gravis(CARE-MG)が開始された.これは国際MG/COVID-19ワーキンググループと脳神経内科医の共同作業である. 10月26日の段階で,日本からの1例を含む99例の登録がなされている.完全回復は26例(26%)で,COVID-19が原因で死亡した患者は23例(23%)であった(図3).COVID-19の感染が疾患の増悪を起こし,死亡率が高いことがすでに示されている.もし症例を経験したら,私達も登録を行いたい.症例登録は電子形式または紙形式での提出により行われ,データ入力にはおよそ10分かかる.追加の研究の詳細と症例提出の手順については,以下のURLを参照されたい.
https://myasthenia.org/Professionals/Resources-for-Professionals/CARE-MG
Lancet Neurol. 2020 Dec;19(12):970-971.(doi.org/10.1016/S1474-4422(20)30413-0)
◆小児でCOVID-19による重症化がまれな理由.
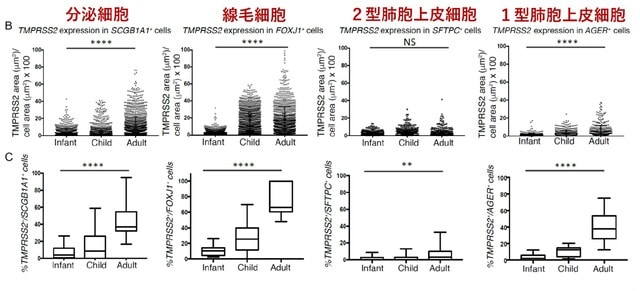
高齢者でCOVID-19による重症化のリスクは高く,逆に小児では比較的まれであるが,そのメカニズム十分にわかっていない.米国から蛋白分解酵素TMPRSS2の年齢依存性の発現変化により説明ができるという研究が報告された.まず基本的な知識として,ウイルスのスパイク蛋白質が,ヒト細胞のACE2受容体に結合したあと,蛋白分解酵素であるTMPRSS2で切断されてスパイク蛋白質が活性化されることが,ウイルス外膜とヒト細胞膜との融合(=感染)には重要である.この研究では,発達過程にあるマウス肺の単一細胞RNAシーケンシング(scRNA-seq)と,マウスおよびヒトの肺組織の免疫蛍光染色を統合した結果,TMPRSS2 の発現は線毛細胞および I 型肺胞上皮細胞で最も高いこと,そして,マウスおよびヒトでは加齢に伴い,TMPRSS2 の発現が増加することを明らかにした(図4).COVID-19患者の剖検組織の解析でも,気道上皮の分泌細胞と線毛細胞,末梢肺のI 型肺胞上皮細胞でウイルスRNAが最も多く検出され,かつウイルスRNAはTMPRSS2を発現する細胞に高頻度で局在していた.以上より,TMPRSS2の発現抑制が乳幼児や小児を重篤な呼吸器疾患から相対的に保護する基盤となっている可能性が示唆された.
J Clin Invest. Nov 12, 2020(doi.org/10.1172/JCI140766)
◆モデルナ社製ワクチンmRNA-1273の第1相試験.
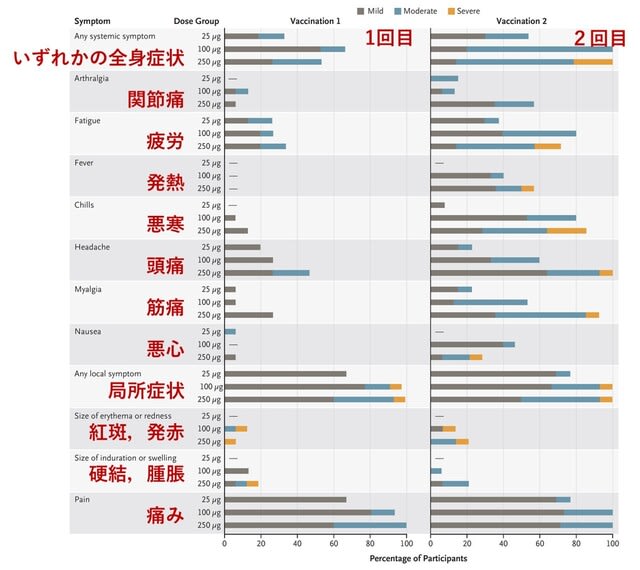
米国ファイザー社とともに期待されるモデルナ社製ワクチン候補mRNA-1273に関する第1相試験がNEJM誌に報告された.目的は安全性と,ヒトで中和抗体が誘導できるか明らかにすることである.このワクチンは,スパイク蛋白質に変異を導入し,感染前のperfusion conformationという安定化した構造をとらせることで,10倍もの抗体価の誘導を実現したものである.この研究は第 1 相,用量漸増,オープンラベル試験である.健康成人(18~55 歳) 45 名を対象に,ワクチン接種を 28 日間隔で 2 回,25 μg,100 μg,250 μg の投与量で行った(各群15名).1回目のワクチン接種後は,投与量が多いほど抗体反応が高くなった.2回目のワクチン接種後にさらに抗体力価は上昇した.血清中和活性はすべての参加者で検出され,その値は対照である回復期患者血清検体の分布の上半分の値と同等であった.また2ヶ月間で抗体価は維持された.半数以上の参加者で有害事象がみられ,疲労,悪寒,頭痛,筋肉痛,注射部位の痛みが含まれていた.全身性の有害事象は2回目の接種後,特に最高用量の接種群で多く見られた(1例は重篤で,39.6℃の高熱だった).以上,本ワクチンは全参加者に抗ウイルス免疫反応を誘導し,基本的に安全性に関する懸念は認めないと判断された. → 現在,3万人が参加した第3相が進行中である.日本はモデルナ社から来年1~6月中に2000万人分,ファイザー社から6月までに6000万人分のワクチン供給を受けることになっている.よって3万人の段階とは異なる未知の副作用が第4相試験(市販後調査)で出てくる可能性はある.接種を受けるかどうかは,今回及び第3相の科学的データをみて各自が慎重に判断する必要がある.
N Engl J Med. Nov 12, 2020(doi.org/10.1056/NEJMoa2022483)
地域によって第3波による医療崩壊が現実のものになってきました.医療崩壊はCOVID-19患者さんの診療や救命が困難になるだけでなく,他の疾患に対する通常の診療ができなくなることが大きな問題です.また医療者は自らが感染し,診療から離脱したり,院内感染を起こしたりすることを恐れています.第3波は行動様式をコロナ前に戻しても良いのだという意識変化がもたらされたことにより生じたのではないかと思います.初心に戻り,感染予防の基本を「粘り強く」遵守することが必要だと思います.
◆ダウン症候群のあるかたから学ぶべき教訓.
スペインからの報告.ダウン症候群では,免疫機能障害,呼吸器感染症,慢性炎症,早期高齢化がみられ,さらにCOVID-19 の危険因子となる併存疾患の有病率が高いという特徴がある.このためCOVID-19に対してダウン症候群患者が脆弱である恐れがある.ところがスペインのTrisomy 21 Research Societyが行った調査によると,ダウン症候群におけるCOVID-19感染は,2020年3~5月の第1波後,そして9月に第2波が生じて以降も大幅に減少している.著者らは,この感染率の低下は,ダウン症の人が有する,身だしなみや衛生面での「粘り強さ」によって説明できるのではないかと議論している.この議論が正しいとすれば,ダウン症の人々が示す行動パターンは,感染拡大を避けるために有用な教訓,もしくは注意喚起として役立つであろう.
Lancet Neurol. Dec, 2020(doi.org/10.1016/S1474-4422(20)30401-4)
◆COVID-19入院患者の退院60日まで観察ではさまざまな予後が不良である.
COVID-19患者の入院中の転帰に関する報告は多いものの,退院後の長期の転帰はよく分かっていない.米国ミシガン州の38病院から,入院患者1648名(中央値62歳)の退院後 60 日間の転帰を明らかにした研究が報告された.398名(24.2%)が入院中に死亡した.退院した残1250名のうち,975名(78.0%)が自宅に帰り,158名(12.6%)が看護師のいる療養施設・リハビリテーション施設に退院した.退院後60日までに,さらに84名の患者(6.7%,ICU入室者の10.4%)が死亡した.以上よりコホート全体の死亡率は29.2%,ICU治療を受けた405名の死亡率は63.5%と高率であった.退院後60日以内に189名(病院生存者の15.1%)が再入院した.また65名は60日後でも味覚や嗅覚の喪失を認めた.入院前に就業していた195名のうち,78名は健康上の問題,または仕事を失って復職できなかった.28名が退院後にメンタルヘルスのケアを求めた.179名の患者が少なくとも軽度の経済的影響を受け,47名が貯蓄の大部分または全部を使い果たした.→ 国によって入院の条件も異なるため,単純に日本に当てはめられないものの,長期的なさまざまな予後が不良であることを考慮すると,とにかくCOVID-19を甘く見ず感染者を拡大させないこと,ならびに生存者を支援する制度をつくることが必要である.
Ann Intern Med. Nov 11, 2020(doi.org/10.7326/M20-5661)
◆長期の予後不良に関わる横隔膜筋症.
呼吸に関わる主要な筋である横隔膜に焦点を当てたオランダからの研究.COVID-19により死亡した26名(中央値71歳)の剖検時に横隔膜筋標本を採取した.対照群として,他の疾患で死亡した8名の剖検標本を使用した.COVID-19患者のうち24 例(92.3%)が侵襲的機械換気を受け,その中央値は12 日間であった.ACE2は主に筋線維膜に局在し(図1A),SARS-CoV-2ウイルスが横隔膜に感染するための入り口となると考えられた.実際に横隔膜でウイルスRNAが検出されたのは4名(15.4%)であった.ウイルスRNAは横隔膜の筋線維内に局在していた.発現遺伝子の解析では,線維化に関わるFGFシグナルが活性化していた.実際に免疫染色で,COVID-19患者では線維化が2倍以上高度であった(図1C).横隔膜筋障害がSARS-CoV-2ウイルスによる直接的な変化であるかは不明であるが,COVID-19感染に伴う高度の横隔膜筋障害がその脱力につながり,退院しても人工呼吸器離脱困難,持続的な呼吸困難,疲労につながる可能性がある.
JAMA Intern Med. Nov 16, 2020(doi.org/10.1001/jamainternmed.2020.6278)

◆動物実験で鼻粘膜への感染により,ウイルスは速やかに脳へ移行する.
米国からの研究.上皮細胞特異性発現K18プロモーターにより,ヒトのACE2を発現するモデルマウスを作成し,感染実験を行った研究が報告された.この実験系では,SARS-CoV2ウイルスは上皮細胞にのみ感染し,嗅細胞には感染を認めないが,なんと脳では感染後2日,4日,6日と経時的に,他の臓器よりも多くウイルスが検出されるようになる(図2上).具体的には,ウイルス105 PFUを経鼻接種すると,5/8匹のマウス脳から感染性ウイルスが検出された.感染後4および6日目にウイルスヌクレオカプシド(N)タンパク質の免疫染色を行ったところ,4日後では染色されなかったが,6日後では嗅球,大脳皮質,馬尾・翼状突起,視床,視床下部,腹側線条体を含むいくつかの脳領域で染色が観察された(図2下).HE染色では,視床で細胞死と血栓が認められ,細胞死の病巣が変性上衣細胞に隣接して検出された.影響を受けた領域のほとんどが嗅球の二次的,三次的に連絡するのに対し,いくつかの領域,例えば,後眼球と舌下神経核のような領域は,直接連絡していない.この結果は,脳へのウイルス伝播における嗅球感染の役割を示唆するものの,ウイルスが他のルートで中枢神経系に入る可能性を示唆する.→ このデータを見ると,ヒトでもウイルスが脳に移行し,将来,再活性化する可能性があるのではないかと危惧される.
Nature. 2020 Nov 9.(doi.org/10.1038/s41586-020-2943-z)

◆神経難病のケア(1)ALSの集学的ケアは遠隔診療でも十分可能である.
集学的ALSケアは,生存期間を延長し,患者と介護者の生活の質を向上させる.しかしパンデミックにより,直接のケアが困難な状況になった.大流行が生じたイタリアから,第三次ALSセンターの遠隔医療の効果に関する検討が報告された.19名のALS患者を,脳神経内科医,管理栄養士(食事・体重モニタリング),心理士(心理的評価・支援),理学療法士(理学療法治療・機器の処方)から構成される集学的チームが,遠隔医療により診療を行った.結果的に,すべての患者は,リモートではあるものの医療の専門家と対面で話すことについて肯定的な認識を示し,チームが自分の問題を理解していることに満足していた.さまざまな医療行為が行われ,処方内容の変更が11/19例,非侵襲的陽圧呼吸(NPPV)管理の開始が2/19例,機器の処方が9/16例で行われた.ALSFRS-Rの月平均低下率は,遠隔医療開始前は0.88,開始後は0.49と改善した.体重と1日のカロリー摂取量も安定していた. 不安・うつスコアは改善し,QOLスコアも安定していた. → ALSの集学的ケアは遠隔診療でも十分可能であり,今後はさらに患者のニーズに応じた個別化プログラムを検討するとのこと!
Acta Neuropathol. Nov 13, 2020(doi.org/10.1111/ane.13373)
◆神経難病のケア(2)COVID-19に感染した重症筋無力症の国際的な患者登録(レジストリ)の開始.
重症筋無力症患者は,免疫療法を行っていることからCOVID-19感染により予後が悪化するリスクがある.また感染自体が症状悪化の引き金となる.しかしリアルワールドで利用可能なエビデンスが乏しい.4月9日に,医師によるレジストリCOVID-19 Associated Risks and Effects in Myasthenia Gravis(CARE-MG)が開始された.これは国際MG/COVID-19ワーキンググループと脳神経内科医の共同作業である. 10月26日の段階で,日本からの1例を含む99例の登録がなされている.完全回復は26例(26%)で,COVID-19が原因で死亡した患者は23例(23%)であった(図3).COVID-19の感染が疾患の増悪を起こし,死亡率が高いことがすでに示されている.もし症例を経験したら,私達も登録を行いたい.症例登録は電子形式または紙形式での提出により行われ,データ入力にはおよそ10分かかる.追加の研究の詳細と症例提出の手順については,以下のURLを参照されたい.
https://myasthenia.org/Professionals/Resources-for-Professionals/CARE-MG
Lancet Neurol. 2020 Dec;19(12):970-971.(doi.org/10.1016/S1474-4422(20)30413-0)

◆小児でCOVID-19による重症化がまれな理由.
高齢者でCOVID-19による重症化のリスクは高く,逆に小児では比較的まれであるが,そのメカニズム十分にわかっていない.米国から蛋白分解酵素TMPRSS2の年齢依存性の発現変化により説明ができるという研究が報告された.まず基本的な知識として,ウイルスのスパイク蛋白質が,ヒト細胞のACE2受容体に結合したあと,蛋白分解酵素であるTMPRSS2で切断されてスパイク蛋白質が活性化されることが,ウイルス外膜とヒト細胞膜との融合(=感染)には重要である.この研究では,発達過程にあるマウス肺の単一細胞RNAシーケンシング(scRNA-seq)と,マウスおよびヒトの肺組織の免疫蛍光染色を統合した結果,TMPRSS2 の発現は線毛細胞および I 型肺胞上皮細胞で最も高いこと,そして,マウスおよびヒトでは加齢に伴い,TMPRSS2 の発現が増加することを明らかにした(図4).COVID-19患者の剖検組織の解析でも,気道上皮の分泌細胞と線毛細胞,末梢肺のI 型肺胞上皮細胞でウイルスRNAが最も多く検出され,かつウイルスRNAはTMPRSS2を発現する細胞に高頻度で局在していた.以上より,TMPRSS2の発現抑制が乳幼児や小児を重篤な呼吸器疾患から相対的に保護する基盤となっている可能性が示唆された.
J Clin Invest. Nov 12, 2020(doi.org/10.1172/JCI140766)

◆モデルナ社製ワクチンmRNA-1273の第1相試験.
米国ファイザー社とともに期待されるモデルナ社製ワクチン候補mRNA-1273に関する第1相試験がNEJM誌に報告された.目的は安全性と,ヒトで中和抗体が誘導できるか明らかにすることである.このワクチンは,スパイク蛋白質に変異を導入し,感染前のperfusion conformationという安定化した構造をとらせることで,10倍もの抗体価の誘導を実現したものである.この研究は第 1 相,用量漸増,オープンラベル試験である.健康成人(18~55 歳) 45 名を対象に,ワクチン接種を 28 日間隔で 2 回,25 μg,100 μg,250 μg の投与量で行った(各群15名).1回目のワクチン接種後は,投与量が多いほど抗体反応が高くなった.2回目のワクチン接種後にさらに抗体力価は上昇した.血清中和活性はすべての参加者で検出され,その値は対照である回復期患者血清検体の分布の上半分の値と同等であった.また2ヶ月間で抗体価は維持された.半数以上の参加者で有害事象がみられ,疲労,悪寒,頭痛,筋肉痛,注射部位の痛みが含まれていた.全身性の有害事象は2回目の接種後,特に最高用量の接種群で多く見られた(1例は重篤で,39.6℃の高熱だった).以上,本ワクチンは全参加者に抗ウイルス免疫反応を誘導し,基本的に安全性に関する懸念は認めないと判断された. → 現在,3万人が参加した第3相が進行中である.日本はモデルナ社から来年1~6月中に2000万人分,ファイザー社から6月までに6000万人分のワクチン供給を受けることになっている.よって3万人の段階とは異なる未知の副作用が第4相試験(市販後調査)で出てくる可能性はある.接種を受けるかどうかは,今回及び第3相の科学的データをみて各自が慎重に判断する必要がある.
N Engl J Med. Nov 12, 2020(doi.org/10.1056/NEJMoa2022483)


























