今回のキーワードは80歳以上男性の感染致死率の高さ,英国におけるワクチン接種順位,隔離期間の短縮と残存感染リスク,2ヶ月間以上,感染力をもつウイルスを排出する患者の特徴,中枢神経血管内皮細胞における初のウイルスタンパク質の検出,4薬剤のドラッグリポジショニングの結果,肺の線維化と肺移植,モデルナ社ワクチン第1相試験の続報です.
この1週間は身近に感染が迫ってきたと実感する出来事が何度かありました.またCOVID-19対応のため,他の疾患の患者さんの医療への影響が避けられない状況になりつつあります.年末年始以降,目を覆うばかりの状況になるのを避けるためには,感染流行地域とそれ以外の地域の往来の制限は必要ではないかと思います.
◆80歳以上男性の感染致死率は12~16%.
スペインの4689万人の6月22日までのSARS-CoV-2に対する抗体保有率は4.9%(230万人)であった.全体の感染致死リスクは,確定死亡で0.8~1.1%(230万人中19228人)であった.感染致死リスクは,男性では1.1~1.4%,女性では0.6%~0.8%であった.感染致死リスクは50歳以降に急激に増加し,とくに男性において顕著だった(図1).80歳以上では,男性の12~16%,女性の5~6%が死亡した.季節性インフルエンザなどの他の一般的な呼吸器疾患で報告されているものよりも,COVID-19による致死率は高い.→ 新型コロナがただの風邪のはずはなく,高齢者を感染から守る必要がある.
BMJ. Nov 27, 2020(doi.org/10.1136/bmj.m4509)

◆英国におけるPfizer/BioNTechのワクチン接種順位.
世界で初めてのCOVID-19予防ワクチンの承認国となった英国では,来週から80万回投与分のワクチンが使用される.3週間間隔で2回接種される.注文した4000万回分は,英国の人口の1/3にワクチン接種するのに十分な量である.優先順位リストがGOV.UKに掲載されていた.
1)高齢者向けケアホームの入居者とその職員
2)80歳以上の人,第一線の医療・福祉従事者
3)75歳以上の人
4)70歳以上の人と臨床的に極めて脆弱な人
5)65歳以上の人
6)重篤な疾患や死亡リスクの高い基礎疾患を持つ16~64歳の人
7)60歳以上の人
8)55歳以上の人
9)50歳以上の人
日本でもおそらく類似した基準が採用されるものと思われる.図2は筆者によるCOVID-19神経筋合併症の病態だが,ワクチン後の副反応として「感染後免疫介在性反応」と同じ病態が生じうるリスクはある.今後,脳神経内科医はワクチン接種後の副反応も念頭において鑑別診断を行う必要がある.
https://www.gov.uk/government/news/COVID-19-vaccine-authorised-by-medicines-regulator

◆隔離(1).隔離期間の短縮と残存感染リスク.
自身の周辺でも感染者や濃厚接触者に遭遇するリスクが高くなってきたと実感している.隔離期間の考え方について,アメリカ疾病予防管理センター(CDC)を確認してみた.CDCは基本的に14日間の隔離を推奨している.ただ隔離期間を短縮するための代替案も最近,発表されている(図3).これによると①PCRを行わず,毎日の経過観察で症状がない場合,10日間で隔離を終了できる.ただし終了後の残存感染リスクは約1%,上限は約10%と推定される.②施行したPCRが陰性で,毎日の経過観察で症状がない場合は,7日間で隔離を終了できる.ただし終了後の残存感染リスクは約5%,上限は約12%と推定される.いずれの場合も,終了後14日目まで症状の経過観察を継続し,マスクを着用するなどの必要がある.→ 感染者にマスク無しで接触した場合,PCR偽陰性の可能性を考えると最低7日間は隔離が必要である.マスクは必ずすべきである.またPCR陰性だけでは感染リスクは否定されないことを再度認識する必要がある.
CDC. Dec. 2, 2020(https://www.cdc.gov/coronavirus/2019-ncov/more/scientific-brief-options-to-reduce-quarantine.html)

◆隔離(2).2ヶ月間以上,感染力をもつウイルスを排出する患者の特徴.
米国からの報告. COVID-19に感染した免疫不全患者20名(造血幹細胞移植またはCAR(キメラ抗原受容体)-T細胞療法のレシピエント18名およびリンパ腫患者2名)から,鼻咽頭および喀痰サンプルを連続的に採取し,感染力のあるウイルスを検出するためにベロ細胞を用いて培養を行った.この結果,20日以上,感染力のあるウイルスを排出した患者が3名いた.過去6ヵ月以内に同種造血幹細胞移植(2名)またはCAR-T細胞療法(1名)を受け,ウイルス核タンパクに対する抗体は陰性のままであった.全ゲノムシークエンシングの結果,各患者は別個のウイルスに感染しており,また持続感染と考えられた.以上より,造血幹細胞移植後,またはCAR-T細胞治療後に免疫抑制療法を行っている患者では,少なくとも2ヶ月間,感染力のあるSARS-CoV-2を排出する可能性がある.患者隔離のガイドラインにおいて,免疫不全患者に関しては改訂が必要であろう.
New Engl J Med. Dec 1, 2020(doi.org/10.1056/NEJMc2031670)
◆中枢神経血管内皮細胞における初のウイルスタンパク質の検出.
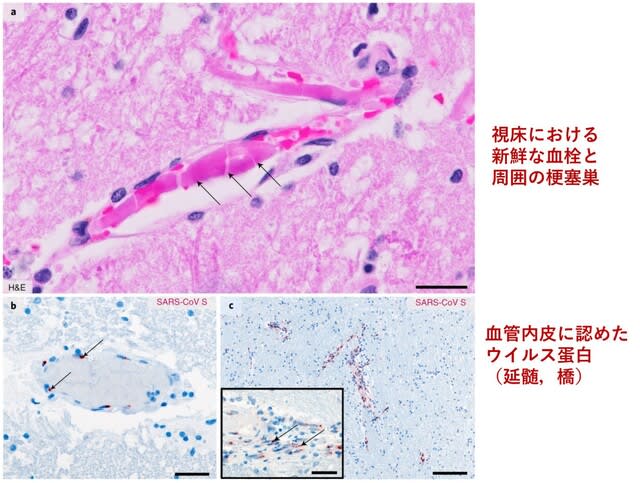
ドイツからの報告.SARS-CoV-2ウイルスが中枢神経系に侵入する可能性が高いことは複数の研究で指摘されている.今回,病理学的にウイルスが,嗅粘膜の神経-粘膜界面を通過し,軸索輸送を介して,血管内皮細胞,神経組織(嗅神経や感覚神経終末を含む),さらに延髄の呼吸・心血管中枢を含む領域に侵入しているという病理学的検討が報告された.図4aは視床のHE染色で,小血管内に新鮮な血栓(矢印)を認めている.また梗塞をきたした脳幹の小血管の内皮細胞(bは延髄,cは橋)の細胞質に,ウイルスタンパク質が同定された!内皮細胞に感染したウイルスは血管障害を助長し,時間経過とともに他の脳領域へのウイルスの拡散を促進,最終的には様々な要因に依存するものの,より重篤な,もしくは慢性的な病態(持続感染)に関与する可能性がある.また小脳のような嗅粘膜とは直接関係のない領域でもウイルスRNAが検出されたことから,中枢神経系へのウイルス侵入には,軸索輸送以外の機序がある可能性が示唆された(例えば,ウイルスを運搬する白血球の血液脳関門通過など).
Nat Neurosci. Nov 30, 2020(doi.org/10.1038/s41593-020-00758-5)
◆治療(1).代表的な4薬剤のドラッグリポジショニングは失敗した.
ドラッグリポジショニング(drug repositionin)とは,既存のある疾患に有効な治療薬から,別の疾患に有効な薬効を見つけ出すことである.COVID-19に対しても第1波からこの戦略が取られ,世界中でその効果が期待された.WHOはこの戦略に基づいて,4つの抗ウイルス薬(レムデシビル,ヒドロキシクロロキン,ロピナビル,インターフェロンβ1a)の効果を入院患者において検証した.30カ国405病院,1万1330人の成人が以下のように無作為に割り付けられた(レムデシビル2750名,ヒドロキシクロロキン954名,ロピナビル1411名,インターフェロンβ1a 2063名,標準治療4088名).結果として,計1253名が中央値8日目に死亡した.28日死亡率は11.8%であった(無作為化時に人工呼吸器管理であった場合は39.0%).対照群との比較で,レムデシビル群は死亡率比0.95(95%CI,0.81~1.11),ヒドロキシクロロキン群1.19(0.89~1.59),ロピナビル群1.00(0.79~1.25),インターフェロン群1.16(0.96~1.39)で,いずれも全死亡率を低下させなかった(図5).さらに人工呼吸器の開始,入院期間にも影響を及ぼさなかった.COVID-19に対するドラッグリポジショニングは今までのところうまく行っていない.
New Engl J Med. Dec 2, 2020(doi.org/10.1056/NEJMoa2023184)

◆治療(2).治療抵抗性呼吸不全の原因としての肺の線維化と肺移植による救命.
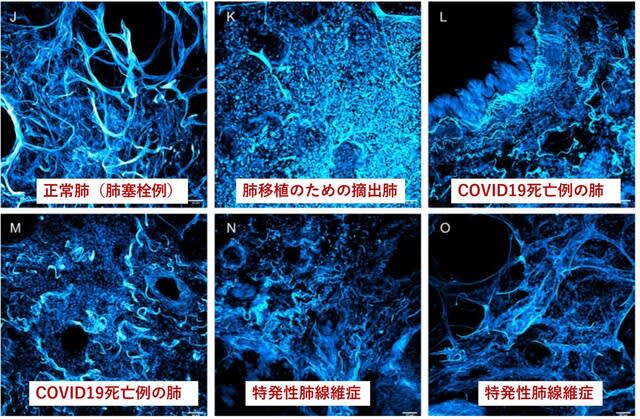
米国から治療抵抗性COVID-19関連呼吸不全に対して肺移植を受けた3名の摘出肺組織と,COVID-19関連肺炎で死亡した2名の肺組織を検討した研究が報告された.まず単一分子蛍光の in situハイブリダイゼーションを用いて肺組織からウイルスの同定を試みたが検出されなかった.しかし病理学的に進行期の肺線維症に似た肺損傷と線維化を認めた(図6).機械学習を用いて,COVID-19患者肺と肺線維症患者から得られたシングルセルRNAシークエンスデータを比較したところ,遺伝子発現に類似性を認めた.以上より,COVID-19重症呼吸不全患者では肺線維症が生じること,生存のための唯一の選択肢として肺移植があることが示された.肺移植の適応として,4~6週人工呼吸器管理を行っても離脱困難な症例,2度のPCR陰性,患者の同意,両側肺移植が望ましいなども記載されている.
Sci Transl Med. Nov 30, 2020(doi.org/10.1126/scitranslmed.abe4282)
◆治療(3).モデルナ社ワクチン第1相試験の続報.
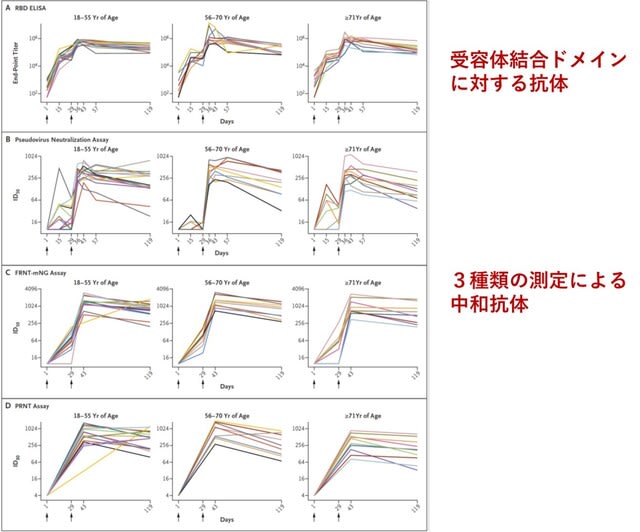
モデルナ社のメッセンジャーRNAワクチンmRNA-1273の第1相試験34名(初回接種から57日まで)の結果はすでに報告されている.ワクチンは28日間隔で2回行われた.100μg の用量では,mRNA-1273 は高レベルの結合抗体および中和抗体を産生した.今回,最初の投与から119日後,2回目投与から90日後の結果が報告された.予想通り,時間の経過とともにわずかに減少したが,3つの年齢で分けた群において,90日後もすべての参加者で上昇したままで,血清中和抗体は 119 日後にも全参加者で検出された(図7).57日目以降もワクチンに関連した新たな有害事象は発生しなかった.以上より,mRNA-1273 が持続的な体液性免疫をもたらす可能性が示唆された.13ヶ月間のフォローアップ解析が進行中である.また現在進行中の第 3 相試験において100μg の用量を用いることを支持する結果である.
NEJM. December 3, 2020(doi.org/10.1056/NEJMc2032195)
この1週間は身近に感染が迫ってきたと実感する出来事が何度かありました.またCOVID-19対応のため,他の疾患の患者さんの医療への影響が避けられない状況になりつつあります.年末年始以降,目を覆うばかりの状況になるのを避けるためには,感染流行地域とそれ以外の地域の往来の制限は必要ではないかと思います.
◆80歳以上男性の感染致死率は12~16%.
スペインの4689万人の6月22日までのSARS-CoV-2に対する抗体保有率は4.9%(230万人)であった.全体の感染致死リスクは,確定死亡で0.8~1.1%(230万人中19228人)であった.感染致死リスクは,男性では1.1~1.4%,女性では0.6%~0.8%であった.感染致死リスクは50歳以降に急激に増加し,とくに男性において顕著だった(図1).80歳以上では,男性の12~16%,女性の5~6%が死亡した.季節性インフルエンザなどの他の一般的な呼吸器疾患で報告されているものよりも,COVID-19による致死率は高い.→ 新型コロナがただの風邪のはずはなく,高齢者を感染から守る必要がある.
BMJ. Nov 27, 2020(doi.org/10.1136/bmj.m4509)

◆英国におけるPfizer/BioNTechのワクチン接種順位.
世界で初めてのCOVID-19予防ワクチンの承認国となった英国では,来週から80万回投与分のワクチンが使用される.3週間間隔で2回接種される.注文した4000万回分は,英国の人口の1/3にワクチン接種するのに十分な量である.優先順位リストがGOV.UKに掲載されていた.
1)高齢者向けケアホームの入居者とその職員
2)80歳以上の人,第一線の医療・福祉従事者
3)75歳以上の人
4)70歳以上の人と臨床的に極めて脆弱な人
5)65歳以上の人
6)重篤な疾患や死亡リスクの高い基礎疾患を持つ16~64歳の人
7)60歳以上の人
8)55歳以上の人
9)50歳以上の人
日本でもおそらく類似した基準が採用されるものと思われる.図2は筆者によるCOVID-19神経筋合併症の病態だが,ワクチン後の副反応として「感染後免疫介在性反応」と同じ病態が生じうるリスクはある.今後,脳神経内科医はワクチン接種後の副反応も念頭において鑑別診断を行う必要がある.
https://www.gov.uk/government/news/COVID-19-vaccine-authorised-by-medicines-regulator

◆隔離(1).隔離期間の短縮と残存感染リスク.
自身の周辺でも感染者や濃厚接触者に遭遇するリスクが高くなってきたと実感している.隔離期間の考え方について,アメリカ疾病予防管理センター(CDC)を確認してみた.CDCは基本的に14日間の隔離を推奨している.ただ隔離期間を短縮するための代替案も最近,発表されている(図3).これによると①PCRを行わず,毎日の経過観察で症状がない場合,10日間で隔離を終了できる.ただし終了後の残存感染リスクは約1%,上限は約10%と推定される.②施行したPCRが陰性で,毎日の経過観察で症状がない場合は,7日間で隔離を終了できる.ただし終了後の残存感染リスクは約5%,上限は約12%と推定される.いずれの場合も,終了後14日目まで症状の経過観察を継続し,マスクを着用するなどの必要がある.→ 感染者にマスク無しで接触した場合,PCR偽陰性の可能性を考えると最低7日間は隔離が必要である.マスクは必ずすべきである.またPCR陰性だけでは感染リスクは否定されないことを再度認識する必要がある.
CDC. Dec. 2, 2020(https://www.cdc.gov/coronavirus/2019-ncov/more/scientific-brief-options-to-reduce-quarantine.html)

◆隔離(2).2ヶ月間以上,感染力をもつウイルスを排出する患者の特徴.
米国からの報告. COVID-19に感染した免疫不全患者20名(造血幹細胞移植またはCAR(キメラ抗原受容体)-T細胞療法のレシピエント18名およびリンパ腫患者2名)から,鼻咽頭および喀痰サンプルを連続的に採取し,感染力のあるウイルスを検出するためにベロ細胞を用いて培養を行った.この結果,20日以上,感染力のあるウイルスを排出した患者が3名いた.過去6ヵ月以内に同種造血幹細胞移植(2名)またはCAR-T細胞療法(1名)を受け,ウイルス核タンパクに対する抗体は陰性のままであった.全ゲノムシークエンシングの結果,各患者は別個のウイルスに感染しており,また持続感染と考えられた.以上より,造血幹細胞移植後,またはCAR-T細胞治療後に免疫抑制療法を行っている患者では,少なくとも2ヶ月間,感染力のあるSARS-CoV-2を排出する可能性がある.患者隔離のガイドラインにおいて,免疫不全患者に関しては改訂が必要であろう.
New Engl J Med. Dec 1, 2020(doi.org/10.1056/NEJMc2031670)
◆中枢神経血管内皮細胞における初のウイルスタンパク質の検出.
ドイツからの報告.SARS-CoV-2ウイルスが中枢神経系に侵入する可能性が高いことは複数の研究で指摘されている.今回,病理学的にウイルスが,嗅粘膜の神経-粘膜界面を通過し,軸索輸送を介して,血管内皮細胞,神経組織(嗅神経や感覚神経終末を含む),さらに延髄の呼吸・心血管中枢を含む領域に侵入しているという病理学的検討が報告された.図4aは視床のHE染色で,小血管内に新鮮な血栓(矢印)を認めている.また梗塞をきたした脳幹の小血管の内皮細胞(bは延髄,cは橋)の細胞質に,ウイルスタンパク質が同定された!内皮細胞に感染したウイルスは血管障害を助長し,時間経過とともに他の脳領域へのウイルスの拡散を促進,最終的には様々な要因に依存するものの,より重篤な,もしくは慢性的な病態(持続感染)に関与する可能性がある.また小脳のような嗅粘膜とは直接関係のない領域でもウイルスRNAが検出されたことから,中枢神経系へのウイルス侵入には,軸索輸送以外の機序がある可能性が示唆された(例えば,ウイルスを運搬する白血球の血液脳関門通過など).
Nat Neurosci. Nov 30, 2020(doi.org/10.1038/s41593-020-00758-5)

◆治療(1).代表的な4薬剤のドラッグリポジショニングは失敗した.
ドラッグリポジショニング(drug repositionin)とは,既存のある疾患に有効な治療薬から,別の疾患に有効な薬効を見つけ出すことである.COVID-19に対しても第1波からこの戦略が取られ,世界中でその効果が期待された.WHOはこの戦略に基づいて,4つの抗ウイルス薬(レムデシビル,ヒドロキシクロロキン,ロピナビル,インターフェロンβ1a)の効果を入院患者において検証した.30カ国405病院,1万1330人の成人が以下のように無作為に割り付けられた(レムデシビル2750名,ヒドロキシクロロキン954名,ロピナビル1411名,インターフェロンβ1a 2063名,標準治療4088名).結果として,計1253名が中央値8日目に死亡した.28日死亡率は11.8%であった(無作為化時に人工呼吸器管理であった場合は39.0%).対照群との比較で,レムデシビル群は死亡率比0.95(95%CI,0.81~1.11),ヒドロキシクロロキン群1.19(0.89~1.59),ロピナビル群1.00(0.79~1.25),インターフェロン群1.16(0.96~1.39)で,いずれも全死亡率を低下させなかった(図5).さらに人工呼吸器の開始,入院期間にも影響を及ぼさなかった.COVID-19に対するドラッグリポジショニングは今までのところうまく行っていない.
New Engl J Med. Dec 2, 2020(doi.org/10.1056/NEJMoa2023184)

◆治療(2).治療抵抗性呼吸不全の原因としての肺の線維化と肺移植による救命.
米国から治療抵抗性COVID-19関連呼吸不全に対して肺移植を受けた3名の摘出肺組織と,COVID-19関連肺炎で死亡した2名の肺組織を検討した研究が報告された.まず単一分子蛍光の in situハイブリダイゼーションを用いて肺組織からウイルスの同定を試みたが検出されなかった.しかし病理学的に進行期の肺線維症に似た肺損傷と線維化を認めた(図6).機械学習を用いて,COVID-19患者肺と肺線維症患者から得られたシングルセルRNAシークエンスデータを比較したところ,遺伝子発現に類似性を認めた.以上より,COVID-19重症呼吸不全患者では肺線維症が生じること,生存のための唯一の選択肢として肺移植があることが示された.肺移植の適応として,4~6週人工呼吸器管理を行っても離脱困難な症例,2度のPCR陰性,患者の同意,両側肺移植が望ましいなども記載されている.
Sci Transl Med. Nov 30, 2020(doi.org/10.1126/scitranslmed.abe4282)

◆治療(3).モデルナ社ワクチン第1相試験の続報.
モデルナ社のメッセンジャーRNAワクチンmRNA-1273の第1相試験34名(初回接種から57日まで)の結果はすでに報告されている.ワクチンは28日間隔で2回行われた.100μg の用量では,mRNA-1273 は高レベルの結合抗体および中和抗体を産生した.今回,最初の投与から119日後,2回目投与から90日後の結果が報告された.予想通り,時間の経過とともにわずかに減少したが,3つの年齢で分けた群において,90日後もすべての参加者で上昇したままで,血清中和抗体は 119 日後にも全参加者で検出された(図7).57日目以降もワクチンに関連した新たな有害事象は発生しなかった.以上より,mRNA-1273 が持続的な体液性免疫をもたらす可能性が示唆された.13ヶ月間のフォローアップ解析が進行中である.また現在進行中の第 3 相試験において100μg の用量を用いることを支持する結果である.
NEJM. December 3, 2020(doi.org/10.1056/NEJMc2032195)


























