自己免疫脳炎の代表的疾患である抗NMDAR脳炎は,精神症状,記銘力障害,痙攣発作,運動異常症,意識障害,中枢性低換気などを呈する若年女性にみられる脳炎です.急性期から積極的な免疫療法を行うことが重要で,第1選択療法でうまくいかないとき,速やかにリツキシマブなどの第2選択療法に踏み切れるかが重要です.ただし現在の治療は,広範な免疫抑制ないし非選択的抗体除去ですので,限界があり副作用も問題になります.
今回,Cell誌に,ドイツからCAR-T細胞療法でNMDAR抗体を作るB細胞を選択的に除去するという研究が報告されました! CAR-T細胞療法は脳神経内科では馴染みがありませんが,急性リンパ性白血病や悪性リンパ腫といった血液がんに大きな進歩をもたらした治療です.少し解説すると,近年,T細胞免疫療法において,キメラ抗原受容体(chimeric antigen receptor: CAR)をもつ遺伝子改変CAR-T細胞の開発が盛んに行われています.CARは腫瘍抗原特異的TCRや抗体を改変して作成した受容体です.一般的に受容体には細胞外領域に抗体の可変領域(抗原認識部位)が配置され,細胞内領域にTCRの一部であるCD3や共刺激分子CD28,CD137の細胞内領域(活性化シグナル伝達領域)が配置されます.そして患者末梢血に存在するT細胞を採取して,ウイルスベクターで受容体を導入して,体外でCAR-T細胞を大量に作ることができます.これを再び体内に戻します.
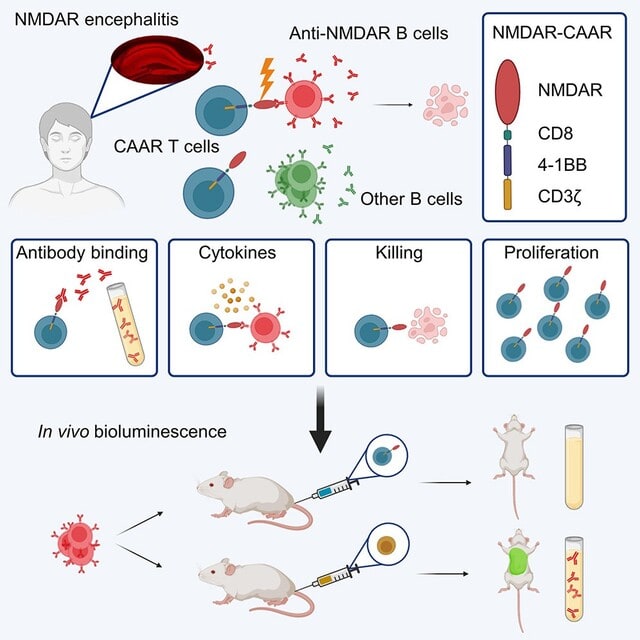
この論文では,まずNMDARの自己抗体遺伝子を14種類クローニングし,ほぼすべてに反応する NMDA受容体の遺伝子構成を決め,それに細胞内の4-1BB/CD3ζドメインを融合させたキメラ遺伝子を作成し,T細胞に発現させています.そうしてできたNMDAR-CAAR T細胞は,患者由来の自己抗体を認識し,サイトカインを放出し,増殖します(図).NMDAR-CAAR T細胞は,In vitroにて標的細胞に対する細胞傷害性を示し,またマウス動物モデルにおいて,抗NMDAR B細胞株を枯渇させ,自己抗体レベルを持続的に低下させることができました.病理学的に標的細胞以外に障害はなく,また標的細胞が少ないため,CAR-T細胞療法の安全上の懸念であるサイトカインストームも生じませんでした.
まだ前臨床研究の段階ですが,抗NMDAR脳炎におけるCAAR T細胞の第I/II相試験への道を開く研究といえます.もしこの治療が臨床応用されると副作用の軽減,長期予後の改善,再発予防が期待できます.同様のCAR-T細胞療法を用いた治療研究は重症筋無力症でも報告されており(Phase 1b/2a),16名の検討で,安全であり,忍容性も良好と報告されています.
近未来の脳神経内科はCAR-T細胞療法を行うことになりそうです.
Granit V, et al. Lancet Neurol. 2023 Jul;22(7):578-590.(doi.org/10.1016/S1474-4422(23)00194-1.)
Reincke SM, et al. Cell. 2023 Oct 26:S0092-8674(23)01083-8.(doi.org/10.1016/j.cell.2023.10.001)
今回,Cell誌に,ドイツからCAR-T細胞療法でNMDAR抗体を作るB細胞を選択的に除去するという研究が報告されました! CAR-T細胞療法は脳神経内科では馴染みがありませんが,急性リンパ性白血病や悪性リンパ腫といった血液がんに大きな進歩をもたらした治療です.少し解説すると,近年,T細胞免疫療法において,キメラ抗原受容体(chimeric antigen receptor: CAR)をもつ遺伝子改変CAR-T細胞の開発が盛んに行われています.CARは腫瘍抗原特異的TCRや抗体を改変して作成した受容体です.一般的に受容体には細胞外領域に抗体の可変領域(抗原認識部位)が配置され,細胞内領域にTCRの一部であるCD3や共刺激分子CD28,CD137の細胞内領域(活性化シグナル伝達領域)が配置されます.そして患者末梢血に存在するT細胞を採取して,ウイルスベクターで受容体を導入して,体外でCAR-T細胞を大量に作ることができます.これを再び体内に戻します.
この論文では,まずNMDARの自己抗体遺伝子を14種類クローニングし,ほぼすべてに反応する NMDA受容体の遺伝子構成を決め,それに細胞内の4-1BB/CD3ζドメインを融合させたキメラ遺伝子を作成し,T細胞に発現させています.そうしてできたNMDAR-CAAR T細胞は,患者由来の自己抗体を認識し,サイトカインを放出し,増殖します(図).NMDAR-CAAR T細胞は,In vitroにて標的細胞に対する細胞傷害性を示し,またマウス動物モデルにおいて,抗NMDAR B細胞株を枯渇させ,自己抗体レベルを持続的に低下させることができました.病理学的に標的細胞以外に障害はなく,また標的細胞が少ないため,CAR-T細胞療法の安全上の懸念であるサイトカインストームも生じませんでした.

まだ前臨床研究の段階ですが,抗NMDAR脳炎におけるCAAR T細胞の第I/II相試験への道を開く研究といえます.もしこの治療が臨床応用されると副作用の軽減,長期予後の改善,再発予防が期待できます.同様のCAR-T細胞療法を用いた治療研究は重症筋無力症でも報告されており(Phase 1b/2a),16名の検討で,安全であり,忍容性も良好と報告されています.
近未来の脳神経内科はCAR-T細胞療法を行うことになりそうです.
Granit V, et al. Lancet Neurol. 2023 Jul;22(7):578-590.(doi.org/10.1016/S1474-4422(23)00194-1.)
Reincke SM, et al. Cell. 2023 Oct 26:S0092-8674(23)01083-8.(doi.org/10.1016/j.cell.2023.10.001)

























